回答下列问题:
(1)氢氧燃料电池在电解质溶液为KOH溶液时,写出氢氧燃料电池工作时的负极电极反应式:_____
(2)在浓硝酸中放入铜片:开始反应的化学方程式为_______ ;若铜有剩余,则反应将要结束时的化学方程式_______ 。
(3)标准状状况下,排空法收集氯化氢气体,做喷泉实验时,如果气体没有溢出,实验完成时所得溶液的物质的量浓度为_______ mol/L(保留两位有效数字)
(4)SiO2在自然界中广泛存在,它是制备现代通讯材料_______ (写该材料名称)的主要原料。
(1)氢氧燃料电池在电解质溶液为KOH溶液时,写出氢氧燃料电池工作时的负极电极反应式:
(2)在浓硝酸中放入铜片:开始反应的化学方程式为
(3)标准状状况下,排空法收集氯化氢气体,做喷泉实验时,如果气体没有溢出,实验完成时所得溶液的物质的量浓度为
(4)SiO2在自然界中广泛存在,它是制备现代通讯材料
更新时间:2022-10-24 20:10:04
|
相似题推荐
填空题
|
较易
(0.85)
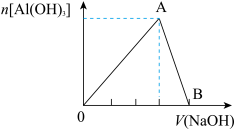
【推荐1】向20mL含有1mol/L的氯化铝溶液中逐滴加入浓度为1mol/L的氢氧化钠溶液,产生沉淀的物质的量与所加碱的体积如图所示:
(1)写出OA段和AB段发生反应的离子方程式:OA段_____ ;AB段_____ 。
(2)A点溶液中的溶质为:____ 。(填化学式)
(3)若产生0.78g白色沉淀,则加入的氢氧化钠溶液的体积可能是____ mL或____ mL。
(4)B点表示的氢氧化钠溶液的体积是___ mL。
(1)写出OA段和AB段发生反应的离子方程式:OA段
(2)A点溶液中的溶质为:
(3)若产生0.78g白色沉淀,则加入的氢氧化钠溶液的体积可能是
(4)B点表示的氢氧化钠溶液的体积是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】将4 g NaOH溶于________ g水中,可使溶液中H2O与Na+的物质的量之比为20∶1,此溶液中溶质的质量分数为_______ 。若测得该溶液的密度为1.1 g/cm3,则该溶液体积为_______ ,溶液中c(Na+)为________
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】现有下列4种物质:①SiO2、②NH3、③Na2CO3、④FeCl3溶液。其中,遇到KSCN溶液时变成红色的是_______ (填序号,下同);可用于制光导纤维的是_______ ;可用作制冷剂的是_______ ;可用作食用碱的是_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有下列3种物质:①液氨、②二氧化硅、③二氧化硫。其中,可以用来生产硫酸的物质是____ (填序号,下同);可以用来做制冷剂的物质是____ ;可以用来制光导纤维的物质是____ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)下列微粒之间,属于同位素的是_______ (填字母),属于同素异形体的是_______ ,属于同一种物质的是_______ 。
a.红磷和白磷b.氕和氚c.氯气和液氯d.冰和干冰e.氧气和臭氧f. 和
和
(2)计算机芯片和太阳能电池的主要成分是_______ ;在碳纤维复合材料中,碳纤维属于_______ (填“增强体”或“基体”)。
(3)玉石的主要成分基本都属于硅酸盐,独山玉是中国四大名玉之一,也称“南阳玉”或“河南玉”,独山玉(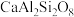 )表示为氧化物形式是
)表示为氧化物形式是_______ 。
(4)铜器表面有时会生成铜绿 ,这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的化学方程式
,这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的化学方程式_______ 。
a.红磷和白磷b.氕和氚c.氯气和液氯d.冰和干冰e.氧气和臭氧f.
 和
和
(2)计算机芯片和太阳能电池的主要成分是
(3)玉石的主要成分基本都属于硅酸盐,独山玉是中国四大名玉之一,也称“南阳玉”或“河南玉”,独山玉(
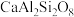 )表示为氧化物形式是
)表示为氧化物形式是(4)铜器表面有时会生成铜绿
 ,这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的化学方程式
,这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)①Ca(ClO)2的名称为____________ ;
②磁铁矿主要成分的化学式为____________ 。
(2)请按要求完成相应的方程式:
①金属镁在二氧化碳中燃烧的化学方程式____________ 。
②铜与浓硫酸混合加热的化学方程式____________ 。
③用离子方程式说明用磨合玻璃塞的试剂瓶不可装NaOH溶液的原因:____________ 。
④用FeCl3溶液与铜反应制作印刷电路板的离子方程式____________ 。
②磁铁矿主要成分的化学式为
(2)请按要求完成相应的方程式:
①金属镁在二氧化碳中燃烧的化学方程式
②铜与浓硫酸混合加热的化学方程式
③用离子方程式说明用磨合玻璃塞的试剂瓶不可装NaOH溶液的原因:
④用FeCl3溶液与铜反应制作印刷电路板的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】氢氧燃料电池是符合绿色化学理念的新型燃料电池,其原理如图所示。
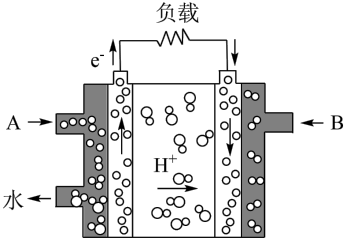
(1)通入的气体A是____________ (填化学式)。
(2)通入气体B的电极上的反应式为____________ 。
(3)若总共消耗气体3.36L(标准状况下),则通过外电路的电子的物质的量为____________ mol。
(4)若将此电池作为电源,电解熔融的氧化铝制备金属铝,理论上制备9g的金属铝,需消耗氢气的体积为____________ L(标准状况下)。

(1)通入的气体A是
(2)通入气体B的电极上的反应式为
(3)若总共消耗气体3.36L(标准状况下),则通过外电路的电子的物质的量为
(4)若将此电池作为电源,电解熔融的氧化铝制备金属铝,理论上制备9g的金属铝,需消耗氢气的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某课外活动小组进行电解饱和食盐水的实验(如图)。请回答下列问题。

(1)通电一段时间后,可观察到_______ 电极(填“阴极”或“阳极”)附近溶液颜色先变红,该电极上的电极反应式为_______ 。
(2)该溶液电解反应的化学方程式为_______ 。
(3)若开始时改用银棒做阳极,阳极的电极反应式为_______ 。
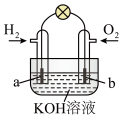
(4)若用H2和O2为反应物,以KOH为电解质溶液,可构成新型燃料电池(如图),两个电极均由多孔性炭制成,通入的气体由孔隙中逸出,并在电极表面放电。则a极的电极反应式为_______ 。

(1)通电一段时间后,可观察到
(2)该溶液电解反应的化学方程式为
(3)若开始时改用银棒做阳极,阳极的电极反应式为
(4)若用H2和O2为反应物,以KOH为电解质溶液,可构成新型燃料电池(如图),两个电极均由多孔性炭制成,通入的气体由孔隙中逸出,并在电极表面放电。则a极的电极反应式为

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O=2H2↑+O2↑。制得的氢气可用于燃料电池。请完成下列问题:
(1)太阳光分解海水时,实现了从________ 能转化为________ 能,二氧化钛作______ 。
(2)生成的氢气,用于燃料电池时,实现________ 能转化为________ 能。水分解时,断裂的化学键有_______ 键,分解海水的反应属于_____ (填“放热”或“吸热”)反应。
(3)某种氢燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应式为:
A极:H2+O2--2e-=H2O
则A极是电池的________ 极;电子从该极________ (填“流入”或“流出”),另一电极的电极反应式为________________ 。
(1)太阳光分解海水时,实现了从
(2)生成的氢气,用于燃料电池时,实现
(3)某种氢燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应式为:
A极:H2+O2--2e-=H2O
则A极是电池的
您最近一年使用:0次



