现有以下物质:①碳酸氢钠;②氯气;③CaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧稀醋酸。
(1)上述物质中属于非电解质的是_______ 。(填序号)
(2)上述物质中属于能导电的电解质是_______ 。(填序号)
(3)写出④的电离方程式_______ 。
(4)写出①受热分解的化学方程式为_______ 。该反应_______ (填是或不是)氧化还原反应,如果是氧化还原反应,氧化产物为_______ (如果不是此空不填)。
(5)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈_______ 色,停止加热即制得Fe(OH)3胶体。写出制备物质⑤的化学方程式:_______ 。
(1)上述物质中属于非电解质的是
(2)上述物质中属于能导电的电解质是
(3)写出④的电离方程式
(4)写出①受热分解的化学方程式为
(5)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈
更新时间:2022-10-26 19:58:43
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】铁是地壳中占比较高的元素,其化合物在自然界十分常见。
(1)某铁原子可表示为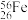 ,其核内中子数是
,其核内中子数是___________ 。
(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为___________ ;设阿伏加德罗常数的值为 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为___________ 。
(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入___________ 溶液并振荡,若滤液变为红色,则药品已变质。
(4)现有甲、乙、丙三名同学分别进行制备 胶体的实验。甲同学向
胶体的实验。甲同学向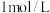 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
①操作正确的同学是___________ 。
②写出制备胶体过程中的离子方程式___________ 。欲除去胶体中混有的 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是___________ 。
③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为___________ 。
(1)某铁原子可表示为
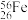 ,其核内中子数是
,其核内中子数是(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为
 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入
(4)现有甲、乙、丙三名同学分别进行制备
 胶体的实验。甲同学向
胶体的实验。甲同学向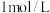 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。①操作正确的同学是
②写出制备胶体过程中的离子方程式
 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)下列物质中:A.碳酸氢钠晶体;B.乙醇;C.盐酸;D.铜;E.蔗糖;F. ;G.干冰;H.液态氯化氢;I.熔融的氯化铁;J.纯醋酸;K.氮气;L.石墨。
;G.干冰;H.液态氯化氢;I.熔融的氯化铁;J.纯醋酸;K.氮气;L.石墨。
①以上物质能导电的是__________ (填字母,下同);
②以上物质中属于电解质的是__________ ;
③以上物质中属于非电解质的是__________ 。
(2)上述物质中,A在水溶液中的电离方程式为______________________________ ,A与C在溶液中反应的离子方程式为______________________________ 。
(3)写出用I的饱和溶液制备组氧化铁胶体的化学反应方程式______________________________ ,制备步骤为:首先取少量__________ 于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的 溶液,继续煮沸至
溶液,继续煮沸至____________________ ,判断胶体制备是否成功,可利用胶体的____________________ 。
(1)下列物质中:A.碳酸氢钠晶体;B.乙醇;C.盐酸;D.铜;E.蔗糖;F.
 ;G.干冰;H.液态氯化氢;I.熔融的氯化铁;J.纯醋酸;K.氮气;L.石墨。
;G.干冰;H.液态氯化氢;I.熔融的氯化铁;J.纯醋酸;K.氮气;L.石墨。①以上物质能导电的是
②以上物质中属于电解质的是
③以上物质中属于非电解质的是
(2)上述物质中,A在水溶液中的电离方程式为
(3)写出用I的饱和溶液制备组氧化铁胶体的化学反应方程式
 溶液,继续煮沸至
溶液,继续煮沸至
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若向装有饱和FeCl3溶液的烧杯中分别滴入下列物质中,能形成胶体的是_______ (填序号)。
a.冷水 b.沸水 c.NaOH浓溶液 d.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学方程式:_____________________
(3)用激光笔照射装有Fe(OH)3胶体的烧杯,能在侧面看到一条_________ ,这种现象称为丁达尔效应
(4)Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是________ (填序号)。
a.分散质粒子大小不同 b.颜色不同 c.后者不稳定
(5)若向制得的胶体中再加入稀HCl,红褐色分散系会被破坏,变为黄色溶液,写出相关离子方程式____________________
(1)若向装有饱和FeCl3溶液的烧杯中分别滴入下列物质中,能形成胶体的是
a.冷水 b.沸水 c.NaOH浓溶液 d.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学方程式:
(3)用激光笔照射装有Fe(OH)3胶体的烧杯,能在侧面看到一条
(4)Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是
a.分散质粒子大小不同 b.颜色不同 c.后者不稳定
(5)若向制得的胶体中再加入稀HCl,红褐色分散系会被破坏,变为黄色溶液,写出相关离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有以下几种物质(或微粒):
①Cu丝② ③
③ ④液态HCl⑤
④液态HCl⑤ 溶液⑥熔融
溶液⑥熔融 ⑦
⑦ 溶液⑧饱和
溶液⑧饱和 溶液⑨消毒酒精
溶液⑨消毒酒精
回答下列问题:
(1)②和③之间互为___________ 。
(2)以上物质中属于能导电的电解质是___________ 。(填代号)
(3)⑤中溶质熔融状态的电离方程式为___________ 。
(4)向⑤中逐渐加入过量 溶液的离子方程式为
溶液的离子方程式为___________ 。
①Cu丝②
 ③
③ ④液态HCl⑤
④液态HCl⑤ 溶液⑥熔融
溶液⑥熔融 ⑦
⑦ 溶液⑧饱和
溶液⑧饱和 溶液⑨消毒酒精
溶液⑨消毒酒精回答下列问题:
(1)②和③之间互为
(2)以上物质中属于能导电的电解质是
(3)⑤中溶质熔融状态的电离方程式为
(4)向⑤中逐渐加入过量
 溶液的离子方程式为
溶液的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)请找出下列各组物质中与其它3种不同的一种物质。
A.CaO、Na2O、CO2、CuO
B.豆浆、淀粉溶液、石灰乳、雾
C.HCl、HClO4、H2SO4、HNO3
A______ ;B______ ;C______ 。
(2)①汞 ②烧碱 ③石灰石 ④NaHCO3晶体 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧氯气 ⑨液态氯化氢 ⑩酒精溶液上述物质中能导电的是______ ,属于电解质的是___________ ,属于非电解质的是___________ 。(填序号)
(1)请找出下列各组物质中与其它3种不同的一种物质。
A.CaO、Na2O、CO2、CuO
B.豆浆、淀粉溶液、石灰乳、雾
C.HCl、HClO4、H2SO4、HNO3
A
(2)①汞 ②烧碱 ③石灰石 ④NaHCO3晶体 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧氯气 ⑨液态氯化氢 ⑩酒精溶液上述物质中能导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥盐酸;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3。其中:属于电解质的是___ ;
Ⅱ.已知0.1 mol/L的NaHSO4溶液中H+的物质的量浓度为0.1 mol/L,请回答下列问题:
(1)写出NaHSO4在水溶液中电离的方程式:____ 。
(2)写出NaHSO4与氢氧化钠溶液反应的离子方程式___ 。
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液恰好显中性,则该反应的离子方程式是:____ 。
Ⅲ.钠是一种还原性很强的金属,甚至能和冷水发生剧烈反应,写出钠加入到水中反生反应的离子反应方程式___ ;把钠加入到饱和的石灰水中的现象是___ ,产生这种现象的原因是_____ ;把钠加入到硫酸铜溶液中的现象是___ ,写出该过程中产生沉淀的离子反应方程式____ ;写出少量的钠加入到足量硫酸氢钠溶液中反应的离子方程式____ 。
Ⅳ.将一定体积的CuSO4溶液、NaCl溶液和Na2SO3混合,充分反应后有白色沉淀生成。经分析可知白色沉淀中只含有铜元素和氯元素,且该化合物的摩尔质量为99.5g/mol。试回答下列问题:
(1)白色沉淀的化学式为____ 。
(2)题述过程发生的反应____ (填“属于”或“不属于”)氧化还原反应。
(3)题述反应的离子方程式为Cu2++Cl-+SO32-+H2O→白色沉淀+( )+H+(离子方程式没有配平),则括号内的离子为___ 。
Ⅱ.已知0.1 mol/L的NaHSO4溶液中H+的物质的量浓度为0.1 mol/L,请回答下列问题:
(1)写出NaHSO4在水溶液中电离的方程式:
(2)写出NaHSO4与氢氧化钠溶液反应的离子方程式
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液恰好显中性,则该反应的离子方程式是:
Ⅲ.钠是一种还原性很强的金属,甚至能和冷水发生剧烈反应,写出钠加入到水中反生反应的离子反应方程式
Ⅳ.将一定体积的CuSO4溶液、NaCl溶液和Na2SO3混合,充分反应后有白色沉淀生成。经分析可知白色沉淀中只含有铜元素和氯元素,且该化合物的摩尔质量为99.5g/mol。试回答下列问题:
(1)白色沉淀的化学式为
(2)题述过程发生的反应
(3)题述反应的离子方程式为Cu2++Cl-+SO32-+H2O→白色沉淀+( )+H+(离子方程式没有配平),则括号内的离子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有如下物质:①铜;② 溶液;③熔融
溶液;③熔融 ;④
;④ ;⑤酒精;⑥饱和氯化铁溶液;⑦
;⑤酒精;⑥饱和氯化铁溶液;⑦ 溶液;⑧
溶液;⑧ 晶体
晶体
(1)以上物质中,属于电解质的是_______ (填序号,下同),属于非电解质的是_______ ,上述物质能导电的是_______ 。
(2)将②与⑦进行混合,该过程中发生的离子反应方程式是_______ 。
(3)利用物质⑥可以制备氢氧化铁胶体,其离子方程式为_______ 。
(4)向氢氧化钡溶液中加入物质③的溶液至恰好沉淀完全,其离子方程式为_______ 。
 溶液;③熔融
溶液;③熔融 ;④
;④ ;⑤酒精;⑥饱和氯化铁溶液;⑦
;⑤酒精;⑥饱和氯化铁溶液;⑦ 溶液;⑧
溶液;⑧ 晶体
晶体(1)以上物质中,属于电解质的是
(2)将②与⑦进行混合,该过程中发生的离子反应方程式是
(3)利用物质⑥可以制备氢氧化铁胶体,其离子方程式为
(4)向氢氧化钡溶液中加入物质③的溶液至恰好沉淀完全,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在图(Ⅰ)所示的装置中,烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐渐加入某种溶液A时,溶液的导电性的变化趋势如图(Ⅱ)所示。
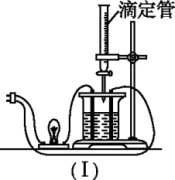
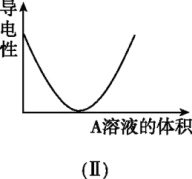
(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质可能是(填序号)___________ 。
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(2)NaHSO4属于___________ (填“酸”“碱”或“盐”),写出NaHSO4在水溶液中的电离方程式:___________ 。
(3)用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂。
Ⅰ.CaCl2(HCl):试剂___________ , Ⅱ.O2(CO2):试剂___________ 。


(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质可能是(填序号)
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(2)NaHSO4属于
(3)用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂。
Ⅰ.CaCl2(HCl):试剂
您最近一年使用:0次
【推荐3】硼及其化合物生产中有广泛用途,硼和铝位于同主族,具有相类似的化学性质。
(1)硼和氯气反应生成 BCl3,在该分子中,硼原子最外层有__________ 个电子。
(2)硼与氢氧化钠溶液反应生成 Na[B(OH)4](四羟基合硼酸钠)和氢气,该反应的化学方程式为____________ 。
(3)B(OH)3(硼酸)是一元弱酸,它在水中类似氨的电离: NH3+H2O⇌ +OH- ,硼酸在水中电离的方程式为
+OH- ,硼酸在水中电离的方程式为____ 。
(4)NaBH4 是有机合成中重要的还原剂。工业上合成方法之一是:Na2B4O7 +16Na+8H2 +7SiO2 7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是
7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是___________ ,制备1 mol NaBH4时转移 ____________ mol 电子。
(5)NaBH4与水反应生成Na[B(OH)4]和一种气体,写出化学方程式:_____________ 。
(1)硼和氯气反应生成 BCl3,在该分子中,硼原子最外层有
(2)硼与氢氧化钠溶液反应生成 Na[B(OH)4](四羟基合硼酸钠)和氢气,该反应的化学方程式为
(3)B(OH)3(硼酸)是一元弱酸,它在水中类似氨的电离: NH3+H2O⇌
 +OH- ,硼酸在水中电离的方程式为
+OH- ,硼酸在水中电离的方程式为(4)NaBH4 是有机合成中重要的还原剂。工业上合成方法之一是:Na2B4O7 +16Na+8H2 +7SiO2
 7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是
7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是(5)NaBH4与水反应生成Na[B(OH)4]和一种气体,写出化学方程式:
您最近一年使用:0次
【推荐1】现有下列几种物质:①盐酸;②Na2O;③Na2O2;④Al(OH)3;⑤Na2CO3;⑥H2O;⑦CO2;⑧乙醇;⑨Cu;⑩NaOH溶液。
(1)其中属于电解质的有___________ (填写序号,下同),属于碱性氧化物的有_______ 。
(2)④与⑩反应的离子方程式为______________________________________ 。
(3)Na2O2因能发生下列反应被用作供氧剂:2Na2O2+2CO2=2Na2CO3+O2,该反应中,氧化剂与还原剂的物质的量之比为:______ 。
(4)如用超氧化钾(KO2)作供氧剂,写出它和CO2反应的化学方程式,并标出电子转移的方向和数目______________________________________________________ 。
(1)其中属于电解质的有
(2)④与⑩反应的离子方程式为
(3)Na2O2因能发生下列反应被用作供氧剂:2Na2O2+2CO2=2Na2CO3+O2,该反应中,氧化剂与还原剂的物质的量之比为:
(4)如用超氧化钾(KO2)作供氧剂,写出它和CO2反应的化学方程式,并标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】废水中氨氮(NH3、NH )的处理技术有生物脱氮法、化学沉淀法、折点加氯法和电催化氧化法等。
)的处理技术有生物脱氮法、化学沉淀法、折点加氯法和电催化氧化法等。
(1)氨氮污水直接排放入河流、湖泊导致的环境问题是_____ 。
(2)生物脱氮法:利用微生物脱氮,原理如下:



 N2
N2
反应①的离子方程式为_____ 。
(3)化学沉淀法:向废水中加入含MgCl2、Na3PO4的溶液, 转化为MgNH4PO4·6H2O沉淀。若pH过大,氨氮去除率和磷利用率均降低,其原因是
转化为MgNH4PO4·6H2O沉淀。若pH过大,氨氮去除率和磷利用率均降低,其原因是_____ (用离子方程式表示)。
(4)折点加氯法:向废水中加入NaClO溶液,使氨氮氧化成N2,相关反应如下:
NaClO+H2O=HClO+NaOH(Ⅰ);
NH3+HClO=NH2Cl+H2O(Ⅱ);
NH2Cl+HClO=NHCl2+H2O(Ⅲ);
NHCl2+H2O=NOH+2HCl(Ⅳ);
NHCl2+NOH=N2↑+HClO+HCl(Ⅴ)。
探究NaClO的投加量[以m(Cl2)表示]对氨氮去除率的影响,实验结果如图所示。

①当m(Cl2)∶m(NH3)≥7.7时,污水中总氮去除率缓慢下降,其原因是_____ 。
②当m(Cl2)∶m(NH3)<7.7时,随着m(Cl2)∶m(NH3)的减小,污水中余氯(除Cl-外的氯元素存在形式)浓度升高,其原因是_____ 。
 )的处理技术有生物脱氮法、化学沉淀法、折点加氯法和电催化氧化法等。
)的处理技术有生物脱氮法、化学沉淀法、折点加氯法和电催化氧化法等。(1)氨氮污水直接排放入河流、湖泊导致的环境问题是
(2)生物脱氮法:利用微生物脱氮,原理如下:



 N2
N2反应①的离子方程式为
(3)化学沉淀法:向废水中加入含MgCl2、Na3PO4的溶液,
 转化为MgNH4PO4·6H2O沉淀。若pH过大,氨氮去除率和磷利用率均降低,其原因是
转化为MgNH4PO4·6H2O沉淀。若pH过大,氨氮去除率和磷利用率均降低,其原因是(4)折点加氯法:向废水中加入NaClO溶液,使氨氮氧化成N2,相关反应如下:
NaClO+H2O=HClO+NaOH(Ⅰ);
NH3+HClO=NH2Cl+H2O(Ⅱ);
NH2Cl+HClO=NHCl2+H2O(Ⅲ);
NHCl2+H2O=NOH+2HCl(Ⅳ);
NHCl2+NOH=N2↑+HClO+HCl(Ⅴ)。
探究NaClO的投加量[以m(Cl2)表示]对氨氮去除率的影响,实验结果如图所示。

①当m(Cl2)∶m(NH3)≥7.7时,污水中总氮去除率缓慢下降,其原因是
②当m(Cl2)∶m(NH3)<7.7时,随着m(Cl2)∶m(NH3)的减小,污水中余氯(除Cl-外的氯元素存在形式)浓度升高,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.实验室利用二氧化锰和浓盐酸反应制取Cl2,化学方程式如下: MnO2+4HCl(浓)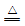 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)请用单线桥标出该反应电子转移的方向和数目___________ ,该反应的氧化产物是___________ 。
(2)其中氧化剂与还原剂的物质的量之比是___________ ;若实验中有87g的MnO2完全反应,则制得的Cl2在标况下的体积是___________ L。
Ⅱ.盐酸广泛应用在稀有金属的湿法治金、漂染工业、金属加工、无机药品及有机药物的生产等领域中。HCl极易溶于水,工业上用HCl气体溶于水的方法制取盐酸。
(1)用密度为1.2 g/mL,质量分数为36.5%的浓盐酸配制250mL 3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为________ mL。
(2)溶液配制中需要的玻璃仪器有烧杯、玻璃棒、量筒、___________ 、___________ 。
(3)实验过程中,下列操作会导致最终所配溶液浓度偏高的是____________ 。
A.量取浓盐酸时俯视刻度线 B.实验前,容量瓶中有少量残留蒸馏水
C.定容时俯视刻度线 D.转移时,未洗涤烧杯和玻璃棒
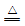 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(1)请用单线桥标出该反应电子转移的方向和数目
(2)其中氧化剂与还原剂的物质的量之比是
Ⅱ.盐酸广泛应用在稀有金属的湿法治金、漂染工业、金属加工、无机药品及有机药物的生产等领域中。HCl极易溶于水,工业上用HCl气体溶于水的方法制取盐酸。
(1)用密度为1.2 g/mL,质量分数为36.5%的浓盐酸配制250mL 3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为
(2)溶液配制中需要的玻璃仪器有烧杯、玻璃棒、量筒、
(3)实验过程中,下列操作会导致最终所配溶液浓度偏高的是
A.量取浓盐酸时俯视刻度线 B.实验前,容量瓶中有少量残留蒸馏水
C.定容时俯视刻度线 D.转移时,未洗涤烧杯和玻璃棒
您最近一年使用:0次



