硼及其化合物生产中有广泛用途,硼和铝位于同主族,具有相类似的化学性质。
(1)硼和氯气反应生成 BCl3,在该分子中,硼原子最外层有__________ 个电子。
(2)硼与氢氧化钠溶液反应生成 Na[B(OH)4](四羟基合硼酸钠)和氢气,该反应的化学方程式为____________ 。
(3)B(OH)3(硼酸)是一元弱酸,它在水中类似氨的电离: NH3+H2O⇌ +OH- ,硼酸在水中电离的方程式为
+OH- ,硼酸在水中电离的方程式为____ 。
(4)NaBH4 是有机合成中重要的还原剂。工业上合成方法之一是:Na2B4O7 +16Na+8H2 +7SiO2 7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是
7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是___________ ,制备1 mol NaBH4时转移 ____________ mol 电子。
(5)NaBH4与水反应生成Na[B(OH)4]和一种气体,写出化学方程式:_____________ 。
(1)硼和氯气反应生成 BCl3,在该分子中,硼原子最外层有
(2)硼与氢氧化钠溶液反应生成 Na[B(OH)4](四羟基合硼酸钠)和氢气,该反应的化学方程式为
(3)B(OH)3(硼酸)是一元弱酸,它在水中类似氨的电离: NH3+H2O⇌
 +OH- ,硼酸在水中电离的方程式为
+OH- ,硼酸在水中电离的方程式为(4)NaBH4 是有机合成中重要的还原剂。工业上合成方法之一是:Na2B4O7 +16Na+8H2 +7SiO2
 7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是
7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是(5)NaBH4与水反应生成Na[B(OH)4]和一种气体,写出化学方程式:
2020·海南·模拟预测 查看更多[1]
更新时间:2020-07-04 10:02:03
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】电解熔融氯化钙可以得到金属钙和氯气,钙在氯气中燃烧又能生成氯化钙(如图所示),回答下列问题:
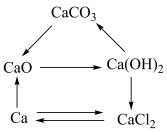
(1)氯化钙在水中的电离方程式为_______ 。
(2)用特殊的方法把固体 加工成纳米级的超细粉末粒子,可制得纳米材料(直径为1~100
加工成纳米级的超细粉末粒子,可制得纳米材料(直径为1~100 )。
)。
①下列分散系中,分散质粒子直径和这种超细粉末粒子的直径具有相同数量级的是_______ (填标号)。
A.溶液 B.悬浊液 C.胶体 D.乳浊液
②将少量的超细粉末粒子的 加入盛有水的烧杯中,搅拌后静置片刻。当光束垂直通过该分散系时,可观察到的现象为
加入盛有水的烧杯中,搅拌后静置片刻。当光束垂直通过该分散系时,可观察到的现象为_______ ,该分散系能吸附水中的悬浮颗粒物,利用了其_______ 性。
(3)图示出现的物质中,属于盐的有_______ 种。
(4)将少量的固体 与碳酸氢钠溶液混合的化学方程式为
与碳酸氢钠溶液混合的化学方程式为_______ 。
(5)将少量的固体 与稀盐酸混合,发生反应的化学方程式为
与稀盐酸混合,发生反应的化学方程式为 。
。
①该反应的反应类型为_______ (填“氧化还原反应”或“复分解反应”)。
②下列有关稀盐酸的说法正确的是_______ (填标号)。
A. 的摩尔质量为36.5
的摩尔质量为36.5
B.稀盐酸能导电,是由于其溶液中有可自由移动的 和
和
C.稀盐酸能导电,但稀盐酸既不是电解质又不是非电解质
D.实验室中,稀盐酸可用铝制器皿来盛装
③该反应中,每消耗4g ,同时生成
,同时生成 的体积为
的体积为_______  (标准状况下)。
(标准状况下)。

(1)氯化钙在水中的电离方程式为
(2)用特殊的方法把固体
 加工成纳米级的超细粉末粒子,可制得纳米材料(直径为1~100
加工成纳米级的超细粉末粒子,可制得纳米材料(直径为1~100 )。
)。①下列分散系中,分散质粒子直径和这种超细粉末粒子的直径具有相同数量级的是
A.溶液 B.悬浊液 C.胶体 D.乳浊液
②将少量的超细粉末粒子的
 加入盛有水的烧杯中,搅拌后静置片刻。当光束垂直通过该分散系时,可观察到的现象为
加入盛有水的烧杯中,搅拌后静置片刻。当光束垂直通过该分散系时,可观察到的现象为(3)图示出现的物质中,属于盐的有
(4)将少量的固体
 与碳酸氢钠溶液混合的化学方程式为
与碳酸氢钠溶液混合的化学方程式为(5)将少量的固体
 与稀盐酸混合,发生反应的化学方程式为
与稀盐酸混合,发生反应的化学方程式为 。
。①该反应的反应类型为
②下列有关稀盐酸的说法正确的是
A.
 的摩尔质量为36.5
的摩尔质量为36.5B.稀盐酸能导电,是由于其溶液中有可自由移动的
 和
和
C.稀盐酸能导电,但稀盐酸既不是电解质又不是非电解质
D.实验室中,稀盐酸可用铝制器皿来盛装
③该反应中,每消耗4g
 ,同时生成
,同时生成 的体积为
的体积为 (标准状况下)。
(标准状况下)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】生活离不开化学。家庭厨卫中有许多中学化学常见的物质,它们的主要成分如下表。
回答下列问题:
(1)以上主要成分中属于弱电解质的有_______ (填序号)。
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是_______ 。
(3)KAl(SO4)2·12H2O的电离方程式为_______ 。
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为_______ ;Na2CO3固体中若含有少量NaHCO3,可采取的除杂方法为_______ 。
(5)NaHCO3溶液与白醋反应的离子方程式为_______ 。
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:_______ 。
| 商品 | 食盐 | 碱面 | 84消毒液 | 发酵粉 |
| 主要成分 | ①NaCl | ②Na2CO3 | ③NaClO | ④ NaHCO3⑤KAl(SO4)2·12H2O |
| 商品 | 料酒 | 白醋 | 洁厕灵 | \ |
| 主要成分 | ⑥C2H5OH | ⑦CH3COOH | ⑧HCl |
(1)以上主要成分中属于弱电解质的有
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是
(3)KAl(SO4)2·12H2O的电离方程式为
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为
(5)NaHCO3溶液与白醋反应的离子方程式为
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】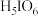 (正高碘酸)是用于光度法测定苯肼的试剂。工业上用
(正高碘酸)是用于光度法测定苯肼的试剂。工业上用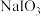 制备
制备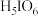 的流程如图:
的流程如图:
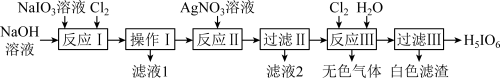
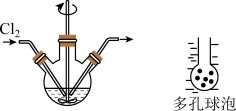
(1)“反应Ⅰ”可在如图所示的装置中生成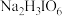 ,则操作Ⅰ所需的玻璃仪器除烧杯外,还有
,则操作Ⅰ所需的玻璃仪器除烧杯外,还有________ 。若对装置进行改进,将通 的导管下端连接多孔球泡装置,则主要目的是
的导管下端连接多孔球泡装置,则主要目的是________ 。
(2)“反应Ⅱ”生成不溶于水的黑色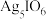 ,“滤液2”呈
,“滤液2”呈________ (填“酸”“碱”或“中”)性。
(3)“无色气体”为________ (填化学式)。
(4)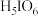 具有强氧化性,可将
具有强氧化性,可将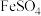 氧化为
氧化为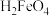 ,自身被还原为
,自身被还原为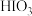 ,该反应的化学方程式为
,该反应的化学方程式为________ 。
(5)工业上为降低成本,减少对环境的污染,整个流程需要控制加入 和
和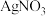 的物质的量之比为
的物质的量之比为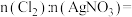
________ 。
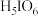 (正高碘酸)是用于光度法测定苯肼的试剂。工业上用
(正高碘酸)是用于光度法测定苯肼的试剂。工业上用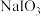 制备
制备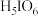 的流程如图:
的流程如图:
(1)“反应Ⅰ”可在如图所示的装置中生成
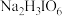 ,则操作Ⅰ所需的玻璃仪器除烧杯外,还有
,则操作Ⅰ所需的玻璃仪器除烧杯外,还有 的导管下端连接多孔球泡装置,则主要目的是
的导管下端连接多孔球泡装置,则主要目的是
(2)“反应Ⅱ”生成不溶于水的黑色
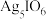 ,“滤液2”呈
,“滤液2”呈(3)“无色气体”为
(4)
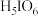 具有强氧化性,可将
具有强氧化性,可将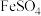 氧化为
氧化为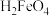 ,自身被还原为
,自身被还原为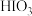 ,该反应的化学方程式为
,该反应的化学方程式为(5)工业上为降低成本,减少对环境的污染,整个流程需要控制加入
 和
和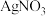 的物质的量之比为
的物质的量之比为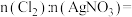
您最近一年使用:0次
【推荐2】KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
______KClO3+______HCl(浓)=______KCl+______ClO2↑+______Cl2↑+______H2O
(1)请配平上述化学方程式_____ 。
(2)浓盐酸在反应中显示出来的性质是___ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)氧化剂是____ ,氧化产物是___ 。
______KClO3+______HCl(浓)=______KCl+______ClO2↑+______Cl2↑+______H2O
(1)请配平上述化学方程式
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,回答下列问题:
(1)该反应中还原产物的化学式是______ ,被氧化的元素是______ (填元素符号)。
(2)用双线桥标出上述反应的电子转移情况______ 。
(3)若反应共产生了8.96L(标准状况)气体,则反应转移的电子的物质的量为______ mol,消耗还原剂的物质的量为______ mol。
(4)标准状况下44.8mL的ClO2恰好能与50mL0.1mol•L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为______ ,此过程说明ClO2具有______ (填“氧化”或“还原”)性。
(5)在硫化钠溶液中通入ClO2可发生如下反应,请完成配平:______ 。
ClO2+ S2- H2O= Cl-+ SO H+
H+
(1)该反应中还原产物的化学式是
(2)用双线桥标出上述反应的电子转移情况
(3)若反应共产生了8.96L(标准状况)气体,则反应转移的电子的物质的量为
(4)标准状况下44.8mL的ClO2恰好能与50mL0.1mol•L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为
(5)在硫化钠溶液中通入ClO2可发生如下反应,请完成配平:
ClO2+ S2- H2O= Cl-+ SO
 H+
H+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在工农业生产、日常生活中具有广泛用途。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+,故维生素C具有___________ 性(填“氧化”或“还原”,下同),在反应过程中维生素C发生___________ 反应。
(2)黑火药是我国古代的四大发明之一,爆炸时的反应为:
①配平上述反应。________
②该反应中还原剂是___________ ,还原产物是___________ ,生成1molN2转移电子的物质的量为___________ 。
(3)高温下铝粉和氧化铁的反应可以用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后将钢轨牢牢地焊接在一起。该反应的化学方程式为___________ ,其中被还原的物质是___________ (填化学式)。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+,故维生素C具有
(2)黑火药是我国古代的四大发明之一,爆炸时的反应为:

①配平上述反应。
②该反应中还原剂是
(3)高温下铝粉和氧化铁的反应可以用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后将钢轨牢牢地焊接在一起。该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学计量在化学中占有重要地位,请回答下列问题。
(1)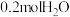 中所含有的质于数目为
中所含有的质于数目为___________ 。
(2)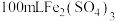 溶液中含
溶液中含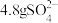 ,取出10mL溶液,用水稀释成50mL,则稀释溶液中
,取出10mL溶液,用水稀释成50mL,则稀释溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(3)在反应 中,每生成标准状况下6.72LCO气体,转移的电子数目为
中,每生成标准状况下6.72LCO气体,转移的电子数目为___________ 。
(4)制备 化学方程式为:
化学方程式为: (未配平),现有
(未配平),现有 的
的 溶液与足量浓盐酸反应,可获得
溶液与足量浓盐酸反应,可获得 的质量为
的质量为___________ 。
(5)甘氨酸(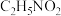 )样品
)样品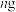 ,其中的氮全部变为氨气用盐酸吸收(已知
,其中的氮全部变为氨气用盐酸吸收(已知 ),消耗浓度为
),消耗浓度为 的盐酸
的盐酸 ,则样品中氮的质量分数为
,则样品中氮的质量分数为___________ %,样品的纯度为___________ %。
(1)
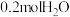 中所含有的质于数目为
中所含有的质于数目为(2)
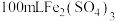 溶液中含
溶液中含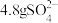 ,取出10mL溶液,用水稀释成50mL,则稀释溶液中
,取出10mL溶液,用水稀释成50mL,则稀释溶液中 的物质的量浓度为
的物质的量浓度为(3)在反应
 中,每生成标准状况下6.72LCO气体,转移的电子数目为
中,每生成标准状况下6.72LCO气体,转移的电子数目为(4)制备
 化学方程式为:
化学方程式为: (未配平),现有
(未配平),现有 的
的 溶液与足量浓盐酸反应,可获得
溶液与足量浓盐酸反应,可获得 的质量为
的质量为(5)甘氨酸(
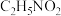 )样品
)样品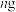 ,其中的氮全部变为氨气用盐酸吸收(已知
,其中的氮全部变为氨气用盐酸吸收(已知 ),消耗浓度为
),消耗浓度为 的盐酸
的盐酸 ,则样品中氮的质量分数为
,则样品中氮的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
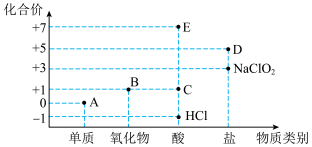
(1)物质E的化学式为___________
(2)A、B、C、D(钾盐)四种物质中,属于电解质的是___________ (填化学式)
(3)A与水反应的离子方程式为___________
(4)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为___________
(5)已知A与氢氧化钠溶液反应生成 和
和 的混合物,若
的混合物,若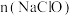 与
与 之比为2:3,则氧化剂与还原剂的物质的量之比为
之比为2:3,则氧化剂与还原剂的物质的量之比为___________
(6)已知二氧化氯( )为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的
)为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的 和物质A比较,所含的原子总数之比为
和物质A比较,所含的原子总数之比为___________ ,电子数目之比为___________ 。
(7)氯碱工业指的是工业上用电解饱和食盐水的方法,制取氯气和烧碱等主要产品,在国民经济和国防建设中占有重要地位。请写出氯化钠溶液在通电条件下,发生反应的离子方程式___________ 。

(1)物质E的化学式为
(2)A、B、C、D(钾盐)四种物质中,属于电解质的是
(3)A与水反应的离子方程式为
(4)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为
(5)已知A与氢氧化钠溶液反应生成
 和
和 的混合物,若
的混合物,若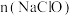 与
与 之比为2:3,则氧化剂与还原剂的物质的量之比为
之比为2:3,则氧化剂与还原剂的物质的量之比为(6)已知二氧化氯(
 )为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的
)为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的 和物质A比较,所含的原子总数之比为
和物质A比较,所含的原子总数之比为(7)氯碱工业指的是工业上用电解饱和食盐水的方法,制取氯气和烧碱等主要产品,在国民经济和国防建设中占有重要地位。请写出氯化钠溶液在通电条件下,发生反应的离子方程式
您最近一年使用:0次



