已知:浓硝酸和铜在常温下反应的化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。回答下列问题:
(1)在这个反应中,浓硝酸表现的化学性质是____ 性(填“酸”或“碱”)和____ 性(填“氧化”或“还原”)。
(2)Cu(NO3)2的电离方程式为____ 。
(3)在离子方程式中,单质、氧化物、水、气体、难溶物等不写成离子形式,该反应的离子方程式为____ 。
(4)随着反应的进行,硝酸的浓度减小,发生3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应。在该反应中,有3个Cu原子反应,有____ 个NO 转化为气体。
转化为气体。
(5)氮的氧化物有毒。用等量的铜制备Cu(NO3)2,有三种方法:
方法一:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
方法二:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
方法三:2Cu+O2+4HNO3 2Cu(NO3)2+2H2O
2Cu(NO3)2+2H2O
请从经济效益(硝酸根都进入硝酸铜)和社会效益(无有毒气体排放)考虑,最优方法是____ 。
(1)在这个反应中,浓硝酸表现的化学性质是
(2)Cu(NO3)2的电离方程式为
(3)在离子方程式中,单质、氧化物、水、气体、难溶物等不写成离子形式,该反应的离子方程式为
(4)随着反应的进行,硝酸的浓度减小,发生3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应。在该反应中,有3个Cu原子反应,有
 转化为气体。
转化为气体。(5)氮的氧化物有毒。用等量的铜制备Cu(NO3)2,有三种方法:
方法一:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
方法二:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
方法三:2Cu+O2+4HNO3
 2Cu(NO3)2+2H2O
2Cu(NO3)2+2H2O请从经济效益(硝酸根都进入硝酸铜)和社会效益(无有毒气体排放)考虑,最优方法是
更新时间:2022-11-04 08:01:37
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)下列物质能导电的是___ ,属于电解质的是___ ,属于非电解质的是___ 。
①NaCl晶体②液态SO2③液态醋酸④汞⑤BaSO4固体⑥纯蔗糖(C12H22O11)⑦氨水⑧熔化的KNO3
(2)写出下列反应的离子反应方程式。
①向NaOH溶液中通入过量CO2___
②NaOH溶液与NaHCO3溶液混合___
③少量澄清石灰水与足量Ca(HCO3)2溶液反应___
①NaCl晶体②液态SO2③液态醋酸④汞⑤BaSO4固体⑥纯蔗糖(C12H22O11)⑦氨水⑧熔化的KNO3
(2)写出下列反应的离子反应方程式。
①向NaOH溶液中通入过量CO2
②NaOH溶液与NaHCO3溶液混合
③少量澄清石灰水与足量Ca(HCO3)2溶液反应
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】甘氨酸铜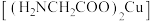 是人体摄取铜元素的主要来源之一。甘氨酸铜存在顺式和反式两种构型,其中一种构型易溶于水,另一种构型相对微溶于水。
是人体摄取铜元素的主要来源之一。甘氨酸铜存在顺式和反式两种构型,其中一种构型易溶于水,另一种构型相对微溶于水。_______ 。
(2)①甘氨酸铜中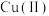 的配位数为4,画出其中一种构型的结构简式
的配位数为4,画出其中一种构型的结构简式_______ 。
②下列说法正确的是_______ 。
A.甘氨酸易溶于水,可溶于乙醇、丙酮等有机溶剂
B.可向硫酸铜溶液中滴加过量氢氧化钠溶液直接制得
C.步骤①可说明与铜离子的配位能力: 大于
大于
D.反式甘氨酸铜在水中的溶解度要小于顺式甘氨酸铜
③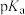 :甘氨酸
:甘氨酸_______ 丙酸(填“>”、“=”或“<”),理由是_______ 。
(3)设计实验检验深蓝色晶体 中的阴离子
中的阴离子_______ 。
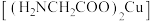 是人体摄取铜元素的主要来源之一。甘氨酸铜存在顺式和反式两种构型,其中一种构型易溶于水,另一种构型相对微溶于水。
是人体摄取铜元素的主要来源之一。甘氨酸铜存在顺式和反式两种构型,其中一种构型易溶于水,另一种构型相对微溶于水。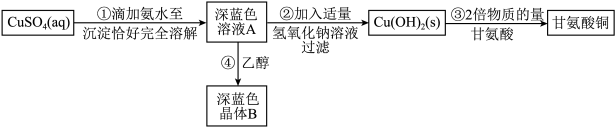
(2)①甘氨酸铜中
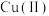 的配位数为4,画出其中一种构型的结构简式
的配位数为4,画出其中一种构型的结构简式②下列说法正确的是
A.甘氨酸易溶于水,可溶于乙醇、丙酮等有机溶剂
B.可向硫酸铜溶液中滴加过量氢氧化钠溶液直接制得

C.步骤①可说明与铜离子的配位能力:
 大于
大于
D.反式甘氨酸铜在水中的溶解度要小于顺式甘氨酸铜
③
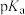 :甘氨酸
:甘氨酸(3)设计实验检验深蓝色晶体
 中的阴离子
中的阴离子
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】三氧化二砷(As2O3),无臭无味,外观为白色霜状粉末,微溶于水。请回答下列问题:
(1)As2O3中As元素的化合价为____ 价。
(2)As2O3与NaOH溶液反应的化学方程式为As2O3+2NaOH=2NaAsO2+H2O,该反应_____ (填“属于”或“不属于”)氧化还原反应,该反应的离子方程式为______ 。
(3)已知As2O3与Zn可发生反应6Zn+As2O3+6H2SO4=2AsH3↑+6ZnSO4+3H2O,其中氢元素的化合价未发生变化。
①上述反应中的氧化剂为______ (填化学式),被氧化的元素为______ (填元素符号)。
②若有9.9 g As2O3完全反应,则生成的AsH3的质量为_____ g。
(1)As2O3中As元素的化合价为
(2)As2O3与NaOH溶液反应的化学方程式为As2O3+2NaOH=2NaAsO2+H2O,该反应
(3)已知As2O3与Zn可发生反应6Zn+As2O3+6H2SO4=2AsH3↑+6ZnSO4+3H2O,其中氢元素的化合价未发生变化。
①上述反应中的氧化剂为
②若有9.9 g As2O3完全反应,则生成的AsH3的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在铜与稀硝酸的反应8HNO3+3Cu=3Cu(NO3)2+aNO↑+4H2O中,a的值为____ ,____ 元素被氧化,化合价____ (填“升高”或“降低”),该反应中____ 是还原剂,____ 是氧化剂;____ 是氧化产物,____ 是还原产物;每生成1个NO转移电子____ 个。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】Ⅰ.现有下列物质:①固体氢氧化钡,②石墨棒,③纯醋酸,④液态氯化氢,⑤硫酸氢钾固体,⑥熔融氯化钠,⑦酒精(C2H5OH),⑧碳酸钠粉末。请用序号回答下列问题:
(1)以上物质中能导电的是_______ 。
(2)以上物质中属于电解质的是_______ 。
(3)以上物质中属于非电解质的是_______ 。
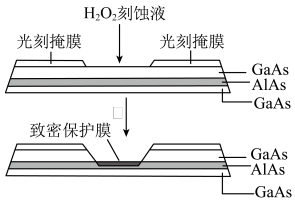
Ⅱ.高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。
(4)已知:Ga和Al最外层电子数相同,As和N最外层电子数相同。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂的物质的量之比为_______ 。
(5)配平下列化学方程式_______ 。
_______Cu+_______HNO3(稀)=_______Cu(NO3)2+_______NO↑+_______H2O
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
Ⅱ.高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。

(4)已知:Ga和Al最外层电子数相同,As和N最外层电子数相同。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂的物质的量之比为
(5)配平下列化学方程式
_______Cu+_______HNO3(稀)=_______Cu(NO3)2+_______NO↑+_______H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】硫、氮元素是高中化学学习的两种重要非金属元素,其价类二维图分别如图所示:
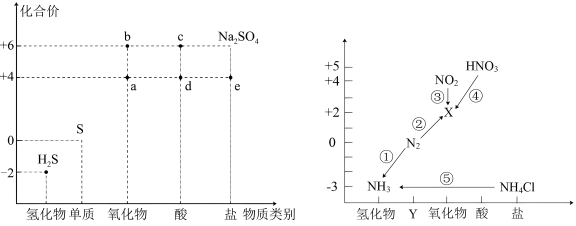
(1)c物质的浓溶液与金属铜发生反应的化学方程式为:_____ 。
(2)a与H2S发生反应的化学方程式:_____ 。
(3)实验室用⑤途径制备NH3的化学方程式为:_____ 。
(4)氨气是工业制硝酸的重要原料,写出①反应的化学方程式_____ 。
(5)关于氮及其化合物的说法错误的是_____ 。

(1)c物质的浓溶液与金属铜发生反应的化学方程式为:
(2)a与H2S发生反应的化学方程式:
(3)实验室用⑤途径制备NH3的化学方程式为:
(4)氨气是工业制硝酸的重要原料,写出①反应的化学方程式
(5)关于氮及其化合物的说法错误的是
| A.氮气分子结构稳定,常做保护气,不支持任何物质燃烧 |
| B.NO、NO2均为大气污染气体,在大气中均可稳定存在 |
| C.可用浓盐酸检测输送NH3的管道是否发生泄漏 |
| D.HNO3具有强氧化性,可溶解铜、银等不活泼金属 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】Cu和稀硝酸在一定条件下反应会生成无色气体一氧化氮,其变化可表述为:___Cu+___HNO3(稀)——___Cu(NO3)2+___NO↑+__H2O
(1)氧化剂是___ ,还原剂是__ ;氧化产物是__ ,还原产物是_ 。
(2)稀硝酸在反应中显示出来的性质是__ (填编号)
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)配平上述化学方程式___ 。
(4)产生0.2molH2O,则转移电子的物质的量为__ mol。
(1)氧化剂是
(2)稀硝酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)配平上述化学方程式
(4)产生0.2molH2O,则转移电子的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)漂白粉有效成分的化学式是___________ ;氯化钠的电子式是___________ 。
(2)高温条件下铁与水蒸气反应的化学方程式是___________ 。
(3)铜和稀硝酸反应的离子方程式是___________ 。
(1)漂白粉有效成分的化学式是
(2)高温条件下铁与水蒸气反应的化学方程式是
(3)铜和稀硝酸反应的离子方程式是
您最近一年使用:0次




