下列用来表示物质变化的化学用语中,正确的是
A.碱性氢氧燃料电池的负极反应式: |
| B.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
C.用惰性电极电解饱和食盐水时,阴极的电极反应式为: |
| D.在铁制品上镀银时,铁制品与电源正极相连,发生电极反应:Fe-2e-=Fe2+ |
更新时间:2022-11-08 23:36:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】如图所示原电池,盐桥中装有含琼胶的KCl饱和溶液,相关的叙述中,不正确的是
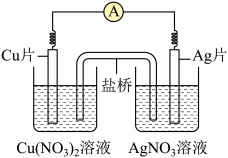

| A.正极的电极反应是Ag++e-=Ag |
| B.电子沿导线由Cu片流向Ag片 |
| C.盐桥中的K+向Cu片移动 |
| D.Cu片上发生氧化反应,Ag片上发生还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B.脱氧过程中铁作原电池正极,电极反应为:Fe-3e-=Fe3+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e-=4OH- |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气0.015mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】富锂锰基正极材料xLi2MnO3·(1-x)LiMO2(M=Fe、Co、Ni等)组成的电池具有容量高、储量丰富、价格便宜、污染小等优点,有可能成为未来电动汽车动力源,该电池首次充电会受电压影响要经历两个阶段:
第一阶段(锂离子脱出):xLi2MnO3·(1-x)LiMO2-(1-x)e-=xLi2MnO3·(1-x)MO2+(1-x)Li+
第二阶段(Li2O脱出及富锂正极材料的电化学活化):xLi2MnO3·(1-x)MO2-=xMnO2·(1-x)MO2+xLi2O
以下相关叙述错误的是
第一阶段(锂离子脱出):xLi2MnO3·(1-x)LiMO2-(1-x)e-=xLi2MnO3·(1-x)MO2+(1-x)Li+
第二阶段(Li2O脱出及富锂正极材料的电化学活化):xLi2MnO3·(1-x)MO2-=xMnO2·(1-x)MO2+xLi2O
以下相关叙述错误的是
| A.放电时富锂正极材料可能发生反应:xMnO2·(1-x)MO2+xe-+Li+=xLiMnO2·(1-x)LiMO2 |
| B.充电的第一阶段金属M被氧化,第二阶段金属Mn被氧化 |
| C.充电时,随着Li+脱出,富锂锰基材料Li1.2Ni0.13Co0.13Mn0.54O2中Ni和Co化合价升高 |
| D.充电时正极材料质量减小,锂离子向负极移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用镁-次氯酸盐电池为电源,模拟电浮选凝聚法处理污水示意图如图所示,通过铁和石墨电极在污水中电解,利用污水中溶解的氧将生成的Fe2+转化为Fe(OH)3沉淀吸附污染物,气泡把污水中悬浮物带到水面形成浮渣层,从而达到净水的目的。下列说法错误的是
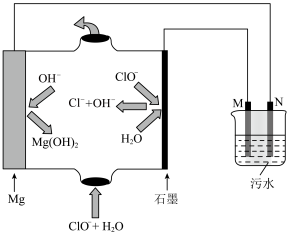

| A.镁-次氯酸盐电池总反应的离子方程式为Mg+ClO-+H2O=Mg(OH)2+Cl- |
| B.M应是石墨电极,N应是铁电极 |
| C.生成Fe(OH)3,沉淀反应的离子方程式为4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ |
| D.将污水中悬浮物带到水面形成浮渣层的气泡成分主要是H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】能正确表示下列反应的离子方程式是
A.用惰性电极电解NaCl水溶液:2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
B.(NH4)2Fe(SO4)2溶液与等物质的量Ba(OH)2溶液混合:SO +Ba2++NH +Ba2++NH +OH-=NH3•H2O+BaSO4↓ +OH-=NH3•H2O+BaSO4↓ |
C.向NaClO溶液中通入足量的SO2:2ClO-+H2O+SO2=2HClO+SO |
D.乙酸乙酯与NaOH溶液共热:CH3COOCH2CH3+OH- CH3COO-+CH3CH2OH CH3COO-+CH3CH2OH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用如图所示装置模拟电解原理在工业生产中的应用,下列说法正确的是
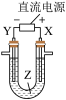

| A.在铁片上镀铜时,每转移2mol电子,Y极增重64g |
B.电解精炼铜时,Z溶液中的 浓度不变 浓度不变 |
C.氯碱工业中,X电极上的反应式是 |
| D.制取金属铝时,Z是熔融的氯化铝 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】关于下列装置说法正确的是


| A.装置①中,盐桥中的K+移向ZnSO4 |
| B.装置②中滴入酚酞,a极附近变红 |
| C.用装置③精炼铜时,c极为粗铜 |
| D.装置④中发生吸氧腐蚀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.用电解粗铜的方法精炼铜,当阳极失去0.1NA个电子时,则阳极质量减少3.2g |
| B.常温下,pH=3的NH4Cl溶液中,由水电离的H+数为0.001NA |
| C.向含有FeI2的溶液中通入适量氯气,当有1molFe2+被氧化时该反应转移的电子数至少为3NA |
| D.标准状况下,2.24L二氯甲烷中含有的碳氯共价键数目为0.2NA |
您最近一年使用:0次

 等共存物的存在会影响水体修复效果。下列说法错误的是
等共存物的存在会影响水体修复效果。下列说法错误的是
 +3H2O
+3H2O =BaSO4↓
=BaSO4↓