Ⅰ.根据下图转化关系及现象回答问题:
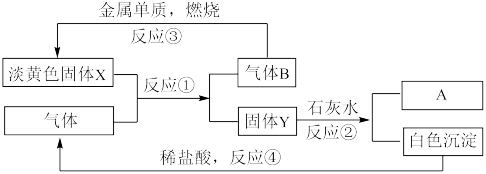
(1)物质A是_______ (填写化学式)
(2)反应①的化学方程式为_______ 。
II.将少量金属钠投入盛有下列溶液的小烧杯中,
(3)既有气体,又有白色沉淀产生的是_______ 。(填序号)
①NaCl溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液 ⑧
溶液 ⑧ 溶液
溶液
Ⅲ.我国科学家侯德榜发明的联合制碱法,对世界制碱工业以及我国化工事业的发展做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已省略)。
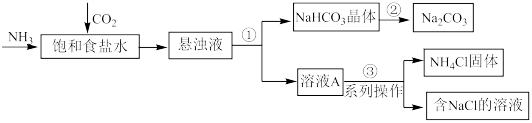
(4)步骤①②③中涉及“过滤”操作的是_______ (填序号)。
(5)向饱和食盐水中通入 和
和 后,生成
后,生成 的化学方程式是
的化学方程式是_______ 。
(6)从步骤①中分离出的 晶体表面含有的杂质可能是
晶体表面含有的杂质可能是_______ (写出杂质的化学式),欲得到纯净的 ,需将其洗涤、干燥。判断
,需将其洗涤、干燥。判断 固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,_______ 。

(1)物质A是
(2)反应①的化学方程式为
II.将少量金属钠投入盛有下列溶液的小烧杯中,
(3)既有气体,又有白色沉淀产生的是
①NaCl溶液 ②
 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液 ⑧
溶液 ⑧ 溶液
溶液Ⅲ.我国科学家侯德榜发明的联合制碱法,对世界制碱工业以及我国化工事业的发展做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已省略)。

(4)步骤①②③中涉及“过滤”操作的是
(5)向饱和食盐水中通入
 和
和 后,生成
后,生成 的化学方程式是
的化学方程式是(6)从步骤①中分离出的
 晶体表面含有的杂质可能是
晶体表面含有的杂质可能是 ,需将其洗涤、干燥。判断
,需将其洗涤、干燥。判断 固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
固体已经纯净的操作方法是:取少量最后一次洗涤液于试管中,
更新时间:2022-11-16 07:27:21
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】A、B、C、D是初中化学常见的物质,在一定条件下四种物质存在如下图所示的转化关系:A + B → C + D。
→ C + D。
(1)若A是硫酸,B是氢氧化钠,该反应的基本类型是__________ 反应。
(2)若A、C均是含同种元素的非金属氧化物,且A有毒性,D能被磁铁吸引。则C的化学式是___________ ;D的合金可用于制作炊具,主要是利用它的_________ 性。
(3)若A、C是都是金属单质,B、D都是盐,该反应说明金属活动性:A_____ (选填“<”或“>”)C。
 → C + D。
→ C + D。(1)若A是硫酸,B是氢氧化钠,该反应的基本类型是
(2)若A、C均是含同种元素的非金属氧化物,且A有毒性,D能被磁铁吸引。则C的化学式是
(3)若A、C是都是金属单质,B、D都是盐,该反应说明金属活动性:A
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】甲、乙、丙、X是中学化学中常见的物质,在一定条件下,它们之间的转化关系如下图所示(部分产物已略去)。请回答下列问题:
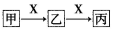
(1)若X是 O2,则甲不可能是______ (填代号)
a.Mg b.N2 c.S d.Al
(2)若甲能使湿润的红色石蕊试纸变蓝,丙为红棕色气体。写出甲转化为乙的化学方程式:________________________________________ 。
(3)若乙是一种常见的温室气体,则X的化学式为__________ 。
(4)若丙为淡黄色粉末,常用作呼吸面具中的供氧剂,则丙与水反应的离子方程式为______ ;1mol丙与水发生反应时转移电子的物质的量为______ mol。
(5)若X是一种常见的金属单质,常温下甲的浓溶液可盛放在铝制容器中,丙为浅绿色溶液。
①检验乙是否完全转化为丙的试剂为_______ (填试剂名称)。
②保存丙溶液常加入少量X,其目的是____________ 。
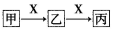
(1)若X是 O2,则甲不可能是
a.Mg b.N2 c.S d.Al
(2)若甲能使湿润的红色石蕊试纸变蓝,丙为红棕色气体。写出甲转化为乙的化学方程式:
(3)若乙是一种常见的温室气体,则X的化学式为
(4)若丙为淡黄色粉末,常用作呼吸面具中的供氧剂,则丙与水反应的离子方程式为
(5)若X是一种常见的金属单质,常温下甲的浓溶液可盛放在铝制容器中,丙为浅绿色溶液。
①检验乙是否完全转化为丙的试剂为
②保存丙溶液常加入少量X,其目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】B、D、C、A、E 五种元素的原子序数顺序依次增大,其中只有E为金属元素,D、C 元素在元素周期表中位置相邻,在一定条件下,B 的单质可以分别和A、C、D 的单质化合生成甲、乙、丙化合物,C 的单质和D 的单质化合可得丁,戊、己、庚均为化合物。已知乙、丙每个分子中均含有10 个电子,下图为相互转化关系:
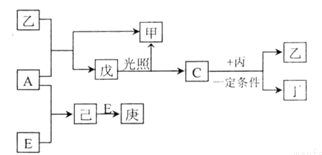
请回答下列问题:
(1)写出E 的原子结构示意图_____________ 。
(2)写出C、D 氢化物的稳定性由强到弱的顺序_________ (用化学式表示)。
(3)A、B、D 三种元素形成的化合物中其中一种可用作化肥,写该化合物的电子式__________ 。
(4)写出C与丙反应的化学反应方程式________________ 。
(5)写出工业上从海水中制取A 的离子反应方程式_______________ 。
(6)工业上通过如下转化可制得含A 元素的钾盐KAO3 晶体:
NaA溶液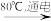 NaAO3
NaAO3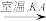 KAO3晶体
KAO3晶体
Ⅰ Ⅱ
①完成Ⅰ中反应的总化学方程式:___________________ 。
NaA+□H2O □NaAO3+□
□NaAO3+□
②Ⅱ中反应过程能析出KClO3晶体而无其他晶体析出的原因是_____________ 。

请回答下列问题:
(1)写出E 的原子结构示意图
(2)写出C、D 氢化物的稳定性由强到弱的顺序
(3)A、B、D 三种元素形成的化合物中其中一种可用作化肥,写该化合物的电子式
(4)写出C与丙反应的化学反应方程式
(5)写出工业上从海水中制取A 的离子反应方程式
(6)工业上通过如下转化可制得含A 元素的钾盐KAO3 晶体:
NaA溶液
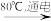 NaAO3
NaAO3 KAO3晶体
KAO3晶体Ⅰ Ⅱ
①完成Ⅰ中反应的总化学方程式:
NaA+□H2O
 □NaAO3+□
□NaAO3+□ ②Ⅱ中反应过程能析出KClO3晶体而无其他晶体析出的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)将金属钠放入盛有下列溶液的小烧杯中,既有气体又有白色沉淀产生的是________ 。
①MgSO4溶液 ② NaCl溶液 ③Na2SO4溶液 ④饱和澄清石灰水 ⑤Ca(HCO3)2溶液⑥CuSO4溶液 ⑦饱和NaCl溶液
(2)按要求书写下列反应的总离子方程式。
①将Na投入CuSO4溶液中:________________________________ 。
②将Na投入NH4HCO3溶液中,有刺激性气味气体放出:_________________________ 。
①MgSO4溶液 ② NaCl溶液 ③Na2SO4溶液 ④饱和澄清石灰水 ⑤Ca(HCO3)2溶液⑥CuSO4溶液 ⑦饱和NaCl溶液
(2)按要求书写下列反应的总离子方程式。
①将Na投入CuSO4溶液中:
②将Na投入NH4HCO3溶液中,有刺激性气味气体放出:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)下列物质属于非电解质的是__________
A.NH3 B.(NH4)2SO4 C.Cl2 D.CH3COOH
(2)将金属钠投入到下列溶液中,溶液质量会减少的是_____________
A.盐酸 B.硫酸铜溶液 C.水 D.氢氧化钠溶液
A.NH3 B.(NH4)2SO4 C.Cl2 D.CH3COOH
(2)将金属钠投入到下列溶液中,溶液质量会减少的是
A.盐酸 B.硫酸铜溶液 C.水 D.氢氧化钠溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】过一硫酸(H2SO5) 和过二硫酸(H2S2O8) 都是硫的含氧酸。过一硫酸是一种一元强酸,可用于游泳池消毒,其结构式如图所示,过二硫酸是一种白色晶体,受热易分解,有强吸水性,极易溶于水且在水中会逐渐水解得到硫酸和过氧化氢。请回答下列相关问题。
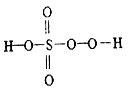
(1)过一硫酸中硫元素的化合价是_________ 。过二硫酸的结构式是_________ 。
(2)过一硫酸用于游泳池消毒是利用它的_________ 。(填性质)
(3)过硫酸盐受热也易分解,如过二硫酸钾(K2S2O8) 受热会放出SO3和O2,该反应的化学方程式是_________ ,该反应中每转移4NA个电子,生成的O2在标准状况下的体积是_________ 。
(4)实验室常用氯磺酸(ClSO3H) 和H2O2混合制H2S2O8:H2O2 + 2 ClSO3H = H2S2O8+2HCl,要制得高纯度的H2S2O8关键在于反应体系要处于___________ 环境。

(1)过一硫酸中硫元素的化合价是
(2)过一硫酸用于游泳池消毒是利用它的
(3)过硫酸盐受热也易分解,如过二硫酸钾(K2S2O8) 受热会放出SO3和O2,该反应的化学方程式是
(4)实验室常用氯磺酸(ClSO3H) 和H2O2混合制H2S2O8:H2O2 + 2 ClSO3H = H2S2O8+2HCl,要制得高纯度的H2S2O8关键在于反应体系要处于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是_______。
(2)海水中所得粗盐中通常含 、
、 、
、 等杂质。
等杂质。
①为了得到精盐,下列试剂加入的先后顺序正确的是_______ 。
A.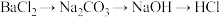 B.
B.
C. D.
D.
②为了检验精盐中是否含有 ,正确的方法是
,正确的方法是_______ 。
(3)月壤中含有丰富的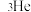 ,从月壤中提炼
,从月壤中提炼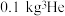 同时可得
同时可得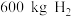 和
和 ,若以所得
,若以所得 和
和 为原料经一系列反应最多可制得碳酸氢铵
为原料经一系列反应最多可制得碳酸氢铵_______  。
。
(4)将 溶液和
溶液和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液温度,实验结果如图所示
溶液混合均匀后测量并记录溶液温度,实验结果如图所示 已知:实验中始终保持
已知:实验中始终保持 ,酸碱恰好完全反应时,体系的温度最高
,酸碱恰好完全反应时,体系的温度最高 。请按要求填空:
。请按要求填空:
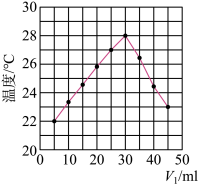
该实验表明此反应_______  填“吸收”或“释放”
填“吸收”或“释放” 能量,由图示分析可以得出做该实验时,环境温度
能量,由图示分析可以得出做该实验时,环境温度_______  填“高于”“低于”或“等于
填“高于”“低于”或“等于 。根据图示计算该
。根据图示计算该 溶液的浓度约是
溶液的浓度约是_______  。
。
(5)设计实验方案:选择合适的试剂,用二氧化硅制硅酸_______ 。(用流程图表达,例:A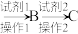 ……)
……)
(1)浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是_______。
| A.酸性 | B.脱水性 | C.强氧化性 | D.吸水性 |
 、
、 、
、 等杂质。
等杂质。①为了得到精盐,下列试剂加入的先后顺序正确的是
A.
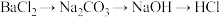 B.
B.
C.
 D.
D.
②为了检验精盐中是否含有
 ,正确的方法是
,正确的方法是(3)月壤中含有丰富的
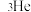 ,从月壤中提炼
,从月壤中提炼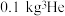 同时可得
同时可得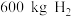 和
和 ,若以所得
,若以所得 和
和 为原料经一系列反应最多可制得碳酸氢铵
为原料经一系列反应最多可制得碳酸氢铵 。
。(4)将
 溶液和
溶液和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液温度,实验结果如图所示
溶液混合均匀后测量并记录溶液温度,实验结果如图所示 已知:实验中始终保持
已知:实验中始终保持 ,酸碱恰好完全反应时,体系的温度最高
,酸碱恰好完全反应时,体系的温度最高 。请按要求填空:
。请按要求填空:
该实验表明此反应
 填“吸收”或“释放”
填“吸收”或“释放” 能量,由图示分析可以得出做该实验时,环境温度
能量,由图示分析可以得出做该实验时,环境温度 填“高于”“低于”或“等于
填“高于”“低于”或“等于 。根据图示计算该
。根据图示计算该 溶液的浓度约是
溶液的浓度约是 。
。(5)设计实验方案:选择合适的试剂,用二氧化硅制硅酸
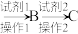 ……)
……)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 是重要的化工原料。以软锰矿(主要成分为
是重要的化工原料。以软锰矿(主要成分为 ,杂质有
,杂质有 和
和 )为原料,经研磨、还原、纯化、电解等步骤,可制备
)为原料,经研磨、还原、纯化、电解等步骤,可制备 。
。
资料:①题给条件下, 不与硫酸反应。
不与硫酸反应。
②金属离子沉淀的pH
(1)向一定量研磨后的软锰矿中加入过量 和过量铁屑,在50℃充分反应后过滤,向所得滤液中先加入
和过量铁屑,在50℃充分反应后过滤,向所得滤液中先加入 ,充分反应后再加入
,充分反应后再加入 调溶液的
调溶液的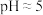 ,过滤,得到
,过滤,得到 纯化液,电解
纯化液,电解 纯化液得到纯净的
纯化液得到纯净的 。
。
①加入 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
②加入 调溶液
调溶液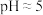 的目的是
的目的是_______ 。
(2)产品 纯度测定。向
纯度测定。向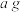 产品中依次加入
产品中依次加入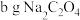 和足量稀
和足量稀 ,加热至80℃(温度过高草酸易分解)使之充分反应,再用
,加热至80℃(温度过高草酸易分解)使之充分反应,再用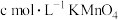 溶液滴定剩余
溶液滴定剩余 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 。涉及的离子反应方程式为
。涉及的离子反应方程式为
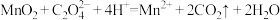
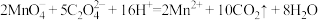
①上述实验中若加热温度过高,产品中的 质量分数的测定结果将
质量分数的测定结果将_______ (填“偏大”或“偏小”或“无影响”)。
②计算该产品中 的质量分数
的质量分数_______ (写出计算过程;相对分子质量: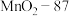 ;
;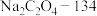 )。
)。
 是重要的化工原料。以软锰矿(主要成分为
是重要的化工原料。以软锰矿(主要成分为 ,杂质有
,杂质有 和
和 )为原料,经研磨、还原、纯化、电解等步骤,可制备
)为原料,经研磨、还原、纯化、电解等步骤,可制备 。
。资料:①题给条件下,
 不与硫酸反应。
不与硫酸反应。②金属离子沉淀的pH
 |  |  |  | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
 和过量铁屑,在50℃充分反应后过滤,向所得滤液中先加入
和过量铁屑,在50℃充分反应后过滤,向所得滤液中先加入 ,充分反应后再加入
,充分反应后再加入 调溶液的
调溶液的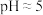 ,过滤,得到
,过滤,得到 纯化液,电解
纯化液,电解 纯化液得到纯净的
纯化液得到纯净的 。
。①加入
 氧化
氧化 的离子方程式为
的离子方程式为②加入
 调溶液
调溶液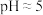 的目的是
的目的是(2)产品
 纯度测定。向
纯度测定。向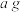 产品中依次加入
产品中依次加入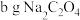 和足量稀
和足量稀 ,加热至80℃(温度过高草酸易分解)使之充分反应,再用
,加热至80℃(温度过高草酸易分解)使之充分反应,再用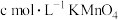 溶液滴定剩余
溶液滴定剩余 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 。涉及的离子反应方程式为
。涉及的离子反应方程式为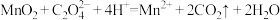
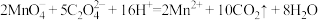
①上述实验中若加热温度过高,产品中的
 质量分数的测定结果将
质量分数的测定结果将②计算该产品中
 的质量分数
的质量分数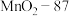 ;
;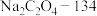 )。
)。
您最近一年使用:0次



