某无色透明溶液中可能大量存在 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种。某校实验小组对此进行了如下检验:
中的几种。某校实验小组对此进行了如下检验:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ (填离子符号,下同)。
(2)取少量原溶液,加入过量稀硫酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ 。
(3)取少量原溶液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有_______ ,有关的离子方程式为_______ 。
(4)原溶液中可能存在的阴离子是_______ (填字母)。
A. B.
B. C.
C. D.
D. E.
E.
(5)原溶液还可能含有的阳离子是_______ ,可通过_______ 检验,写出检验方法及现象结论:_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种。某校实验小组对此进行了如下检验:
中的几种。某校实验小组对此进行了如下检验:(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀硫酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取少量原溶液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液中可能存在的阴离子是
A.
 B.
B. C.
C. D.
D. E.
E.
(5)原溶液还可能含有的阳离子是
更新时间:2022-11-23 11:03:58
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】有一无色透明溶液,欲确定其是否含有下列离子: 、
、 、
、 、
、 、
、 、
、 、
、 ,实验如下:
,实验如下:
①用玻璃棒蘸取少量该溶液,点在pH试纸中部,试纸变为红色;
②取少量该溶液,加入过量 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
③取②中反应后的上层清液,加入 溶液,有白色沉淀生成,且不溶于稀硝酸;
溶液,有白色沉淀生成,且不溶于稀硝酸;
④取少量原溶液,加入过量的NaOH溶液,有白色沉淀生成。
回答下列问题:
(1)溶液中一定存在的离子是______ ;溶液中肯定不存在的离子是______ 。
(2)分别写出实验②、③中发生反应的离子方程式:______ 。
(3)写出实验④中生成的沉淀的化学式:______ 。
(4)不能确定是否含有的离子是______ ,为了进一步确定其是否存在,应该补充的实验是______ (写出实验操作、现象和结论)。
 、
、 、
、 、
、 、
、 、
、 、
、 ,实验如下:
,实验如下:①用玻璃棒蘸取少量该溶液,点在pH试纸中部,试纸变为红色;
②取少量该溶液,加入过量
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;③取②中反应后的上层清液,加入
 溶液,有白色沉淀生成,且不溶于稀硝酸;
溶液,有白色沉淀生成,且不溶于稀硝酸;④取少量原溶液,加入过量的NaOH溶液,有白色沉淀生成。
回答下列问题:
(1)溶液中一定存在的离子是
(2)分别写出实验②、③中发生反应的离子方程式:
(3)写出实验④中生成的沉淀的化学式:
(4)不能确定是否含有的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某溶液中可能含有下列阴离子:SO42-、SO32-、CO32-、Cl-。
(1)当溶液中存在大量H+时,溶液中不能大量存在的离子是_____________ 。
(2)当溶液中存在大量的Ba2+时,溶液中能大量存在的离子是_____________ 。
(3)当溶液中同时存在大量_____ 和_____ 离子时,上述阴离子都不能大量不存在。
(1)当溶液中存在大量H+时,溶液中不能大量存在的离子是
(2)当溶液中存在大量的Ba2+时,溶液中能大量存在的离子是
(3)当溶液中同时存在大量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.请根据题目要求,写出下列反应的离子方程式。
(1)向 溶液中加入NaOH溶液离子方程式:
溶液中加入NaOH溶液离子方程式:___________ 。
(2)将碳酸氢钠溶液与稀盐酸混合离子方程式:___________ 。
(3)湿法炼铜,曾青得铁化为铜的离子方程式:___________ 。
Ⅱ.有一瓶透明澄清的溶液,其中可能含有 、
、 、
、 、
、 、
、 ,取该溶液进行以下实验:
,取该溶液进行以下实验:
①取pH试纸检验,测得溶液呈强酸性。
②另取部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,有白色沉淀产生。
请回答下列问题:
(4)用pH试纸检验,表明溶液呈强酸性,可以排除___________ 的存在。
(5)步骤②中产生白色沉淀的离子方程式为___________ 。
(6)该溶液中可能存在的离子为___________ ,请设计实验验证该离子是否存在:___________ 。
(7)根据上述实验事实能确定溶液中肯定存在的离子是___________ 。
(1)向
 溶液中加入NaOH溶液离子方程式:
溶液中加入NaOH溶液离子方程式:(2)将碳酸氢钠溶液与稀盐酸混合离子方程式:
(3)湿法炼铜,曾青得铁化为铜的离子方程式:
Ⅱ.有一瓶透明澄清的溶液,其中可能含有
 、
、 、
、 、
、 、
、 ,取该溶液进行以下实验:
,取该溶液进行以下实验:①取pH试纸检验,测得溶液呈强酸性。
②另取部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,有白色沉淀产生。
请回答下列问题:
(4)用pH试纸检验,表明溶液呈强酸性,可以排除
(5)步骤②中产生白色沉淀的离子方程式为
(6)该溶液中可能存在的离子为
(7)根据上述实验事实能确定溶液中肯定存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠的四种无色溶液,为了测定四种溶液各是什么?将它们随意编号为A、B、C、D后,按下表进行实验。产生的现象如表所示:
回答下列问题:
(1)A、C溶液中分散质的化学式:A:___________ ;C:___________ 。
(2)写出实验顺序②③中有关的离子反应方程式。
②___________ 。
③___________ 。
(3)写出下列反应的离子方程式:向NaHSO4溶液逐滴加Ba(OH)2溶液至SO 刚好沉淀完全:
刚好沉淀完全:___________ 。
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有现象发生 |
| ② | B+D | 有气体放出 |
| ③ | B+C | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
(1)A、C溶液中分散质的化学式:A:
(2)写出实验顺序②③中有关的离子反应方程式。
②
③
(3)写出下列反应的离子方程式:向NaHSO4溶液逐滴加Ba(OH)2溶液至SO
 刚好沉淀完全:
刚好沉淀完全:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_______ (填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中可能含有下列离子中的某些离子: 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。取该溶液进行如下实验:
。取该溶液进行如下实验:
Ⅰ.取少许原溶液,滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许原溶液,滴入 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。
Ⅲ.取少许原溶液先滴加稀硝酸,再滴入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
Ⅳ.取少许原溶液,滴入少量 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是_______ ;肯定存在的离子是_______ 。
②若原溶液中各种离子的浓度相等,确定该溶液中_______ (填“有”或“无”) ,判断依据是
,判断依据是_______ 。
③若原溶液中各离子的浓度相等,取一定量该溶液,加入等体积的稀硫酸(其中硫酸根浓度与原溶液中各离子浓度相等),写出发生反应的离子方程式:_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中可能含有下列离子中的某些离子:
 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。取该溶液进行如下实验:
。取该溶液进行如下实验:Ⅰ.取少许原溶液,滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许原溶液,滴入
 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。Ⅲ.取少许原溶液先滴加稀硝酸,再滴入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。Ⅳ.取少许原溶液,滴入少量
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。①根据以上现象判断,原溶液中肯定不存在的离子是
②若原溶液中各种离子的浓度相等,确定该溶液中
 ,判断依据是
,判断依据是③若原溶液中各离子的浓度相等,取一定量该溶液,加入等体积的稀硫酸(其中硫酸根浓度与原溶液中各离子浓度相等),写出发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈__________ 色。
(2)实验室中需0.2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是__________ 。
A. 1000mL;21.2g B.950mL;20.14g C.500mL;21.2g D.500mL;10.6g
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为______ 。
(4)某同学为确定一包可能由碳酸钠和碳酸氢钠组成的白色混合物的成分,他取少量该白色物质溶于水,并向所得溶液中加入适量澄清石灰水,产生白色沉淀,据此该同学认为有碳酸钠。你是否同意该同学的观点,请你用适当的化学方程式阐述你的观点________ 。
(5)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:

①曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为_______ mL。
②曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________ ,其物质的量之比为________ 。
(1)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈
(2)实验室中需0.2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是
A. 1000mL;21.2g B.950mL;20.14g C.500mL;21.2g D.500mL;10.6g
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为
(4)某同学为确定一包可能由碳酸钠和碳酸氢钠组成的白色混合物的成分,他取少量该白色物质溶于水,并向所得溶液中加入适量澄清石灰水,产生白色沉淀,据此该同学认为有碳酸钠。你是否同意该同学的观点,请你用适当的化学方程式阐述你的观点
(5)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:

①曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为
②曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识填空
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:___________ 。
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
(3)向1mol KAl(SO4)2溶液中滴加Ba(OH)2溶液至沉淀的物质的量最大时的离子方程式___________
(4)现有以下四种物质:
请根据题意选择恰当的选项用字母代号填空。
①可与KSCN溶液反应,溶液变红的是___________ ;
②常用于焙制糕点,也可用作抗酸药的是___________ ;
③可用于制备硅胶和木材防火剂的是___________ ;
④可用于制造计算机芯片的是___________ 。
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
| A.黄绿色 | B.洋红色 | C.紫红色 | D.绿色 |
(4)现有以下四种物质:
| A.Si | B.FeCl3 | C.NaHCO3 | D.Na2SiO3 |
①可与KSCN溶液反应,溶液变红的是
②常用于焙制糕点,也可用作抗酸药的是
③可用于制备硅胶和木材防火剂的是
④可用于制造计算机芯片的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4)反应的产物,以其产物为原料制备氯气:室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。分析实验并回答相应问题。
(1)M的化学式是_____ ,组成草酸的三种元素中,非金属性最强的是_____ (填元素符号)。
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为_____ ,向滤液中加入盐酸时又产生无色无味气体,该反应的离子方程式为______ 。
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是_____ 。
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为_____ 。
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:______ 。
(1)M的化学式是
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在Na+浓度为0.5mol/L的某澄清溶液中,还可能含有下表中若干种离子
现取该溶液100mL进行如下实验(气体体积均在标准状况下测定)。
查阅资料可知:硅酸( )是一种酸性极弱的难溶性酸,不稳定,加热易分解
)是一种酸性极弱的难溶性酸,不稳定,加热易分解
请回答下列问题:
(1)实验I能确定一定不存在的离子是_______ 。
(2)实验I中生成沉淀的离子方程式为_______ 。
(3)通过实验I、II、III和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)。
(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:___ 。
| 阳离子 |  |  |  |  |
| 阴离子 |  、 、 、 、 、 、 | |||
| 序号 | 实验内容 | 实验结果 |
| I | 向该溶液中加入足量稀盐酸 | 产生白色沉淀并放出标准状况下0.56L气体 |
| II | 将I的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| III | 向II的滤液中滴加 溶液 溶液 | 无明显现象 |
 )是一种酸性极弱的难溶性酸,不稳定,加热易分解
)是一种酸性极弱的难溶性酸,不稳定,加热易分解请回答下列问题:
(1)实验I能确定一定不存在的离子是
(2)实验I中生成沉淀的离子方程式为
(3)通过实验I、II、III和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)。
| 阴离子 |  |  |  |  |
| c/mol/L |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在一条河边有四座工厂:甲、乙、丙、丁(如图所示),它们所排出的废液里每厂只含有NaHCO3、FeCl3、Ca(OH)2、HCl中的一种。某环保小组对河水监测时发现:

①甲处河水呈乳白色
②乙处河水有红褐色沉淀
③丙处河水由浑浊变澄清
④丁处河水产生气泡,河水仍澄清
请推断四座工厂排出的废液里含有的物质分别是(填化学式):
甲:___ ,乙:___ ,丙:___ ,丁:___ 。

①甲处河水呈乳白色
②乙处河水有红褐色沉淀
③丙处河水由浑浊变澄清
④丁处河水产生气泡,河水仍澄清
请推断四座工厂排出的废液里含有的物质分别是(填化学式):
甲:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.现有以下物质:①石墨;②乙醇;③氨水;④二氧化碳;⑤碳酸钠固体;⑥氢氧化钡溶液;⑦纯醋酸;⑧氯化氢气体。(填序号)
(1)其中能导电的是_______ ;属于非电解质的是_______ ;属于电解质的是_______ 。
II.某100mL溶液可能含有 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知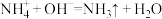 ,气体全部逸出)。
,气体全部逸出)。
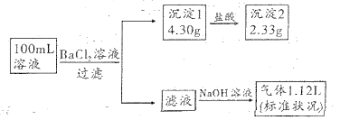
(2)原溶液中一定含有_______ 离子,可能含有_______ 离子。
(3)实验中生成硫酸钡的离子方程式为_______ 。
(4)原溶液中 的物质的量浓度范围是
的物质的量浓度范围是_______ 。
(5)对可能存在的离子用什么方法检验_______ 。
(1)其中能导电的是
II.某100mL溶液可能含有
 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知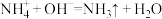 ,气体全部逸出)。
,气体全部逸出)。
(2)原溶液中一定含有
(3)实验中生成硫酸钡的离子方程式为
(4)原溶液中
 的物质的量浓度范围是
的物质的量浓度范围是(5)对可能存在的离子用什么方法检验
您最近一年使用:0次

 、H+、NO
、H+、NO
 、H+、AlO
、H+、AlO 、SO
、SO 、K+、
、K+、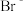 、NO
、NO 、Na+、SO
、Na+、SO
 、SO
、SO 、H+、
、H+、
 、SO
、SO 、Br-、OH-
、Br-、OH-


