离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_______ (填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中可能含有下列离子中的某些离子: 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。取该溶液进行如下实验:
。取该溶液进行如下实验:
Ⅰ.取少许原溶液,滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许原溶液,滴入 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。
Ⅲ.取少许原溶液先滴加稀硝酸,再滴入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
Ⅳ.取少许原溶液,滴入少量 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是_______ ;肯定存在的离子是_______ 。
②若原溶液中各种离子的浓度相等,确定该溶液中_______ (填“有”或“无”) ,判断依据是
,判断依据是_______ 。
③若原溶液中各离子的浓度相等,取一定量该溶液,加入等体积的稀硫酸(其中硫酸根浓度与原溶液中各离子浓度相等),写出发生反应的离子方程式:_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中可能含有下列离子中的某些离子:
 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。取该溶液进行如下实验:
。取该溶液进行如下实验:Ⅰ.取少许原溶液,滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许原溶液,滴入
 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。Ⅲ.取少许原溶液先滴加稀硝酸,再滴入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。Ⅳ.取少许原溶液,滴入少量
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。①根据以上现象判断,原溶液中肯定不存在的离子是
②若原溶液中各种离子的浓度相等,确定该溶液中
 ,判断依据是
,判断依据是③若原溶液中各离子的浓度相等,取一定量该溶液,加入等体积的稀硫酸(其中硫酸根浓度与原溶液中各离子浓度相等),写出发生反应的离子方程式:
22-23高一上·陕西西安·期中 查看更多[2]
更新时间:2022-11-21 15:16:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)以下为中学化学中常见的几种物质:
①氯化钠晶体②干冰③HCl气体④铜⑤硫酸钡晶体⑥酒精⑦熔融的硝酸钾
能导电的是_______ ;(填序号,下同)属于电解质的是_______ ;属于非电解质的是__________ ;属于氧化物的是:________ 。
(2)按要求写出方程式:
①Fe2(SO4)3电离方程式________________________________ 。
②硫酸氢钠在水溶液中的电离方程式______________________ 。
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是________ (填字母)。

①氯化钠晶体②干冰③HCl气体④铜⑤硫酸钡晶体⑥酒精⑦熔融的硝酸钾
能导电的是
(2)按要求写出方程式:
①Fe2(SO4)3电离方程式
②硫酸氢钠在水溶液中的电离方程式
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)选择适宜的物质完成下列反应,并写出有关反应的化学方程式:
① +2H+=CO2↑+H2O
+2H+=CO2↑+H2O____ 。
②Ag++Cl-=AgCl↓___ 。
(2)写出下列反应的离子方程式:
①盐酸溶解氢氧化铜沉淀___ 。
②硫酸氢钠溶液中加入少量碳酸钠溶液:___ 。
③碳酸氢钠溶液中加入少量氢氧化钠溶液:___ 。
(1)选择适宜的物质完成下列反应,并写出有关反应的化学方程式:
①
 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O②Ag++Cl-=AgCl↓
(2)写出下列反应的离子方程式:
①盐酸溶解氢氧化铜沉淀
②硫酸氢钠溶液中加入少量碳酸钠溶液:
③碳酸氢钠溶液中加入少量氢氧化钠溶液:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】酒后驾车是马路第一杀手。已知酒精(C2H5OH)能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生反应: 2K2Cr2O7+ 3C2H5OH+ 8H2SO4=2K2SO4+ 2Cr2(SO4)3+ 3CH3COOH+ 11H2O, 且知 和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
(1)该反应__________________ (填 “是”或“不是”)离子反应。.
(2)将上述化学方程式改写成离子方程式__________ 。
(3)该反应________________ (填“是”或“不是”)氧化还原反应,判断的依据是______________ 。
(4)能否用这一反应来检测司机是否酒后驾车________ (填“能” 或“否”),理由是_______________________ 。
 和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
和Cr3+在溶液中分别显橙色和绿色。回答下列问题:(1)该反应
(2)将上述化学方程式改写成离子方程式
(3)该反应
(4)能否用这一反应来检测司机是否酒后驾车
您最近一年使用:0次
【推荐1】(I)有以下10种物质,请回答下列问题:(填序号)
①石墨 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤NaHSO4溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩铜
(1)其中能导电的是_______ ;属于电解质的是______ ;属于非电解质的是_______ 。
(2)写出物质④和⑦反应的离子方程式:___________ 。
(3)写出过量的物质⑦和少量的物质⑤发生反应的离子方程式:_________ 。
(II)用一种试剂除去下列各物质中的杂质(括号内的物质)。写出所用试剂及离子方程式。
(1)NaCl溶液(Na2CO3):试剂_______ 离子方程式_____________ 。
(2)FeSO4溶液(CuSO4):试剂_______ 离子方程式_____________ 。
(III)
(1)K2FeO4可用作水处理剂,它可由以下反应制得:
3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,当有1mol K2FeO4生成时转移的电子数目为________ 。
(2)4NH3+6NO=5N2+6H2O反应中氧化产物和还原产物物质的量之比为________ 。
①石墨 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤NaHSO4溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩铜
(1)其中能导电的是
(2)写出物质④和⑦反应的离子方程式:
(3)写出过量的物质⑦和少量的物质⑤发生反应的离子方程式:
(II)用一种试剂除去下列各物质中的杂质(括号内的物质)。写出所用试剂及离子方程式。
(1)NaCl溶液(Na2CO3):试剂
(2)FeSO4溶液(CuSO4):试剂
(III)
(1)K2FeO4可用作水处理剂,它可由以下反应制得:
3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,当有1mol K2FeO4生成时转移的电子数目为
(2)4NH3+6NO=5N2+6H2O反应中氧化产物和还原产物物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有以下物质:①钠;② ;③NaOH;④
;③NaOH;④ ;⑤液氯;⑥氯水;⑦次氯酸钙;⑧氯化铁溶液;⑨澄清的石灰水;⑩稀盐酸。根据问题,请完成以下填空:
;⑤液氯;⑥氯水;⑦次氯酸钙;⑧氯化铁溶液;⑨澄清的石灰水;⑩稀盐酸。根据问题,请完成以下填空:
(1)以上物质中属于电解质的是
(2)以下两种物质溶于水,书写出相应的电离方程式。
 :
:
次氯酸钙:
(3)①与⑧反应,书写出该反应的总的离子方程式
(4)②与⑩反应,书写出相应的化学方程式
(5)④与少量的⑨反应,书写出相应的离子方程式
您最近一年使用:0次
【推荐3】已知:i.用毛笔蘸取少量30%的FeCl3溶液在铜片上写一个“Cu”,放置片刻后用少量蒸馏水冲洗铜片后,在铜片上会出现凹凸的“Cu”。ii.Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。
(1)写出i中反应的离子方程式:_______ 。
(2)反应ii中氧化剂与还原剂的物质的量之比为_______ ,当反应中有0.6mol电子转移时,生成NO的质量为_______ g。
(3)向含有0.2molFeCl3、0.2molCuCl2的混合溶液中加入0.1molZn,充分反应后溶液中没有固体存在,则溶液中的金属阳离子有Zn2+、_______ 。
(4)HNO3、Fe3+、Cu2+的氧化性由强到弱的顺序为_______ 。
(1)写出i中反应的离子方程式:
(2)反应ii中氧化剂与还原剂的物质的量之比为
(3)向含有0.2molFeCl3、0.2molCuCl2的混合溶液中加入0.1molZn,充分反应后溶液中没有固体存在,则溶液中的金属阳离子有Zn2+、
(4)HNO3、Fe3+、Cu2+的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl、OH、NO 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子
六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子_________ ,乙厂的废水中含有另外三种离子。
II.对于该两厂的废水,可采取下列两种方法来处理。
(1)如果在废水中加一定量___________ 选填:活性炭或铁粉),可以发生__________ (选填:基本反应类型)反应,离子方程式是__________ ,并且能够回收其中的金属__________ (填写金属元素符号)。
(2)将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式:___________ ;___________ 。经过滤后的废水主要含___________ ,可用来浇灌农田。从过滤后的废水中提取溶质的方法是 __________ 。
 六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子
六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子II.对于该两厂的废水,可采取下列两种方法来处理。
(1)如果在废水中加一定量
(2)将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I、有A、B、C三种可溶性盐,阴、阳离子各不相同,其阴离子的摩尔质量按A、B、C的顺序依次增大。将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、NH4+、SO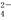 、NO
、NO 、Cl-五种离子,同时生成一种白色沉淀。请回答下列问题:
、Cl-五种离子,同时生成一种白色沉淀。请回答下列问题:
(1)经检验,三种盐中还含有下列选项中的一种离子,该离子是____________ 。
A. Na+ B.Ba2+ C.Mg2+ D. Cu2+
(2)写出C的化学式:C____________ 。
(3)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Fe3+、Cl-、NO 、NH4+四种离子且物质的量之比依次为1∶1∶3∶1(不考虑水电离的影响)。则A、B、C三种盐的物质的量之比为
、NH4+四种离子且物质的量之比依次为1∶1∶3∶1(不考虑水电离的影响)。则A、B、C三种盐的物质的量之比为____________ 。若向B溶液中通入少量SO2气体,有沉淀和无色气体产生,该沉淀为___________ 。
II、已知某KNO3溶液A中,混有少量的Ca2+和SO 等杂质,某同学设计了如下实验方案以制得纯净的KNO3固体。
等杂质,某同学设计了如下实验方案以制得纯净的KNO3固体。
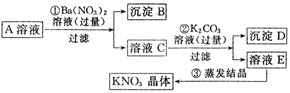
根据上述回答:
(1)沉淀D中所含有的物质是__________________ 。
(2)按上述实验方案制得的KNO3晶体,经分析测定仍含有杂质,其原因是上述第__________ 步(填① ②③)可能有误,请加以改正:___________ 。
 、NO
、NO 、Cl-五种离子,同时生成一种白色沉淀。请回答下列问题:
、Cl-五种离子,同时生成一种白色沉淀。请回答下列问题:(1)经检验,三种盐中还含有下列选项中的一种离子,该离子是
A. Na+ B.Ba2+ C.Mg2+ D. Cu2+
(2)写出C的化学式:C
(3)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Fe3+、Cl-、NO
 、NH4+四种离子且物质的量之比依次为1∶1∶3∶1(不考虑水电离的影响)。则A、B、C三种盐的物质的量之比为
、NH4+四种离子且物质的量之比依次为1∶1∶3∶1(不考虑水电离的影响)。则A、B、C三种盐的物质的量之比为II、已知某KNO3溶液A中,混有少量的Ca2+和SO
 等杂质,某同学设计了如下实验方案以制得纯净的KNO3固体。
等杂质,某同学设计了如下实验方案以制得纯净的KNO3固体。
根据上述回答:
(1)沉淀D中所含有的物质是
(2)按上述实验方案制得的KNO3晶体,经分析测定仍含有杂质,其原因是上述第
您最近一年使用:0次

 、Cu2+中的几种离子。
、Cu2+中的几种离子。

