兰尼镍(Raney-Ni)是一种带有多孔结构的细小晶粒组成的镍铝合金,常用作烯烃、炔烃等氢化反应催化剂,其高催化活性源自于镍本身的催化性质和其多孔结构对氢气的强吸附性。由镍矿渣[主要含Ni(OH)2、NiS,还含少量铁单质及其化合物和铜的化合物,及其他不溶性杂质]制备兰尼镍的过程可表示如图:

已知部分金属化合物的Ksp近似值如表所示:
回答下列问题:
(1)基态Ni原子的电子排布式为_____ 。
(2)在“酸溶”过程中,NiS发生了氧化还原反应,该反应中氧化剂和还原剂的物质的量之比为____ 。
(3)“除杂”过程中加入Ni(OH)2,可以除去Fe3+,发生该反应的离子方程式为____ 。
(4)在工业生产中常使用加入NiS的方法除去溶液中的Cu2+,若沉镍过滤后溶液中c(Ni2+)为0.10mol•L-1,则滤液中残留的c(Cu2+)为____ mol•L-1。(不考虑其他离子的相互影响)
(5)在镍、铝高温熔融时,经常通入一种气体X,通入气体的目的是____ 。
(6)在很多有机化学反应中,如烯烃、炔烃等氢化反应,有时使用新制兰尼镍进行催化加氢反应,不需要通入氢气也能发生氢化反应,原因是____ 。
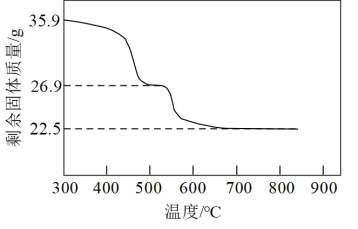
(7)“沉镍”所得沉淀有多种组成,可表示为xNiCO3•yNi(OH)2•zH2O。为测定其组成,进行下列实验:称取干燥沉淀样品35.9g,隔绝空气加热,剩余固体质量随温度变化如图所示。500~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO。则该样品的化学式为____ 。

已知部分金属化合物的Ksp近似值如表所示:
| 化学式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 | NiS | CuS |
| Ksp近似值 | 1.0×10-17 | 1.0×10-39 | 1.0×10-34 | 1.0×10-16 | 1.0×10-21 | 1.0×10-36 |
(1)基态Ni原子的电子排布式为
(2)在“酸溶”过程中,NiS发生了氧化还原反应,该反应中氧化剂和还原剂的物质的量之比为
(3)“除杂”过程中加入Ni(OH)2,可以除去Fe3+,发生该反应的离子方程式为
(4)在工业生产中常使用加入NiS的方法除去溶液中的Cu2+,若沉镍过滤后溶液中c(Ni2+)为0.10mol•L-1,则滤液中残留的c(Cu2+)为
(5)在镍、铝高温熔融时,经常通入一种气体X,通入气体的目的是
(6)在很多有机化学反应中,如烯烃、炔烃等氢化反应,有时使用新制兰尼镍进行催化加氢反应,不需要通入氢气也能发生氢化反应,原因是
(7)“沉镍”所得沉淀有多种组成,可表示为xNiCO3•yNi(OH)2•zH2O。为测定其组成,进行下列实验:称取干燥沉淀样品35.9g,隔绝空气加热,剩余固体质量随温度变化如图所示。500~750℃条件下加热,收集到的气体产物只有一种,750℃以上残留固体为NiO。则该样品的化学式为

更新时间:2022-12-03 14:52:46
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】氨基甲酸铵( )是一种易分解、易水解的白色固体,易溶于水,难溶于
)是一种易分解、易水解的白色固体,易溶于水,难溶于 ,可用做肥料、灭火剂、洗涤剂等。某研究小组模拟制备氨基甲酸铵,反应原理为:
,可用做肥料、灭火剂、洗涤剂等。某研究小组模拟制备氨基甲酸铵,反应原理为:
 。可选用下列装置制备氨基甲酸铵(
。可选用下列装置制备氨基甲酸铵( )。回答下列问题:
)。回答下列问题:
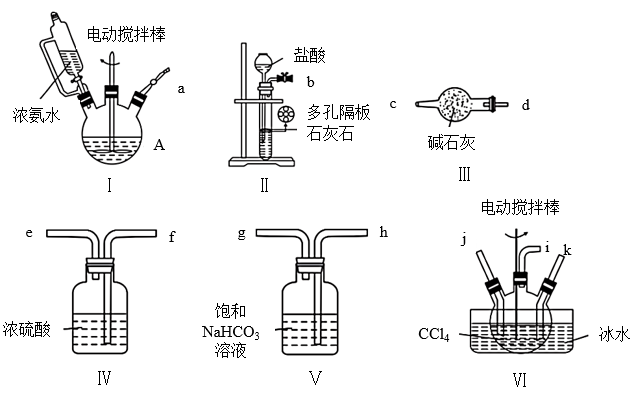
(1)仪器A的名称是___________ ,需往其中加入的固体可能是___________ (填名称)。
(2)按气流方向连接各仪器: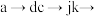
___________  。(用接口字母表示连接顺序)
。(用接口字母表示连接顺序)
(3)装置Ⅵ中,采用冰水浴的原因为___________ ;当 液体中产生较多晶体悬浮物时即停止反应,过滤得到粗产品。为了将所得粗产品干燥,可采取的方法是
液体中产生较多晶体悬浮物时即停止反应,过滤得到粗产品。为了将所得粗产品干燥,可采取的方法是___________ (填标号)。
A.蒸馏 B.高压加热烘干 C.真空微热烘干
某同学认为这套装置制得的氨基甲酸铵易变质,同时不符合绿色化学理念,改进了装置,具体做法是___________ 。
 )是一种易分解、易水解的白色固体,易溶于水,难溶于
)是一种易分解、易水解的白色固体,易溶于水,难溶于 ,可用做肥料、灭火剂、洗涤剂等。某研究小组模拟制备氨基甲酸铵,反应原理为:
,可用做肥料、灭火剂、洗涤剂等。某研究小组模拟制备氨基甲酸铵,反应原理为:
 。可选用下列装置制备氨基甲酸铵(
。可选用下列装置制备氨基甲酸铵( )。回答下列问题:
)。回答下列问题:
(1)仪器A的名称是
(2)按气流方向连接各仪器:
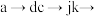
 。(用接口字母表示连接顺序)
。(用接口字母表示连接顺序)(3)装置Ⅵ中,采用冰水浴的原因为
 液体中产生较多晶体悬浮物时即停止反应,过滤得到粗产品。为了将所得粗产品干燥,可采取的方法是
液体中产生较多晶体悬浮物时即停止反应,过滤得到粗产品。为了将所得粗产品干燥,可采取的方法是A.蒸馏 B.高压加热烘干 C.真空微热烘干
某同学认为这套装置制得的氨基甲酸铵易变质,同时不符合绿色化学理念,改进了装置,具体做法是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】下图是某研究性学习小组设计的对一种废旧合金各成分(含有Cu、Fe、Si 三种成分)进行分离、回收再利用的工业流程,通过该流程将各成分转化为常用的单质及化合物。

已知:298K时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=1.9×10-13,根据上面流程回答有关问题:
(1)操作Ⅰ、Ⅱ、Ⅲ指的是________________ 。
(2)加入过量FeCl3溶液过程中与较活泼的金属反应的离子方程式:________________ 。
(3)过量的还原剂应是__________ ,溶液b中所含的金属阳离子有_____________ 。
(4)① 向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为_____________ 。
② 若用X mol/LKMnO4溶液处理溶液b,当恰好反应时消耗KMnO4溶液Y mL,则最后所得红棕色固体C的质量为_____________ g(用含X、Y的代数式表示)。
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶液,则三种金属阳离子沉淀的先后顺序为:________ >________ >________ 。(填金属阳离子)
(6)最后一步电解若用惰性电极电解一段时间后,析出固体B的质量为m g,同时测得阴阳两极收集到的气体体积相等,则标况下阳极生成的最后一种气体体积为___________ L。(用含m的代数式表示)。

已知:298K时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=1.9×10-13,根据上面流程回答有关问题:
(1)操作Ⅰ、Ⅱ、Ⅲ指的是
(2)加入过量FeCl3溶液过程中与较活泼的金属反应的离子方程式:
(3)过量的还原剂应是
(4)① 向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为
② 若用X mol/LKMnO4溶液处理溶液b,当恰好反应时消耗KMnO4溶液Y mL,则最后所得红棕色固体C的质量为
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶液,则三种金属阳离子沉淀的先后顺序为:
(6)最后一步电解若用惰性电极电解一段时间后,析出固体B的质量为m g,同时测得阴阳两极收集到的气体体积相等,则标况下阳极生成的最后一种气体体积为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
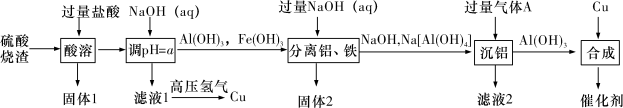
【推荐3】研究发现,Cu/Al(OH)3催化剂在工业上有着巨大作用。现以硫酸烧渣(主要成分为Fe2O3、Al2O3、CuO和SiO2等)为原料制备Cu/ Al(OH)3催化剂,流程如图所示:
已知:常温下,①几种金属离子沉淀的pH如表所示:
②电离常数 H2CO3 Ka1=4.4×10-7 Ka2=4.7×10-11
③A为无色无味气体
回答下列问题:
(1)“固体1”的用途是_______ ,“固体2”的主要成分_______ (填化学式),“分离铝、铁”的操作名称为_______ 。
(2)“酸溶”中,适当加热可提高反应速率,但是要控制温度不能太高,其原因是_______ 。
(3)a的范围为_______ , “滤液1”中通入高压氢制备铜的离子方程式为_______ 。
(4)“沉铝”的离子方程式为_______ ,“滤液2”的pH_______ 7(25℃) (填“>”“<”或“=”),判断依据是_______ 。
(5)合成催化剂 ,测定Cu与Al(OH)3的比例:将制得的“催化剂Cu/Al(OH)3”在空气中充分灼烧,固体质量不改变,则催化剂中n(Cu): n[Al(OH)3]=_______ 。

已知:常温下,①几种金属离子沉淀的pH如表所示:
| 金属离子 | Fe3+ | Al3+ | Cu2+ |
| 开始沉淀pH | 1.9 | 3.4 | 7.4 |
| 完全沉淀pH | 3.7 | 4.7 | 9.6 |
③A为无色无味气体
回答下列问题:
(1)“固体1”的用途是
(2)“酸溶”中,适当加热可提高反应速率,但是要控制温度不能太高,其原因是
(3)a的范围为
(4)“沉铝”的离子方程式为
(5)合成催化剂 ,测定Cu与Al(OH)3的比例:将制得的“催化剂Cu/Al(OH)3”在空气中充分灼烧,固体质量不改变,则催化剂中n(Cu): n[Al(OH)3]=
您最近一年使用:0次



