动手实践:在食盐中加碘是预防碘缺乏症的有效方法。通常,在食盐中加碘有两种方法:一种是加入碘化钾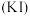 ,另一种是加入碘酸钾
,另一种是加入碘酸钾 。请设计实验方案检测某种含碘盐中加入的是碘化钾还是碘酸钾,并检测自己家中的含碘盐
。请设计实验方案检测某种含碘盐中加入的是碘化钾还是碘酸钾,并检测自己家中的含碘盐_________ 。[提示:①碘单质 遇淀粉变蓝;②维生素C是生活中可利用的还原剂;③“84”消毒液是生活中可利用的氧化剂]
遇淀粉变蓝;②维生素C是生活中可利用的还原剂;③“84”消毒液是生活中可利用的氧化剂]
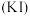 ,另一种是加入碘酸钾
,另一种是加入碘酸钾 。请设计实验方案检测某种含碘盐中加入的是碘化钾还是碘酸钾,并检测自己家中的含碘盐
。请设计实验方案检测某种含碘盐中加入的是碘化钾还是碘酸钾,并检测自己家中的含碘盐 遇淀粉变蓝;②维生素C是生活中可利用的还原剂;③“84”消毒液是生活中可利用的氧化剂]
遇淀粉变蓝;②维生素C是生活中可利用的还原剂;③“84”消毒液是生活中可利用的氧化剂]
更新时间:2022-11-25 21:06:32
|
【知识点】 氧化还原反应的应用
相似题推荐
填空题
|
较易
(0.85)
【推荐1】⑴在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中,_____ 是氧化剂;______ 元素被氧化;_______________ 是氧化产物;7mol HCl参与反应时转移的电子总数为_____ mol。
⑵反应11P+15CuSO4 +24H2O = 5Cu3P+6H3PO4 +15H2SO4中,32g CuSO4能氧化磷的质量为_________ g。
⑵反应11P+15CuSO4 +24H2O = 5Cu3P+6H3PO4 +15H2SO4中,32g CuSO4能氧化磷的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】已知将盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质。
(1)该反应中,化合价升高的反应物是_______ ,化合价没有发生变化的反应物是______ 。
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平):________ 。
(3)上述反应中,氧化剂是________ ,在反应中________ (填“得到”或“失去”)电子发生________ 反应。
(4)如果在反应后的溶液中加入NaBiO3,溶液又显紫红色。此现象说明NaBiO3具有________ 。写出该反应的离子方程式:________ 。(提示:NaBiO3为黄色或棕色粉末,不溶于冷水,在该反应中转化为Bi3+)
(1)该反应中,化合价升高的反应物是
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平):
(3)上述反应中,氧化剂是
(4)如果在反应后的溶液中加入NaBiO3,溶液又显紫红色。此现象说明NaBiO3具有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知:CuI是难溶于水的白色固体。氧化性Cu2+>I2>Cu+,还原性Cu>I->Cu+。请回答:
(1)根据物质氧化性、还原性的强弱推测,在溶液中Cu2+和I-反应离子方程式是_____________ 。
(2)久置于空气中的HI溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,反应的化学方程式为__________________________ ;欲消除HI溶液的黄色,也可向其中通入少量H2S,这是因为当浓度接近时,还原性H2S____________ (填“>”“<”或“=”)I-。
(3)CuI用于监测空气中汞蒸气:4CuI(白色)+Hg=Cu2HgI4(亮黄色)+2Cu。Cu2HgI4是___________ 。
A.氧化产物
B.还原产物
C.既是氧化产物又是还原产物
D.既不是筑化产物也不是还原产物
(4)间接碘量法用于测定溶液中Cu2+含量,即向含Cu2+的溶液中加入足量KI溶液和几滴指示剂X,再用Na2S2O3标准溶液滴定,达到滴定终点的现象是___________ (已知:I2+2S2O32-=2I-+S4O62- )。
(1)根据物质氧化性、还原性的强弱推测,在溶液中Cu2+和I-反应离子方程式是
(2)久置于空气中的HI溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,反应的化学方程式为
(3)CuI用于监测空气中汞蒸气:4CuI(白色)+Hg=Cu2HgI4(亮黄色)+2Cu。Cu2HgI4是
A.氧化产物
B.还原产物
C.既是氧化产物又是还原产物
D.既不是筑化产物也不是还原产物
(4)间接碘量法用于测定溶液中Cu2+含量,即向含Cu2+的溶液中加入足量KI溶液和几滴指示剂X,再用Na2S2O3标准溶液滴定,达到滴定终点的现象是
您最近一年使用:0次



