近年来,乳酸成为研究热点之一、乳酸可以用化学方法合成,也可以由淀粉通过发酵法制备。以乳酸(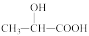 )为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中都可以最终降解为二氧化碳和水。乳酸还有许多其他用途,如它能与铁粉反应制备一种药物,反应的化学方程式为:2
)为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中都可以最终降解为二氧化碳和水。乳酸还有许多其他用途,如它能与铁粉反应制备一种药物,反应的化学方程式为:2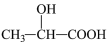 +Fe
+Fe
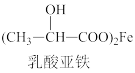 +X。
+X。
(1)乳酸降解为二氧化碳的反应的化学方程式为_______ 。
(2)乳酸与铁的反应中,X的化学式为_______ ,该反应中乳酸表现出酸性和_______ 性。
(3)试从自然界物质循环的角度解释利用乳酸合成高分子材料对环境的重要意义_______ 。
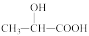 )为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中都可以最终降解为二氧化碳和水。乳酸还有许多其他用途,如它能与铁粉反应制备一种药物,反应的化学方程式为:2
)为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中都可以最终降解为二氧化碳和水。乳酸还有许多其他用途,如它能与铁粉反应制备一种药物,反应的化学方程式为:2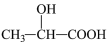 +Fe
+Fe
 +X。
+X。(1)乳酸降解为二氧化碳的反应的化学方程式为
(2)乳酸与铁的反应中,X的化学式为
(3)试从自然界物质循环的角度解释利用乳酸合成高分子材料对环境的重要意义
更新时间:2022-11-26 16:19:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: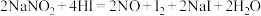 。
。
(1)反应中___________ 元素被还原(填元素名称),___________ 是还原剂(填化学式);
(2)若误食 ,则导致血红蛋白中的
,则导致血红蛋白中的 转化为
转化为 而中毒,可以服用维生素C解毒,维生素C在解毒的过程中表现出
而中毒,可以服用维生素C解毒,维生素C在解毒的过程中表现出___________ (填“还原性”“氧化性”或“既有氧化性又有还原性”)。
(3)根据上述反应,鉴别 和NaCl。可选用的物质有:①水②碘化钾③淀粉溶液④白酒⑤食醋,你认为必须选用的物质有
和NaCl。可选用的物质有:①水②碘化钾③淀粉溶液④白酒⑤食醋,你认为必须选用的物质有___________ (填序号)。
(4)若有0.5mol的还原剂被氧化,则该过程中转移的电子数为___________ 。
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: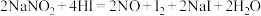 。
。(1)反应中
(2)若误食
 ,则导致血红蛋白中的
,则导致血红蛋白中的 转化为
转化为 而中毒,可以服用维生素C解毒,维生素C在解毒的过程中表现出
而中毒,可以服用维生素C解毒,维生素C在解毒的过程中表现出(3)根据上述反应,鉴别
 和NaCl。可选用的物质有:①水②碘化钾③淀粉溶液④白酒⑤食醋,你认为必须选用的物质有
和NaCl。可选用的物质有:①水②碘化钾③淀粉溶液④白酒⑤食醋,你认为必须选用的物质有(4)若有0.5mol的还原剂被氧化,则该过程中转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
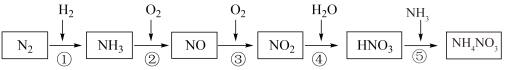
【推荐2】氮元素及其化合物的转化关系如图所示:_____ ,属于氮的固定的是______ (填序号)。
(2)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示:_______ 。
②写出催化转化过程中,生成 的化学方程式
的化学方程式_______ 。
(3) 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是_______ (写出操作步骤、现象和结论) 。
(4)工业制硝酸时尾气中含有 、
、 ,可用以下方法吸收:
,可用以下方法吸收:
① 溶液吸收法。发生的反应有:
溶液吸收法。发生的反应有: ,
,
②用不同浓度的 溶液吸收
溶液吸收 含量不同的尾气,关系如下图:
含量不同的尾气,关系如下图: 、
、 中
中 的含量)
的含量)
i.根据上图得知_______ (填字母)。
a. 溶液浓度越大,氮氧化物的吸收率越大
溶液浓度越大,氮氧化物的吸收率越大
b. 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大
ii.当 小于50%时,加入
小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是_______ 。
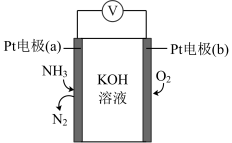
(5)电化学气敏传感器可用于监测环境中氨气的含量,其工作原理示意图如下:_______ 。
②反应消耗的 与
与 的物质的量之比为
的物质的量之比为_______ 。
(2)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示:

②写出催化转化过程中,生成
 的化学方程式
的化学方程式(3)
 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是(4)工业制硝酸时尾气中含有
 、
、 ,可用以下方法吸收:
,可用以下方法吸收:①
 溶液吸收法。发生的反应有:
溶液吸收法。发生的反应有: ,
,
②用不同浓度的
 溶液吸收
溶液吸收 含量不同的尾气,关系如下图:
含量不同的尾气,关系如下图: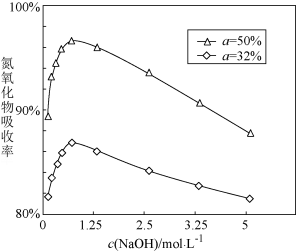
 、
、 中
中 的含量)
的含量)i.根据上图得知
a.
 溶液浓度越大,氮氧化物的吸收率越大
溶液浓度越大,氮氧化物的吸收率越大b.
 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大ii.当
 小于50%时,加入
小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是(5)电化学气敏传感器可用于监测环境中氨气的含量,其工作原理示意图如下:
②反应消耗的
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】M是一种无毒的聚酯纤维,可用作毛级玩真的内充物。工业上常以有机物A和乙二醇为原料在一定条件下合成高分子化合物M。有机物A的结构、性质如下:
①16.6gA完全燃烧,可产生0.8molCO2和0.3molH2O。
②A的相对分子质量在100-200之间,分子中含有一个苯环,苯环上有两个互为对位的取代基。
③1molA可与足量NaHCO3溶液反应,放出2molCO2气体。
请回答:
(1)A的结构简式是_______ 。
(2)等质量的钠分别与足量的A和乙二醇反应生成气体的体积比为_______ 。
(3)合成M的反应的化学方程式和反应类型是_______ ;_______ 反应。
(4)A有多种同分异构体,其中既能与NaHCO3溶液反应放出CO2气体,又能发生银镜反应和水解反应,且分子内含有苯环,请写出一种符合要求的物质的结构简式_______ 。
①16.6gA完全燃烧,可产生0.8molCO2和0.3molH2O。
②A的相对分子质量在100-200之间,分子中含有一个苯环,苯环上有两个互为对位的取代基。
③1molA可与足量NaHCO3溶液反应,放出2molCO2气体。
请回答:
(1)A的结构简式是
(2)等质量的钠分别与足量的A和乙二醇反应生成气体的体积比为
(3)合成M的反应的化学方程式和反应类型是
(4)A有多种同分异构体,其中既能与NaHCO3溶液反应放出CO2气体,又能发生银镜反应和水解反应,且分子内含有苯环,请写出一种符合要求的物质的结构简式
您最近一年使用:0次
【推荐2】合理使用药物是保证身心健康、提高生活质量的有效手段。药物化学已经成为化学的一个重要领域。
(1)我国科学家屠呦呦因发现治疗疟疾的特效药——青蒿素,而获得2015年诺贝尔生理学或医学奖。青蒿素的结构简式如右图所示,其含有的过氧基(—O—O—)具有强氧化性。

请回答下列问题:
①青蒿素的分子式为_______________________ 。
②下列有关青蒿素的叙述中,正确的是__________ (填字母)。
A、青蒿素属于芳香族化合物
B、青蒿素具有强氧化性,可用于杀菌
C、青蒿素分子中的所有碳原子在同一个平面上
D、在一定条件下,青蒿素能与NaOH溶液发生反应
(2)阿司匹林(乙酰水杨酸)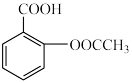 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:

请回答下列问题:
①乙酰水杨酸中的含氧官能园的名称为____________________ 。
②制得的阿司匹林中常含有少量的杂质水杨酸,下列试剂可用于检验阿司匹林样品中是否混有水杨酸的是________________ (填字母)。
A、碳酸氢钠溶液 B、三氯化铁溶液 C、石蕊试液
③写出水杨酸与足量的NaHCO3溶液完全反应所得有机产物的结构简式:_____________ 。
④1 mol乙酰水杨酸与足量的NaOH溶液反应,最多消耗NaOH物质的量为_________ mol。
(1)我国科学家屠呦呦因发现治疗疟疾的特效药——青蒿素,而获得2015年诺贝尔生理学或医学奖。青蒿素的结构简式如右图所示,其含有的过氧基(—O—O—)具有强氧化性。

请回答下列问题:
①青蒿素的分子式为
②下列有关青蒿素的叙述中,正确的是
A、青蒿素属于芳香族化合物
B、青蒿素具有强氧化性,可用于杀菌
C、青蒿素分子中的所有碳原子在同一个平面上
D、在一定条件下,青蒿素能与NaOH溶液发生反应
(2)阿司匹林(乙酰水杨酸)
 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:
请回答下列问题:
①乙酰水杨酸中的含氧官能园的名称为
②制得的阿司匹林中常含有少量的杂质水杨酸,下列试剂可用于检验阿司匹林样品中是否混有水杨酸的是
A、碳酸氢钠溶液 B、三氯化铁溶液 C、石蕊试液
③写出水杨酸与足量的NaHCO3溶液完全反应所得有机产物的结构简式:
④1 mol乙酰水杨酸与足量的NaOH溶液反应,最多消耗NaOH物质的量为
您最近一年使用:0次
【推荐3】成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成份的存在,请你参与并协助他们完成相关实验.
(1)用小试管取少量的苹果汁,加入新制Cu(OH)2悬浊液,并加热,产生砖红色的沉淀,则苹果中含有_______________ (写结构简式)。
(2)葡萄糖在一定条件下可以得到化学式为C2H6O的化合物A。A+CH3COOH→有香味的产物,含A的体积分数为75%的水溶液可以用做_______________ 。
(3)苹果中含有苹果酸,测得其相对分子质量为134,取0.02mol苹果酸,使其完全燃烧,将燃烧后的产物先后通过足量的无水CaCl2和碱石灰,两者分别增重1.08g 和 3.52g。则分子中C、H原子的个数比_______________ ,苹果酸的分子式是_______________ 。
(4)若苹果酸具有如下性质:①1mol苹果酸与足量金属钠反应产生1.5mol气体;②在有浓硫酸和加热条件下,苹果酸与醇或羧酸均反应生成有香味的产物;③苹果酸在一定条件下的分子内脱水产物可和溴水发生加成反应。④1mol苹果酸能与2mol碳酸氢钠反应。根据上述信息,推测苹果酸可能的一种结构简式是_____________ 。
(1)用小试管取少量的苹果汁,加入新制Cu(OH)2悬浊液,并加热,产生砖红色的沉淀,则苹果中含有
(2)葡萄糖在一定条件下可以得到化学式为C2H6O的化合物A。A+CH3COOH→有香味的产物,含A的体积分数为75%的水溶液可以用做
(3)苹果中含有苹果酸,测得其相对分子质量为134,取0.02mol苹果酸,使其完全燃烧,将燃烧后的产物先后通过足量的无水CaCl2和碱石灰,两者分别增重1.08g 和 3.52g。则分子中C、H原子的个数比
(4)若苹果酸具有如下性质:①1mol苹果酸与足量金属钠反应产生1.5mol气体;②在有浓硫酸和加热条件下,苹果酸与醇或羧酸均反应生成有香味的产物;③苹果酸在一定条件下的分子内脱水产物可和溴水发生加成反应。④1mol苹果酸能与2mol碳酸氢钠反应。根据上述信息,推测苹果酸可能的一种结构简式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
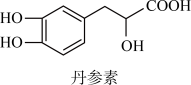
【推荐1】丹参素能明显抑制血小板的聚集,其结构如图所示。_______ 。
(2)丹参素在一定条件下能与 反应生成酯,该反应的类型属于
反应生成酯,该反应的类型属于_______ 反应。
(3)丹参素中含氧官能团有_______ (填名称)。
(4)向丹参素溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丹参素溶液具有_______ 性。
(5)向稀的酸性 溶液中滴入几滴丹参素溶液,观察到的现象为
溶液中滴入几滴丹参素溶液,观察到的现象为_______ ,说明丹参素具有_______ 性(填“氧化”或“还原”)
(6)根据丹参素结构,预测1mol丹参素和足量的氢氧化钠溶液反应时,最多能够消耗_______ mol ;
; 在一定条件下被氧化的生成物,其分子式为
在一定条件下被氧化的生成物,其分子式为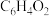 该分子有一个六元碳环,且4个氢原子的化学环境相同,该物质的键线式
该分子有一个六元碳环,且4个氢原子的化学环境相同,该物质的键线式_______ 。
①在表示有机化合物的组成和结构时,如果将碳、氢元素符号省略,只表示分子中的键的连接情况和官能团,每个拐点或终点均表示有一个碳原子,则得到键线式。如丙烯可表示为 ,乙醇可表示为
,乙醇可表示为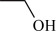 。
。
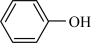
③苯酚(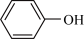 )是最简单的酚,酚羟基在水中可微弱电离,产生
)是最简单的酚,酚羟基在水中可微弱电离,产生 。
。
(2)丹参素在一定条件下能与
 反应生成酯,该反应的类型属于
反应生成酯,该反应的类型属于(3)丹参素中含氧官能团有
(4)向丹参素溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丹参素溶液具有
(5)向稀的酸性
 溶液中滴入几滴丹参素溶液,观察到的现象为
溶液中滴入几滴丹参素溶液,观察到的现象为(6)根据丹参素结构,预测1mol丹参素和足量的氢氧化钠溶液反应时,最多能够消耗
 ;
; 在一定条件下被氧化的生成物,其分子式为
在一定条件下被氧化的生成物,其分子式为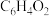 该分子有一个六元碳环,且4个氢原子的化学环境相同,该物质的键线式
该分子有一个六元碳环,且4个氢原子的化学环境相同,该物质的键线式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】丙烯是石油化工的重要原料,一定条件下可发生下列转化:
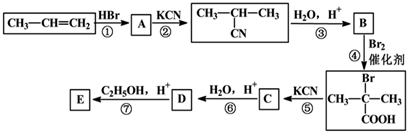
已知: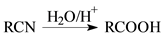
(1)A的结构简式为:____________ ;
(2)反应④的类型为:_________________ 反应;反应⑦进行所需的条件是:_________ 。
(3)D与足量乙醇反应生成E的化学方程式为:__________________ 。
(4)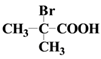 与足量NaOH溶液反应的化学方程式为
与足量NaOH溶液反应的化学方程式为_________________ 。
(5)B的同分异构体有多种.写出其中一种既能发生银镜反应,又能发生酯化反应,并且核磁共振氢谱峰值为6:1:1的同分异构体的结构简式:_____________________ 。
(6)请写出以丙烯为原料制备聚2-羟基丙酸的合成路线,无机试剂任选。______________
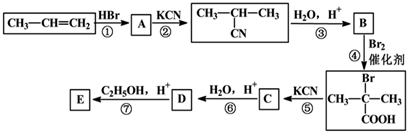
已知:
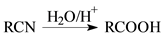
(1)A的结构简式为:
(2)反应④的类型为:
(3)D与足量乙醇反应生成E的化学方程式为:
(4)
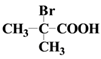 与足量NaOH溶液反应的化学方程式为
与足量NaOH溶液反应的化学方程式为(5)B的同分异构体有多种.写出其中一种既能发生银镜反应,又能发生酯化反应,并且核磁共振氢谱峰值为6:1:1的同分异构体的结构简式:
(6)请写出以丙烯为原料制备聚2-羟基丙酸的合成路线,无机试剂任选。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硅橡胶具有无毒、无味、耐高温和低温的特性,可制成密封材料、人造血管等。它是由二甲基二氯硅烷 水解得到二甲基硅二醇,经脱水缩聚生成聚硅氧烷,再经交联制成的。请写出二甲基二氯硅烷水解及水解产物生成线型缩聚物的化学方程式
水解得到二甲基硅二醇,经脱水缩聚生成聚硅氧烷,再经交联制成的。请写出二甲基二氯硅烷水解及水解产物生成线型缩聚物的化学方程式___________ 。
 水解得到二甲基硅二醇,经脱水缩聚生成聚硅氧烷,再经交联制成的。请写出二甲基二氯硅烷水解及水解产物生成线型缩聚物的化学方程式
水解得到二甲基硅二醇,经脱水缩聚生成聚硅氧烷,再经交联制成的。请写出二甲基二氯硅烷水解及水解产物生成线型缩聚物的化学方程式
您最近一年使用:0次