卤素性质的递变规律及原因
从F→I,电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐_______ ,原子得电子能力逐渐_______ ,非金属性逐渐_______ 。
从F→I,电子层数逐渐增多,原子半径逐渐增大,原子核对最外层电子的引力逐渐
22-23高一上·全国·课时练习 查看更多[1]
(已下线)物质结构 元素周期表——整体认识
更新时间:2022-12-07 16:44:33
|
【知识点】 同主族元素性质递变规律
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】下图是中学教材中元素周期表的一部分,其中标出A~Q14种元素,试回答下列问题:
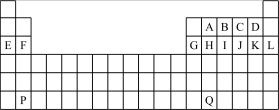
(1)在上表所列出的短周期元素中
①性质最不活泼的是____________ ;②原子半径最大的是(除稀有气体元素)__________ 。
③形成的气态氢化物最稳定的是______________________________ ;
④最高价氧化物对应的水化物中酸性最强的是____________ 碱性最强的是_____________ 。
⑤形成的阴离子还原性最弱的是_____________ ,阳离子半径最小的是_____________ 。
(2)①B的气态氢化物与最高价氧化物对应的水化物发生反应的化学方程式为________________ ;
②A单质与J的最高价氧化物对应的水化物反应的方程式________________________________ 。
(3)设P的原子序数为Z,则F的原子序数为______________ ,Q的原子序数为________________ 。

(1)在上表所列出的短周期元素中
①性质最不活泼的是
③形成的气态氢化物最稳定的是
④最高价氧化物对应的水化物中酸性最强的是
⑤形成的阴离子还原性最弱的是
(2)①B的气态氢化物与最高价氧化物对应的水化物发生反应的化学方程式为
②A单质与J的最高价氧化物对应的水化物反应的方程式
(3)设P的原子序数为Z,则F的原子序数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】根据所学知识,回答下列问题:
(1)元素周期表1~20号元素中,金属性最强的元素是__________ (填元素符号,下同);属于稀有气体的是________________ ;非金属性最强的元素在周期表中的位置是_______________________ 。
(2)已知NO2和N2O4之间发生可逆反应:2NO2 (g) (红棕色) N2O4(g) (无色)。将装有NO2 和N2O4混合气体的烧瓶浸入热水中,观察到的现象是
N2O4(g) (无色)。将装有NO2 和N2O4混合气体的烧瓶浸入热水中,观察到的现象是____________________ ,产生该现象的原因是____________________________________ 。
(3)一定条件下,向2L恒容密闭容器中按体积比1:3充入4.48L(标准状况)N2和H2的混合气体,发生反应N2(g)+3H2(g) 2NH3(g),3min时反应达到平衡状态,测得c(N2)=0.02mol·L-1。
2NH3(g),3min时反应达到平衡状态,测得c(N2)=0.02mol·L-1。
① 0~3min内,v (NH3)=___________________ 。
②下列叙述可证明上述反应达到平衡状态的是_________ (填序号)。
a. v(H2)= 3 v(N2) b.容器内压强保持不变
c.每消耗1mol N2,同时生成2mol NH3
d. N2、H2和NH3的物质的量浓度不再变化
(1)元素周期表1~20号元素中,金属性最强的元素是
(2)已知NO2和N2O4之间发生可逆反应:2NO2 (g) (红棕色)
 N2O4(g) (无色)。将装有NO2 和N2O4混合气体的烧瓶浸入热水中,观察到的现象是
N2O4(g) (无色)。将装有NO2 和N2O4混合气体的烧瓶浸入热水中,观察到的现象是(3)一定条件下,向2L恒容密闭容器中按体积比1:3充入4.48L(标准状况)N2和H2的混合气体,发生反应N2(g)+3H2(g)
 2NH3(g),3min时反应达到平衡状态,测得c(N2)=0.02mol·L-1。
2NH3(g),3min时反应达到平衡状态,测得c(N2)=0.02mol·L-1。① 0~3min内,v (NH3)=
②下列叙述可证明上述反应达到平衡状态的是
a. v(H2)= 3 v(N2) b.容器内压强保持不变
c.每消耗1mol N2,同时生成2mol NH3
d. N2、H2和NH3的物质的量浓度不再变化
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。表中列出了①~⑨九种元素在周期表中的位置。
请回答:
(1)这九种元素中化学性质最不活泼的是___ (填元素符号)。
(2)写出④元素单质的一种用途____ 。
(3)写出⑧元素最高价氧化物对应水化物的化学式:___ 。
(4)写出⑤元素氢化物的化学式:___ 。
(5)在①②③三种元素的最高价氧化物对应的水化物中,碱性最强的是___ (填化学式)。
(6)④③⑥三种元素按原子半径由大到小的顺序依次为____ (填元素符号)。
(7)写出③的氧化物与氢氧化钠反应的离子方程式:___ 。
(8)⑦元素与氢元素形成化合物的电子式是____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ② | ③ | ④ | ⑧ | ⑨ | |||
| 4 | ① |
(1)这九种元素中化学性质最不活泼的是
(2)写出④元素单质的一种用途
(3)写出⑧元素最高价氧化物对应水化物的化学式:
(4)写出⑤元素氢化物的化学式:
(5)在①②③三种元素的最高价氧化物对应的水化物中,碱性最强的是
(6)④③⑥三种元素按原子半径由大到小的顺序依次为
(7)写出③的氧化物与氢氧化钠反应的离子方程式:
(8)⑦元素与氢元素形成化合物的电子式是
您最近一年使用:0次



