化学工作者对反应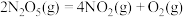 提出下列三步机理(
提出下列三步机理(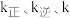 为速率常数):
为速率常数):
第一步: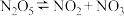 快速平衡,且平衡时有:
快速平衡,且平衡时有: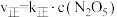
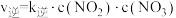 ;
;
第二步: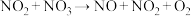 慢反应,
慢反应,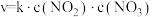 ;
;
第三步: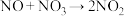 快反应。
快反应。
下列说法中错误的是
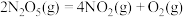 提出下列三步机理(
提出下列三步机理(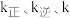 为速率常数):
为速率常数):第一步:
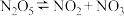 快速平衡,且平衡时有:
快速平衡,且平衡时有: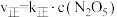
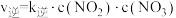 ;
;第二步:
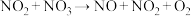 慢反应,
慢反应,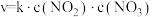 ;
;第三步:
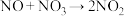 快反应。
快反应。下列说法中错误的是
A.第一步反应的平衡常数 |
| B.第二步反应速率决定总反应的快慢 |
C.第三步中NO与 的碰撞仅部分发生反应 的碰撞仅部分发生反应 |
D.速率常数: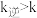 |
21-22高三下·湖南娄底·期中 查看更多[2]
更新时间:2022-08-22 11:03:39
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】在某催化剂的作用下,乙烷催化氧化生成乙醛的反应路径如图所示。下列说法错误的是


| A.该反应为放热反应 |
B.该历程中最大能垒为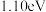 |
C.该反应的活化能 |
| D.在该催化剂上乙烷催化氧化生成乙醛的历程分四步 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】某反应过程能量变化如图所示,下列说法不正确的是( )
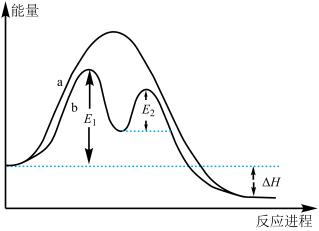

| A.反应过程b有催化剂参与 |
| B.该反应为放热反应,反应热为△H |
| C.加入催化剂,可改变该反应的活化能 |
| D.有催化剂的条件下,反应的活化能等于E1+E2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】少量铁粉与10mL 0.1mol·L-1的稀盐酸反应反应速率太慢。为了加快此反应速率而不改变H2的产量可以使用如下方法中的
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加 CHCOONa固体 ⑤加NaCl溶液⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发)⑧改用10mL 1mol·L-1盐酸
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加 CHCOONa固体 ⑤加NaCl溶液⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发)⑧改用10mL 1mol·L-1盐酸
| A.①⑥⑦ | B.③⑤⑧ | C.③⑦⑧ | D.⑤⑦⑧ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】实验室用锌粒与2 mol/L盐酸制取氢气,下列措施不能增大化学反应速率的是
| A.用锌粉代替锌粒 | B.改用18.4 mol/L硫酸溶液 |
| C.改用热的2 mol/L盐酸溶液 | D.改用2 mol/L硫酸溶液 |
您最近一年使用:0次

 Y+Z是一吸热的可逆基元反应,其正反应的活化能为Ea,逆反应的活化能为Eb,则下列活化能大小关系表述正确的是
Y+Z是一吸热的可逆基元反应,其正反应的活化能为Ea,逆反应的活化能为Eb,则下列活化能大小关系表述正确的是


