氮及氮的化合物有着重要的用途。
(1)氮元素在周期表中的位置是_______ ;NH3的电子式是_______ 。
(2)将空气中游离态的氮转化为含氮化合物的过程叫氮的固定,请举例说明一种自然界中氮的固定的途径_______ (用化学方程式表示)。
(3)工业合成氨是人工固氮的重要方法。2007年化学家格哈德•埃特尔证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下图:
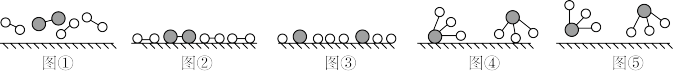
下列说法正确的是_______ (选填字母)。
a图①表示N2、H2分子中均是单键
b 图②→图③需要吸收能量
c 该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
(4)水合肼(N2H4•H2O)为无色透明的油状发烟液体,是一种重要的精细化工原料,通常在催化剂存在下,用次氯酸钠与氨反应可制备,该反应的化学方程式是_______ 。
(1)氮元素在周期表中的位置是
(2)将空气中游离态的氮转化为含氮化合物的过程叫氮的固定,请举例说明一种自然界中氮的固定的途径
(3)工业合成氨是人工固氮的重要方法。2007年化学家格哈德•埃特尔证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下图:

下列说法正确的是
a图①表示N2、H2分子中均是单键
b 图②→图③需要吸收能量
c 该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
(4)水合肼(N2H4•H2O)为无色透明的油状发烟液体,是一种重要的精细化工原料,通常在催化剂存在下,用次氯酸钠与氨反应可制备,该反应的化学方程式是
更新时间:2022/10/23 17:11:11
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】写出下列物质的结构式
①CH4_____________ ② NH3__________ ③ Cl2_____________
①CH4
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】烟道气中含有 ,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质量为184)。
,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质量为184)。

(1)写出 的电子式
的电子式___________ ;
(2)下列叙述正确的是___________ ;
A.烟道气中的 含量可用一定体积、浓度的酸性高锰酸钾溶液测定
含量可用一定体积、浓度的酸性高锰酸钾溶液测定
B. 是橡胶硫化剂,橡胶硫化程度越高,弹性越好
是橡胶硫化剂,橡胶硫化程度越高,弹性越好
C. 可与
可与 发生反应,能作为
发生反应,能作为 的脱水剂
的脱水剂
D. 固体中含阳离子
固体中含阳离子 和阴离子
和阴离子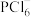 ,
, 空间构型为正四面体
空间构型为正四面体
E. 易溶于
易溶于 ,则
,则 为非极性分子
为非极性分子
(3) 与过量
与过量 反应的化学方程式
反应的化学方程式___________ ;
(4) 与
与 反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为
反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为___________ ;
(5)设计实验检验 与足量NaOH溶液反应生成的阴离子
与足量NaOH溶液反应生成的阴离子___________ 。
 ,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质量为184)。
,通过一系列变化可得重要的无机化合物M(仅含两种元素,相对分子质量为184)。
(1)写出
 的电子式
的电子式(2)下列叙述正确的是
A.烟道气中的
 含量可用一定体积、浓度的酸性高锰酸钾溶液测定
含量可用一定体积、浓度的酸性高锰酸钾溶液测定B.
 是橡胶硫化剂,橡胶硫化程度越高,弹性越好
是橡胶硫化剂,橡胶硫化程度越高,弹性越好C.
 可与
可与 发生反应,能作为
发生反应,能作为 的脱水剂
的脱水剂D.
 固体中含阳离子
固体中含阳离子 和阴离子
和阴离子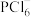 ,
, 空间构型为正四面体
空间构型为正四面体E.
 易溶于
易溶于 ,则
,则 为非极性分子
为非极性分子(3)
 与过量
与过量 反应的化学方程式
反应的化学方程式(4)
 与
与 反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为
反应除生成M外,同时有淡黄色固体和一种盐。则M的分子式为(5)设计实验检验
 与足量NaOH溶液反应生成的阴离子
与足量NaOH溶液反应生成的阴离子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2015年8月12日天津港的爆炸事故中,有700 t氰化钠放在现场。NaCN为白色结晶颗粒(或粉末),熔点为563.7℃,沸点为1496℃,易溶于水,易水解,有剧毒。
回答下列问题:
(1)含NaCN的废液______________ (填“能”或“不能”)直接排放。
(2)常温下,氰化钠能与双氧水反应,生成小苏打和某种碱性气体,大大降低其毒性,写出其反应的化学方程式:___________________ 。该反应中氧化剂的电子式为________________ 。
(3)常见合成氰化钠的反应有以下三步:
①2Na+2M =2NaNH2+H2
②2NaNH2+C=Q+2H2↑
③Q+C=2NaCN
反应中M、Q两物质的化学式分别为_______ 、________ ,在反应②中,若生成1mol H2,则转移的电子数是_______ 。
回答下列问题:
(1)含NaCN的废液
(2)常温下,氰化钠能与双氧水反应,生成小苏打和某种碱性气体,大大降低其毒性,写出其反应的化学方程式:
(3)常见合成氰化钠的反应有以下三步:
①2Na+2M =2NaNH2+H2
②2NaNH2+C=Q+2H2↑
③Q+C=2NaCN
反应中M、Q两物质的化学式分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)用 和
和 组合形成的质子交换膜燃料电池的结构如图。
组合形成的质子交换膜燃料电池的结构如图。
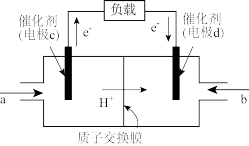
则电极d是_______ (填“正极”或“负极”),电极d的电极反应式为_______ ;
(2)在恒定温度下,向容积恒定的密闭容器中充入一定量的氨基甲酸铵,发生反应: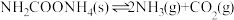 ,下列
,下列不能 判断该反应已达到化学平衡的是_______。
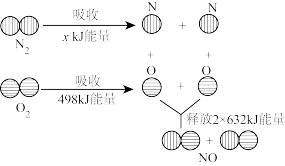
(3)已知 )和
)和 反应生成
反应生成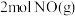 吸收
吸收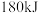 能量,反应过程中能量变化如图所示。断裂
能量,反应过程中能量变化如图所示。断裂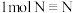 吸收的能量值x为
吸收的能量值x为_______  。
。
(1)用
 和
和 组合形成的质子交换膜燃料电池的结构如图。
组合形成的质子交换膜燃料电池的结构如图。
则电极d是
(2)在恒定温度下,向容积恒定的密闭容器中充入一定量的氨基甲酸铵,发生反应:
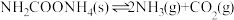 ,下列
,下列A.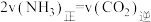 | B.容器中总压强不变 |
| C.密闭容器中混合气体的密度不变 | D.密闭容器中氨气的体积分数不变 |
 )和
)和 反应生成
反应生成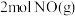 吸收
吸收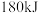 能量,反应过程中能量变化如图所示。断裂
能量,反应过程中能量变化如图所示。断裂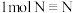 吸收的能量值x为
吸收的能量值x为 。
。
您最近一年使用:0次
【推荐2】完成下列小题
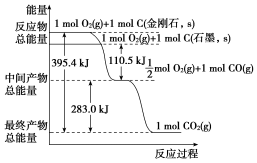
(1)金刚石和石墨在燃烧时,若氧气不足生成一氧化碳,若氧气充足生成二氧化碳,反应中放出的热量如图所示。______ (填“金刚石”或“石墨”)放出的热量更多,在通常状况下,______ (填“金刚石”或“石墨”)更稳定,1mol石墨完全转化为金刚石的反应______ (填“吸收”或“释放”)______ kJ热量,断开1mol石墨中的化学键所吸收的能量______ (填“大于”或“小于”)断开1mol金刚石中的化学键所吸收的能量。
(2)将V1mL1.0mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50)。______ (填“吸收”或“释放”)能量,通过上图分析可以得出,做该实验时,环境温度______ (填“高于”“低于”或“等于”)22℃。
②根据上图可以得出,该NaOH溶液的浓度约是______ 。
(1)金刚石和石墨在燃烧时,若氧气不足生成一氧化碳,若氧气充足生成二氧化碳,反应中放出的热量如图所示。
(2)将V1mL1.0mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50)。
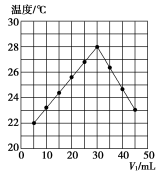
②根据上图可以得出,该NaOH溶液的浓度约是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)下列变化:①碘的升华;②氧气溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解。(填序号 )
化学键没有被破坏的是________ ;仅发生离子键破坏的是_______ ; 仅发生共价键破坏的是________ ;既发生离子键又发生共价键破坏的是_______ 。
(2)已知1mol Si中含1mol Si—Si键。
请回答下列问题:
①已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列物质的熔点高低(填“>”或“<”):SiC________ Si。
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),则2 mol H2生成高纯硅需
Si(s)+4HCl(g),则2 mol H2生成高纯硅需________ (填“吸收”或“放出”)能量________ kJ。
化学键没有被破坏的是
(2)已知1mol Si中含1mol Si—Si键。
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/ kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
①已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列物质的熔点高低(填“>”或“<”):SiC
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
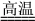 Si(s)+4HCl(g),则2 mol H2生成高纯硅需
Si(s)+4HCl(g),则2 mol H2生成高纯硅需
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我国的食品添加剂有多种,如富硒(Se)酵母、二氧化硅、硫黄等,新品种食品添加剂的安全性需通过审查和测试,食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂等,用于食品生产中能更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为___________ ;普通玻璃的主要成分为二氧化硅,用氢氟酸蚀刻普通玻璃时,发生反应的化学方程式为___________ 。
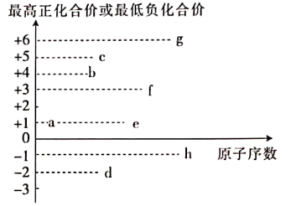
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。
①由a、c、d三种元素形成的离子化合物的化学式为___________ 。
②图中所示元素中金属性最强的是___________ (填元素符号),工业上得到该元素的单质的原理为___________ (填化学方程式)。
③e、f、g元素的简单离子半径由大到小的顺序为___________ (用离子符号回答)。
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为___________ (填化学式)。
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为___________ 。
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。

①由a、c、d三种元素形成的离子化合物的化学式为
②图中所示元素中金属性最强的是
③e、f、g元素的简单离子半径由大到小的顺序为
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
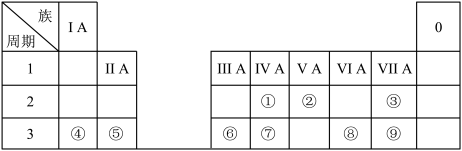
【推荐2】根据表中9种元素及由这些元素形成的单质和化合物,完成下列问题:_____ 。
(2)①②③非金属性最强的是_____ (填元素符号)。
(3)④的单质与水反应的离子方程式为_____ 。
(4)③和④的简单离子半径大小:③_____ (填“ ”或“
”或“ ”)④。
”)④。
(2)①②③非金属性最强的是
(3)④的单质与水反应的离子方程式为
(4)③和④的简单离子半径大小:③
 ”或“
”或“ ”)④。
”)④。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分, 表中列出10种元素在周期表中的位置,按要求回答下列各题。
(1)写出下列序号所代表的元素符号③_____ ;⑩______
(2)写出⑥的一种用途_________________ ;常温下可与表中_______ 单质反应(填化学式)
(3)元素④的原子结构示意图为________________________ ;
(4)⑤和⑨形成的化合物的化学式为:_____________ ;向该化合物的水溶液里逐滴滴入苛性钠溶液,现象为__________________________________________________ .
(5)②⑤⑦⑧的原子半径由大到小的顺序是__________________________ (用元素符号表示)
(6)将①⑤同时投入到水中,发生反应的化学方程式有:______________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑧ | ⑩ | ||||||
| 3 | ① | ③ | ⑤ | ⑥ | ⑦ | ⑨ | ||
| 4 | ② | ④ |
(1)写出下列序号所代表的元素符号③
(2)写出⑥的一种用途
(3)元素④的原子结构示意图为
(4)⑤和⑨形成的化合物的化学式为:
(5)②⑤⑦⑧的原子半径由大到小的顺序是
(6)将①⑤同时投入到水中,发生反应的化学方程式有:
您最近一年使用:0次



