根据所学知识填写下列空白:
(1)现有下列十种物质:①HCl气体②Cu③C2H5OH④CO2⑤CuSO4•5H2O⑥NaHCO3⑦Ba(OH)2溶液⑧熔融Na2SO4⑨液氨⑩空气。
所给物质能导电的是_______ ;属于强电解质的是_______ ;属于非电解质的是_______ (填所给物质的序号)。
(2)如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。
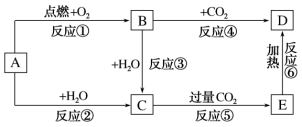
请填写下列空白:
①写出反应②的实验现象:_______ 。
②以上反应中属于氧化还原反应的有_______ (填编号)。
③反应②的离子反应方程式为_______ ;反应④的化学方程式为_______ ;向D中滴入少量盐酸的离子方程式为_______ 。
(1)现有下列十种物质:①HCl气体②Cu③C2H5OH④CO2⑤CuSO4•5H2O⑥NaHCO3⑦Ba(OH)2溶液⑧熔融Na2SO4⑨液氨⑩空气。
所给物质能导电的是
(2)如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。

请填写下列空白:
①写出反应②的实验现象:
②以上反应中属于氧化还原反应的有
③反应②的离子反应方程式为
更新时间:2022-10-31 17:07:03
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】
(1)下面所列物质中,属于强电解质的是________ (填序号,下同),属于弱电解质的是________ ,属于非电解质的是________ 。
①硝酸钠 ②葡萄糖 ③醋酸 ④二氧化碳 ⑤乙醇 ⑥硫化氢 ⑦硫酸氢钾 ⑧一水合氨 ⑨氯气 ⑩硫酸钡 ⑪铜
(2)在新制氯水中加入少量的KCl固体,水的电离平衡________ 移动(填“向右”、“向左”、或“不”)。
(3)已知室温下,H2CO3的电离常数为Ka1=4.4×10-7;Ka2=4.7×10-11,HClO次氯酸的电离平衡常数为Ka=3.0×10-8。向0.2mol/LNa2CO3溶液中加入HClO,离子方程式为___________ ,_____ (填“能”或“不能”)观察到气泡逸出。
(4)某二元酸H2A溶液中检测出含有H+、HA-、A2-三种溶质粒子,则H2A电离方程式为_________ 。
(1)下面所列物质中,属于强电解质的是
①硝酸钠 ②葡萄糖 ③醋酸 ④二氧化碳 ⑤乙醇 ⑥硫化氢 ⑦硫酸氢钾 ⑧一水合氨 ⑨氯气 ⑩硫酸钡 ⑪铜
(2)在新制氯水中加入少量的KCl固体,水的电离平衡
(3)已知室温下,H2CO3的电离常数为Ka1=4.4×10-7;Ka2=4.7×10-11,HClO次氯酸的电离平衡常数为Ka=3.0×10-8。向0.2mol/LNa2CO3溶液中加入HClO,离子方程式为
(4)某二元酸H2A溶液中检测出含有H+、HA-、A2-三种溶质粒子,则H2A电离方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.现有以下物质:①石墨;②乙醇;③氨水;④二氧化碳;⑤碳酸钠固体;⑥氢氧化钡溶液;⑦纯醋酸;⑧氯化氢气体。(填序号)
(1)其中能导电的是_______ ;属于非电解质的是_______ ;属于电解质的是_______ 。
Ⅱ.某100mL溶液可能含有 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知 和
和 反应有气体产生且全部逸出)。
反应有气体产生且全部逸出)。
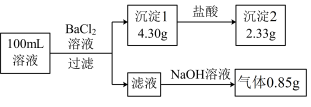
(2)原溶液中除含有 外,一定还含有
外,一定还含有_______ 离子,可能含有_______ 离子;
(3)实验中生成碳酸钡的离子方程式为_______ 。
(1)其中能导电的是
Ⅱ.某100mL溶液可能含有
 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知 和
和 反应有气体产生且全部逸出)。
反应有气体产生且全部逸出)。
(2)原溶液中除含有
 外,一定还含有
外,一定还含有(3)实验中生成碳酸钡的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E均为短周期主族元素,其原子序数依次增大。其中A元素原子核内只有一个质子;A与C、B与D分别同主族;B、D两元素原子序数之和是A、C两元素原子序数之和的2倍。请回答下列问题:
(1)由上述元素组成的下列物质中属于非电解质的是___________(填字母)。
(2)D元素在元素周期表中的位置为___________ ;写出A元素分别与B、D形成的18个电子的分子的化学式___________ 、___________ 。
(3)①单质C在 中反应的离子方程式是
中反应的离子方程式是___________ ;
②实验室制取 的化学方程式是
的化学方程式是___________ 。
(1)由上述元素组成的下列物质中属于非电解质的是___________(填字母)。
A. | B.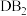 | C. | D.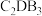 |
(3)①单质C在
 中反应的离子方程式是
中反应的离子方程式是②实验室制取
 的化学方程式是
的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ. (H-O-O-H)既有氧化性又有还原性,其中氧处于中间价态。完成下列填空:
(H-O-O-H)既有氧化性又有还原性,其中氧处于中间价态。完成下列填空:
(1) 是二元弱酸,则
是二元弱酸,则 的第一步电离方程式为
的第一步电离方程式为_______ 。
(2)已知: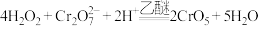 ,
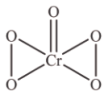
, 结构如图所示,该反应
结构如图所示,该反应_______ (选填“是”或“不是”)氧化还原反应,理由是_______ 。
(3)少量 催化分解
催化分解 的反应分两步进行,第一步:
的反应分两步进行,第一步: ;写出第二步反应的离子方程式。
;写出第二步反应的离子方程式。_______
Ⅱ.称取1.023g (
(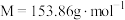 )加入20.0mL
)加入20.0mL 酸化后定容至100mL,取出10.00mL用
酸化后定容至100mL,取出10.00mL用 的
的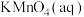 滴定至终点,消耗
滴定至终点,消耗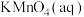 24.34mL。
24.34mL。
已知:①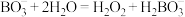
②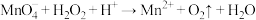 (未配平)
(未配平)
(4)配平离子方程式。_______

(5)实验所需的定量仪器有电子天平、量筒、_______ 。
(6)滴定终点的现象为溶液变为_______ 色,且30s不变色。理论上消耗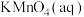
_______ mL,实验过程操作正确,产生误差的原因可能是_______ 。
 (H-O-O-H)既有氧化性又有还原性,其中氧处于中间价态。完成下列填空:
(H-O-O-H)既有氧化性又有还原性,其中氧处于中间价态。完成下列填空:(1)
 是二元弱酸,则
是二元弱酸,则 的第一步电离方程式为
的第一步电离方程式为(2)已知:
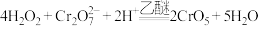 ,
, 结构如图所示,该反应
结构如图所示,该反应
(3)少量
 催化分解
催化分解 的反应分两步进行,第一步:
的反应分两步进行,第一步: ;写出第二步反应的离子方程式。
;写出第二步反应的离子方程式。Ⅱ.称取1.023g
 (
(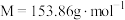 )加入20.0mL
)加入20.0mL 酸化后定容至100mL,取出10.00mL用
酸化后定容至100mL,取出10.00mL用 的
的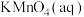 滴定至终点,消耗
滴定至终点,消耗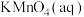 24.34mL。
24.34mL。已知:①
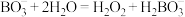
②
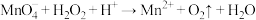 (未配平)
(未配平)(4)配平离子方程式。

(5)实验所需的定量仪器有电子天平、量筒、
(6)滴定终点的现象为溶液变为
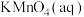
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】从元素化合价和物质类别两个角度研究物质的性质,是一种行之有效的方法。以下是铁元素组成物质的二维图的部分信息。
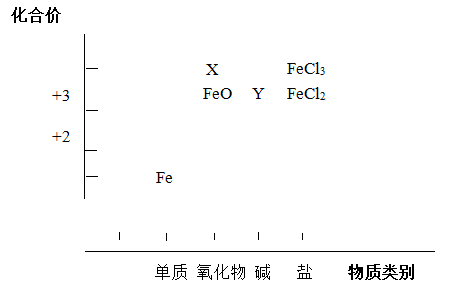
(1)分别写出X、Y的化学式______ 、______ 。
(2)写出FeO与稀硫酸反应的化学方程式____________ 。
(3)FeCl2既具有氧化性也具有还原性,分别写出体现其氧化性、还原性的反应的离子方程式。
(4)某同学预测Fe3+可以与S2-发生反应,为验证预测,他结合资料信息,选择了两种试剂进行实验,确认了反应的发生。
资料:部分硫化物的溶解性表(室温)
选取的试剂是______ 和______ ;可能发生的两种不同原理 的反应的离子方程式是:_________ 、__________ 。

(1)分别写出X、Y的化学式
(2)写出FeO与稀硫酸反应的化学方程式
(3)FeCl2既具有氧化性也具有还原性,分别写出体现其氧化性、还原性的反应的离子方程式。
 | 离子方程式 |
| 氧化性 | |
| 还原性 |
资料:部分硫化物的溶解性表(室温)
| 阴离子 阳离子 | S2- |
| Na+ | 溶 |
| Fe3+ | 不 |
| Fe2+ | 不 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】如图表示中学化学中常见物质的转化关系(部分条件已略去)。其中A属于正盐,B、C、E是常见的气体,C能使湿润的红色石蕊试纸变蓝,D是一种淡黄色固体。

回答下列问题:
(1)A物质的化学式是___________ ,A中存在的化学键有___________ 。
(2)C的电子式是___________ ,在上述①~④反应中属于氧化还原反应的是___________ (填编号)。
(3)写出B和D反应生成E的化学方程式,并用单线桥法表示电子的转移:___________ 。
(4)请写出反应④的化学方程式:___________ ,写出该反应在工业上的用途:___________ 。

回答下列问题:
(1)A物质的化学式是
(2)C的电子式是
(3)写出B和D反应生成E的化学方程式,并用单线桥法表示电子的转移:
(4)请写出反应④的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】金属M在酸性或碱性溶液中均可与HNO3发生氧化还原反应,转化关系如下(部分生成物未列出):

已知:C、D、E、G均为气体,且G为单质;将D通入A溶液产生白色沉淀;将F逐滴加入B溶液至过量,先产生白色沉淀,随后沉淀消失。
请回答下列问题:
(1)写出下列物质的化学式:M___ 、F___ 、G___ 。
(2)A溶液与B溶液混合也能产生白色沉淀,写出该反应的离子方程式______________ 。
(3)除去气体C中的气体E的化学方法是_______________________________________ 。
(4)将10mL充满气体E和O2混合气的试管倒扣在水槽中,反应后试管中残留1mL无色气体,则试管中气体E的体积是_________________ mL。
(5)D →C反应的化学方程式是____________________________________________ 。
(6)M与NO3-在碱性条件下反应的离子方程式为___________________________________ 。

已知:C、D、E、G均为气体,且G为单质;将D通入A溶液产生白色沉淀;将F逐滴加入B溶液至过量,先产生白色沉淀,随后沉淀消失。
请回答下列问题:
(1)写出下列物质的化学式:M
(2)A溶液与B溶液混合也能产生白色沉淀,写出该反应的离子方程式
(3)除去气体C中的气体E的化学方法是
(4)将10mL充满气体E和O2混合气的试管倒扣在水槽中,反应后试管中残留1mL无色气体,则试管中气体E的体积是
(5)D →C反应的化学方程式是
(6)M与NO3-在碱性条件下反应的离子方程式为
您最近一年使用:0次
【推荐2】为探究固体化合物X (仅含三种元素)的组成和性质,溶液D是单一盐的溶液, 某同学设计并完成如下实验。

请回答:
(1) 气体A在标准状况下的密度为1.96 g/L,气体A的化学式是___________ 。
(2) X所含的三种元素为___________ 。
(3)写出X隔绝空气灼烧的方程式___________ 。
(4)写出D和氢氧化钠反应的离子方程式___________ 。

请回答:
(1) 气体A在标准状况下的密度为1.96 g/L,气体A的化学式是
(2) X所含的三种元素为
(3)写出X隔绝空气灼烧的方程式
(4)写出D和氢氧化钠反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色实验均为黄色。
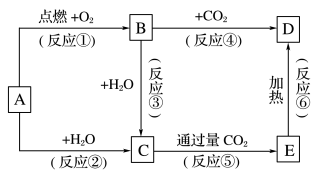
请填写下列空白:
(1)写出下列化学式:A____________ ,D____________
(2)以上反应中,不属于氧化还原反应的有________________ (填序号)。
(3)完成方程式

请填写下列空白:
(1)写出下列化学式:A
(2)以上反应中,不属于氧化还原反应的有
(3)完成方程式
①A→C反应的离子方程式:
②B→D反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D是中学化学中的常见物质,各物质的转化关系如下:
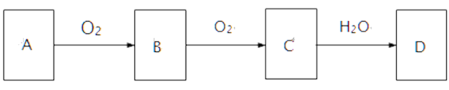
(1)若A是黄色固体,B是形成酸雨的主要成分。
①画出A的原子结构示意图___________
②写出D的浓溶液所具有的特殊性质___________ (两种即可)
(2)若此反应流程能解释农谚“雷雨发庄稼”的化学原理,则叙述正确的是___________
(3)若A、B、C、D的焰色反应均为黄色,C为淡黄色固体,A在加热条件下可直接转化为C,则C→D的化学方程式是___________
(4)若A是化合物,且此流程表示工业制硝酸的物质转化关系,则A→B的反应方程式为___________

(1)若A是黄色固体,B是形成酸雨的主要成分。
①画出A的原子结构示意图
②写出D的浓溶液所具有的特殊性质
(2)若此反应流程能解释农谚“雷雨发庄稼”的化学原理,则叙述正确的是___________
| A.A的化学性质较为稳定 | B.B、C均为酸性氧化物 |
| C.流程中的反应均属氧化还原反应 | D.可用D与金属反应制取氢气 |
(4)若A是化合物,且此流程表示工业制硝酸的物质转化关系,则A→B的反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为测定含有Na2O杂质的Na2O2样品的纯度,甲、乙二位同学设计了二种不同的实验方案。
已知:2Na2O2+2CO2=2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑
甲:用图l所示装置,通过测定Na2O2与CO2反应生成O2的体积来测定样品的纯度。

(1)C中所盛的药品是:______________ 。
(2)A中橡皮管的作用是:_________________________________________________ 。
(3)利用该实验方案所测Na2O2的纯度明显偏大,其原因可能是_______ (填选项字母)。
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左高右低
d.读数时U形量气管中的液面左低右高
乙:称取3.500 g试样,配成1000.00 mL溶液,用0.1000 mol·L-1的标准盐酸滴定。
(4)取上述所配溶液25.00 mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图_________ ,取溶液所用仪器的名称是______________ 。

(5)滴定操作平行实验的数据记录如下表:
由表中数据计算样品中Na2O2纯度为__________ 。
已知:2Na2O2+2CO2=2Na2CO3+O2 2Na2O2+2H2O=4NaOH+O2↑
甲:用图l所示装置,通过测定Na2O2与CO2反应生成O2的体积来测定样品的纯度。

(1)C中所盛的药品是:
(2)A中橡皮管的作用是:
(3)利用该实验方案所测Na2O2的纯度明显偏大,其原因可能是
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左高右低
d.读数时U形量气管中的液面左低右高
乙:称取3.500 g试样,配成1000.00 mL溶液,用0.1000 mol·L-1的标准盐酸滴定。
(4)取上述所配溶液25.00 mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图

(5)滴定操作平行实验的数据记录如下表:
| 滴定次数 | 第一次滴定 | 第二次滴定 | 第三次滴定 |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
由表中数据计算样品中Na2O2纯度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、D、E、F为短周期元素,非金属元素 A 最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的 2 倍。 B在 D中充分燃烧能生成其最高价化合物 BD2。E+与D2-具有相同的电子数。 A 在 F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是____________ ,写出单质 F和NaOH的离子方程式____________ 。
(2)B、D、E 组成的一种盐中, E的质量分数为43%,其俗名为________ ,其水溶液与等物质的量的 F单质反应的化学方程式为___________________ ;
(3)由这些元素组成的物质,其组成和结构信息如下表:
a的化学式为_______ ;b与水反应的化学方程式为_______ ;
(1)A在周期表中的位置是
(2)B、D、E 组成的一种盐中, E的质量分数为43%,其俗名为
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
您最近一年使用:0次



