大气臭氧层可以保护地球生物免受紫外线的伤害,但低空臭氧的浓度过高时对人体有害。
(1)在紫外线作用下,氧气可转化臭氧:
①该反应所属类型为_______ (填“氧化还原”或“非氧化还原”)反应。
②若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为_______ 。
③某区域收集到 和
和 混合气体10g,标准状况下体积为5.6L,其中
混合气体10g,标准状况下体积为5.6L,其中 与
与 的体积之比为
的体积之比为_______ 。
(2)实验室中常用碘量法检测臭氧,其中以淀粉为指示剂,将臭氧通入含有硫酸的碘化钾溶液中进行反应,反应后生成能使带火星的木条复燃的气体,溶液变蓝,则反应的离子方程式为_______ 。
(3)现需450mL 的
的 溶液,用
溶液,用 固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。
固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。
①还缺少的仪器有_______ 、_______ 。
②在配制过程中,下列操作会导致所配制溶液的浓度偏小的是_______ (填字母)。
A.未洗涤烧杯和玻璃棒
B.使用前,容量瓶中有少量蒸馏水
C.定容时俯视凹液面
D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线
(1)在紫外线作用下,氧气可转化臭氧:

①该反应所属类型为
②若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为
③某区域收集到
 和
和 混合气体10g,标准状况下体积为5.6L,其中
混合气体10g,标准状况下体积为5.6L,其中 与
与 的体积之比为
的体积之比为(2)实验室中常用碘量法检测臭氧,其中以淀粉为指示剂,将臭氧通入含有硫酸的碘化钾溶液中进行反应,反应后生成能使带火星的木条复燃的气体,溶液变蓝,则反应的离子方程式为
(3)现需450mL
 的
的 溶液,用
溶液,用 固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。
固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。①还缺少的仪器有
②在配制过程中,下列操作会导致所配制溶液的浓度偏小的是
A.未洗涤烧杯和玻璃棒
B.使用前,容量瓶中有少量蒸馏水
C.定容时俯视凹液面
D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线
更新时间:2022-12-17 13:12:53
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知NA为阿伏加德罗常数的值。回答下列问题:
(1)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是___ (填化学式,下同),在相同温度和相同压强条件下,体积最大的是___ 。
(2)73.0 g HCl气体中含有的分子数为___ ,标准状况下的体积为___ L。
(3)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为___ ,R的相对原子质量为___ 。
(4)已知CO、CO2的混合气体质量共16.0 g,标准状况下体积为8.96 L,则该混合气体中CO与CO2的体积比为___ 。
(1)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是
(2)73.0 g HCl气体中含有的分子数为
(3)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为
(4)已知CO、CO2的混合气体质量共16.0 g,标准状况下体积为8.96 L,则该混合气体中CO与CO2的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氯化亚铜常用作催化剂、杀菌剂、脱色剂,工业上用如下反应制备CuCl:2CuSO4+Na2SO3+2NaCl+Na2CO3=2CuCl+3Na2SO4+CO2↑。回答下列问题:
(1)14.2 g Na2SO4 中Na+的物质的量是_______ mol。
(2)0.1 mol CuSO4中含O原子的物质的量是_______ mol。
(3)上述若生成0.2 mol CuCl时,同时生成标准状况下CO2的体积是_______ L。
(1)14.2 g Na2SO4 中Na+的物质的量是
(2)0.1 mol CuSO4中含O原子的物质的量是
(3)上述若生成0.2 mol CuCl时,同时生成标准状况下CO2的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Fe3+与SCN-生成Fe(SCN)3_______ ;
Ag+与NH3·H2O生成[Ag(NH3)2]+_______ 。
Ag+与NH3·H2O生成[Ag(NH3)2]+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有十种物质:①铝②盐酸③醋酸④氨气⑤氯化钠⑥干冰⑦蔗糖⑧纯水⑨熔融硫酸钡⑩碳酸钠溶液,按要求填空:
(1)属于电解质的是___________ 。
(2)属于非电解质的是___________ 。
(3)能导电的是___________ 。
(4)请写出③与⑩反应的离子方程式___________ 。
(1)属于电解质的是
(2)属于非电解质的是
(3)能导电的是
(4)请写出③与⑩反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】将一定质量的镁、铝合金,投入100mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加5mol/L NaOH溶液,生成的沉淀质量与加入NaOH溶液体积如图所示,由图中数据分析计算:(必须有计算过程,否则不得分)
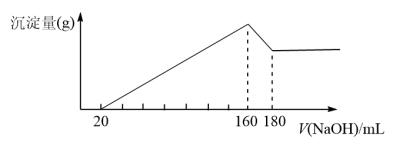
(1)Al与NaOH反应的离子方程式_________________________
(2)铝的质量______________
(3)盐酸的物质的量浓度______________

(1)Al与NaOH反应的离子方程式
(2)铝的质量
(3)盐酸的物质的量浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】实验室欲用NaOH固体配制1.0 mol/L的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却。
其正确的操作顺序为___________ ⑤⑥⑤__________ 。本实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、胶头滴管、还有_____________________ 。
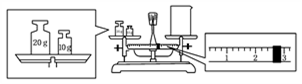
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,烧杯的实际质量为_________ g。要完成本实验该同学应称出_________ g NaOH。
(3)对所配制的NaOH溶液进行测定,发现其浓度低于1.0mol/L。在溶液配制过程中,下列操作会引起该误差的有_________ (填序号)。
A.转移溶解的溶液后没有洗涤烧杯和玻璃棒
B.转移溶液时不慎有少量洒到容量瓶外面
C.容量瓶未干燥就用来配制溶液
D.称量NaOH固体时动作太慢,耗时太长
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平
F.定容时仰视刻度线
G.NaOH固体溶解后未经冷却即转移到容量瓶中
(4)氢氧化钠是一种用途十分广泛的重要化工原料,工业上主要通过电解氯化钠饱和溶液的方法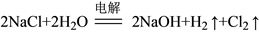 。试用单线桥法标出该反应中电子转移的方向和数目
。试用单线桥法标出该反应中电子转移的方向和数目____________________ 。实验测得,反应中生成的气体在标准状况下的体积为4.48L,则耗氧化剂的物质的量为_________ mol。
(1)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却。
其正确的操作顺序为
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,烧杯的实际质量为

(3)对所配制的NaOH溶液进行测定,发现其浓度低于1.0mol/L。在溶液配制过程中,下列操作会引起该误差的有
A.转移溶解的溶液后没有洗涤烧杯和玻璃棒
B.转移溶液时不慎有少量洒到容量瓶外面
C.容量瓶未干燥就用来配制溶液
D.称量NaOH固体时动作太慢,耗时太长
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平
F.定容时仰视刻度线
G.NaOH固体溶解后未经冷却即转移到容量瓶中
(4)氢氧化钠是一种用途十分广泛的重要化工原料,工业上主要通过电解氯化钠饱和溶液的方法
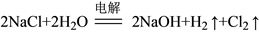 。试用单线桥法标出该反应中电子转移的方向和数目
。试用单线桥法标出该反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】实验室某次实验需用0.1 mol/LNa2CO3溶液250 mL,填空并回答下列问题:
(1)容量瓶使用前应查看___________(选填序号)。
(2)配制适用体积的0.1 mol/LNa2CO3溶液,需称取Na2CO3质量___________ g。
(3)配制时,其正确的操作顺序是(填字母,每个字母只能用一次)___________ 。
A.用30mL水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.将准确称量的Na2CO3固体倒入烧杯中,再加适量水溶解
C.将已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线下1~2cm处
(4)Na2CO3固体在烧杯中溶解后,溶液注入容量瓶前需恢复到室温,这是因为___________ 。
(5)若配制过程中称量、溶解和定容读数操作都准确无误,但所配溶液的浓度偏小,其原因可能是:___________ 。
(1)容量瓶使用前应查看___________(选填序号)。
| A.气密性 | B.是否干燥 | C.是否漏水 | D.是否符合容量规格 |
(3)配制时,其正确的操作顺序是(填字母,每个字母只能用一次)
A.用30mL水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.将准确称量的Na2CO3固体倒入烧杯中,再加适量水溶解
C.将已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线下1~2cm处
(4)Na2CO3固体在烧杯中溶解后,溶液注入容量瓶前需恢复到室温,这是因为
(5)若配制过程中称量、溶解和定容读数操作都准确无误,但所配溶液的浓度偏小,其原因可能是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室需要配制450mL 1.0mol/L的NaCl溶液,请回答下列问题:
(1)应选用容量瓶的规格是___________ mL。
(2)若用固体NaCl配制,用托盘天平称取NaCl的质量为___________ ,若用5mol/L NaCl的浓溶液来配制,则使用量筒量取浓溶液的体积为___________ 。
(3)容量瓶上标有___________ (选填序号)。
①温度;②浓度;③容量;④压强;⑤刻度线
(4)若选用浓溶液稀释来配制,用量筒量取一定体积的浓NaCl溶液,读数时仰视刻度线,则所配制溶液的物质的量浓度会___________ (选填“偏高”、“偏低”或“不变”)
(1)应选用容量瓶的规格是
(2)若用固体NaCl配制,用托盘天平称取NaCl的质量为
(3)容量瓶上标有
①温度;②浓度;③容量;④压强;⑤刻度线
(4)若选用浓溶液稀释来配制,用量筒量取一定体积的浓NaCl溶液,读数时仰视刻度线,则所配制溶液的物质的量浓度会
您最近一年使用:0次



