I.实验室从海藻中提取碘的流程如下:回答下列问题:
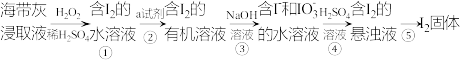
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、_________________ 。
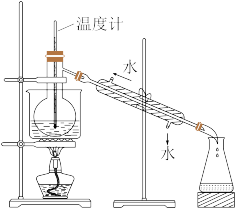
(2)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出右图实验装置中的错误之处:①__ ;②______ ;③_______ 。
(3)步骤④中反应的离子方程式为________ , 在此反应中,每生成38.1gI2转移_____ mol电子。
(4)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是____________ 。
II.如图是某工厂对海水资源进行综合利用的示意图。回答下列问题:

(5)①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法及步骤是______________ 。
②操作b是在通入HCl的氛围中进行,否则会生成Mg(OH)2,写出生成Mg(OH)2的化学方程式:____ 。
(6)金属镁的制备方程式为________ 。
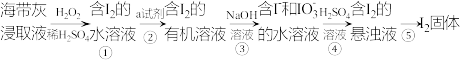
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、
(2)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出右图实验装置中的错误之处:①

(3)步骤④中反应的离子方程式为
(4)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是
II.如图是某工厂对海水资源进行综合利用的示意图。回答下列问题:

(5)①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法及步骤是
②操作b是在通入HCl的氛围中进行,否则会生成Mg(OH)2,写出生成Mg(OH)2的化学方程式:
(6)金属镁的制备方程式为
22-23高二上·河北石家庄·阶段练习 查看更多[2]
更新时间:2022-12-16 13:15:49
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行以下实验:
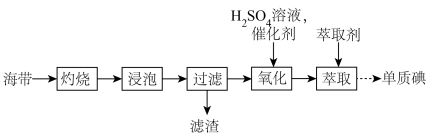
(1)“灼烧”海带时,除需要三脚架、酒精灯外,还需要用到的实验仪器___________ 。(填字母)
a.烧杯 b.坩埚 c.表面皿 d.泥三角
(2)“浸泡”时要将悬浊液煮沸一段时间,目的是___________ 。
(3)“氧化”时氧化剂的选择将影响实验结果。
①若选用 作氧化剂,“氧化”时发生反应的离子方程式为
作氧化剂,“氧化”时发生反应的离子方程式为___________ 。
②若选用新制氯水作氧化剂,氯水过量时可能发生反应: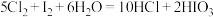 。请用单线桥法表示出该化学反应的电子转移的方向和数目
。请用单线桥法表示出该化学反应的电子转移的方向和数目___________ 。
(4)“萃取”过程中可以选择 作为萃取剂的理由是
作为萃取剂的理由是___________ 。
(5)设计一种检验提取碘后的水溶液中是否含有单质碘的简单方法___________ 。

(1)“灼烧”海带时,除需要三脚架、酒精灯外,还需要用到的实验仪器
a.烧杯 b.坩埚 c.表面皿 d.泥三角
(2)“浸泡”时要将悬浊液煮沸一段时间,目的是
(3)“氧化”时氧化剂的选择将影响实验结果。
①若选用
 作氧化剂,“氧化”时发生反应的离子方程式为
作氧化剂,“氧化”时发生反应的离子方程式为②若选用新制氯水作氧化剂,氯水过量时可能发生反应:
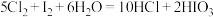 。请用单线桥法表示出该化学反应的电子转移的方向和数目
。请用单线桥法表示出该化学反应的电子转移的方向和数目(4)“萃取”过程中可以选择
 作为萃取剂的理由是
作为萃取剂的理由是(5)设计一种检验提取碘后的水溶液中是否含有单质碘的简单方法
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】海带、紫菜中均含有丰富的碘元素,从海带中提取碘单质的流程如下,思考解答下列问题:
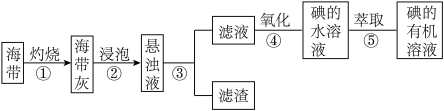
(1)实验操作③的名称是______ 。
(2)根据元素周期表中元素性质的递变规律,实验操作④反应的离子方程式是______ 。
(3)实验操作⑤中不选用酒精的理由:_______ 。
(4)为使海带灰中碘离子转化为碘的有机溶液,实验室里有烧杯玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器物品,尚缺少的玻璃仪器是_____ 。

(1)实验操作③的名称是
(2)根据元素周期表中元素性质的递变规律,实验操作④反应的离子方程式是
(3)实验操作⑤中不选用酒精的理由:
(4)为使海带灰中碘离子转化为碘的有机溶液,实验室里有烧杯玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器物品,尚缺少的玻璃仪器是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提取碘的方法之一,其流程如下:
Ⅰ.pH=2时, 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO;
,同时生成NO;
Ⅱ.
Ⅲ. 在碱性溶液中反应生成
在碱性溶液中反应生成 和
和 。
。
(1)反应①的离子方程式___________ 。
(2)方案甲中,根据 的特性,分离操作X应为
的特性,分离操作X应为___________ 。
(3) 、酸性
、酸性 等都是常用的强氧化剂,但该工艺中氧化卤水中的
等都是常用的强氧化剂,但该工艺中氧化卤水中的 却选择了价格较高的
却选择了价格较高的 ,原因是
,原因是___________ 。
(4)写出反应②的离子反应方程式___________ 。
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的 、
、 。若检验滤液中的
。若检验滤液中的 ,需要选择下列哪些试剂完成检验(填序号)
,需要选择下列哪些试剂完成检验(填序号)___________ 。
可供选择的试剂:①无水乙醇② ③氢氧化钠溶液④稀
③氢氧化钠溶液④稀 ⑤淀粉溶液⑥
⑤淀粉溶液⑥ 溶液。
溶液。

Ⅰ.pH=2时,
 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO;
,同时生成NO;Ⅱ.

Ⅲ.
 在碱性溶液中反应生成
在碱性溶液中反应生成 和
和 。
。(1)反应①的离子方程式
(2)方案甲中,根据
 的特性,分离操作X应为
的特性,分离操作X应为(3)
 、酸性
、酸性 等都是常用的强氧化剂,但该工艺中氧化卤水中的
等都是常用的强氧化剂,但该工艺中氧化卤水中的 却选择了价格较高的
却选择了价格较高的 ,原因是
,原因是(4)写出反应②的离子反应方程式
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的
 、
、 。若检验滤液中的
。若检验滤液中的 ,需要选择下列哪些试剂完成检验(填序号)
,需要选择下列哪些试剂完成检验(填序号)可供选择的试剂:①无水乙醇②
 ③氢氧化钠溶液④稀
③氢氧化钠溶液④稀 ⑤淀粉溶液⑥
⑤淀粉溶液⑥ 溶液。
溶液。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】镁及其合金是用途很广的金属材料。大量的镁是从海水中提取的,海水提镁的主要步骤如图所示:

回答下列问题:
(1)Na元素位于元素周期表的_______ (填“s”、“p”、“d”或“ds”)区。
(2)元素Cl、Mg、Na的原子半径由大到小的顺序为_______ (用元素符号表示)。
(3) 属于
属于_______ (填“分子”、“离子”或“共价”)晶体,判断的理由为_______ 。
(4)若将“ 溶液”(无其他溶质)直接蒸干,
溶液”(无其他溶质)直接蒸干,_______ (填“能”或“不能”)得无水氯化镁,判断的理由为_______ 。
(5)氯化钠晶体结构模型如图所示:

①氯化钠晶体中,每个离子可吸引周围_______ 个带异性电荷的离子。
②氯化钠晶体中,每个 周围最近且等距离的
周围最近且等距离的 有
有_______ 个。
(6)氟与氯位于同一主族,查阅资料可知: 的熔点为1534K,NaF的熔点为1266K,NaF的熔点低于
的熔点为1534K,NaF的熔点为1266K,NaF的熔点低于 的熔点的原因为
的熔点的原因为_______ 。

回答下列问题:
(1)Na元素位于元素周期表的
(2)元素Cl、Mg、Na的原子半径由大到小的顺序为
(3)
 属于
属于(4)若将“
 溶液”(无其他溶质)直接蒸干,
溶液”(无其他溶质)直接蒸干,(5)氯化钠晶体结构模型如图所示:

①氯化钠晶体中,每个离子可吸引周围
②氯化钠晶体中,每个
 周围最近且等距离的
周围最近且等距离的 有
有(6)氟与氯位于同一主族,查阅资料可知:
 的熔点为1534K,NaF的熔点为1266K,NaF的熔点低于
的熔点为1534K,NaF的熔点为1266K,NaF的熔点低于 的熔点的原因为
的熔点的原因为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】开发利用海水化学资源的部分过程如图所示,下列说法不正确的是___________ 。
(2)流程中的②③④⑤步中,属于非氧化还原反应的是___________ 。
(3)步骤④中Na2CO3溶液用于吸收Br2,根据Br2的性质,下列物质也可以用于大量吸收Br2的是___________。
(4)步骤⑤中仅有溴元素的化合价发生变化,每获取3molBr2,转移的电子数目为_________ 。
(5)粗盐中含有Mg2+、Ca2+、 ,得到精盐的步骤中添加试剂的顺序为
,得到精盐的步骤中添加试剂的顺序为___________ ,___________ ,NaOH、过滤、盐酸。(填试剂的化学式)
(6)利用步骤①中得到的精盐配制100mL0.1mol/L的NaCl溶液,实验中需要用到的玻璃仪器除了烧杯、玻璃棒还需要___________ 。

(2)流程中的②③④⑤步中,属于非氧化还原反应的是
(3)步骤④中Na2CO3溶液用于吸收Br2,根据Br2的性质,下列物质也可以用于大量吸收Br2的是___________。
| A.NaCl溶液 | B.FeCl3溶液 |
| C.酸性高锰酸钾溶液 | D.FeCl2溶液 |
(4)步骤⑤中仅有溴元素的化合价发生变化,每获取3molBr2,转移的电子数目为
(5)粗盐中含有Mg2+、Ca2+、
 ,得到精盐的步骤中添加试剂的顺序为
,得到精盐的步骤中添加试剂的顺序为(6)利用步骤①中得到的精盐配制100mL0.1mol/L的NaCl溶液,实验中需要用到的玻璃仪器除了烧杯、玻璃棒还需要
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海洋经济已经成为拉动我国国民经济发展的重要引擎,海水的综合开发、利用是海洋经济的一部分,海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。其流程如图所示:
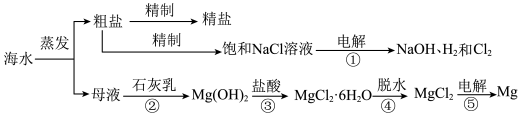
(1)写出镁原子的结构示意图:_______ 。在反应①→⑤中属于氧化还原反应的是______ 。(填序号)
(2)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、________ 溶液;③_________ ;④滤液中加适量盐酸;⑤__________ 。(请补全缺少的实验步骤或试剂)
(3)某同学利用反应①原理制备氯气,将400 mL 5.0 mol·L-1NaCl溶液进行电解,则理论上最多可制得标准状况下氯气的体积为_____ L。
(4)实验室模拟Mg的制取流程时,用11.3 mol·L-1的浓盐酸配置反应③所需要的0.5 mol·L-1稀盐酸100 ml,需要用量筒量取浓盐酸________ ml,接下来的配置过程除了玻璃棒和烧杯外,还需要用到的玻璃仪器有_______ 。

(1)写出镁原子的结构示意图:
(2)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、
(3)某同学利用反应①原理制备氯气,将400 mL 5.0 mol·L-1NaCl溶液进行电解,则理论上最多可制得标准状况下氯气的体积为
(4)实验室模拟Mg的制取流程时,用11.3 mol·L-1的浓盐酸配置反应③所需要的0.5 mol·L-1稀盐酸100 ml,需要用量筒量取浓盐酸
您最近一年使用:0次



