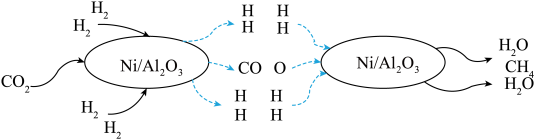
下列说法中正确的说法有几个
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
⑤也能用固体或纯液体的变化量来表示反应快慢
⑥催化剂能增大活化分子百分数,从而增大化学反应速率
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
⑤也能用固体或纯液体的变化量来表示反应快慢
⑥催化剂能增大活化分子百分数,从而增大化学反应速率
| A.①②③ | B.①③⑥ | C.①④⑤ | D.③⑤⑥ |
更新时间:2022-12-01 13:09:39
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在 催化下,
催化下, 与
与 制备乙醛的反应机理如图所示,下列说法正确的是
制备乙醛的反应机理如图所示,下列说法正确的是

 催化下,
催化下, 与
与 制备乙醛的反应机理如图所示,下列说法正确的是
制备乙醛的反应机理如图所示,下列说法正确的是
A.增加 的量, 的量, 的平衡转化率增大 的平衡转化率增大 |
| B.过程①~⑥中铁元素化合价均发生变化 |
C.X为 ,是反应的产物之一 ,是反应的产物之一 |
D.每消耗 可制备 可制备 乙醛 乙醛 |
您最近一年使用:0次
【推荐2】2021年12月28日,中国科学院微生物研究所李寅团队发表了历时5年设计的全新最小化人工固碳循环图。下列关于该循环图叙述错误的是
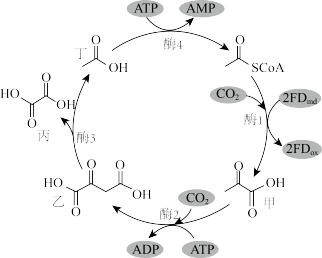

| A.甲、乙、丙、丁均能与乙醇发生酯化反应 |
B.甲与 生成乙的反应是取代反应 生成乙的反应是取代反应 |
| C.该循环过程中存在非极性键的断裂和生成 |
D.每轮循环可以转化两分子 生成一分子草酸 生成一分子草酸 |
您最近一年使用:0次