铁、铝在生产生活中有广泛的应用。完成下列填空:
(1)铝用作电线是利用了铝的_______ 性;铁用作炊具是利用了铁的_______ 性。
(2)常温下由于浓硫酸能使铁_______ ,因此浓硫酸可用铁槽车运输。
(3)氢氧化铝既能跟盐酸反应又能跟氢氧化钠溶液反应,由此可知氢氧化铝是_______ 物质。氢氧化铝和盐酸反应的离子方程式为_______ 。
(4)氯元素原子结构示意图为_______ ,其与钠元素组成的化合物的电子式为_______ 。
(5)钠、铝、铁三种金属元素中,_______ (填名称)是地壳中含量最高的金属元素,其在周期表中位于第_______ 周期_______ 族。
(6)以下不是铝和铁的共同性质的是_______ 。
a.导电性 b.导热性 c.延展性 d.两性
(7)列举一个可以说明氯和硫的非金属性强弱的事实用化学方程式表示_______ 。
(1)铝用作电线是利用了铝的
(2)常温下由于浓硫酸能使铁
(3)氢氧化铝既能跟盐酸反应又能跟氢氧化钠溶液反应,由此可知氢氧化铝是
(4)氯元素原子结构示意图为
(5)钠、铝、铁三种金属元素中,
(6)以下不是铝和铁的共同性质的是
a.导电性 b.导热性 c.延展性 d.两性
(7)列举一个可以说明氯和硫的非金属性强弱的事实用化学方程式表示
更新时间:2022-12-03 21:02:04
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
请回答下列问题。
(1)元素a中,含有1个质子和1个中子的核素的原子符号为_______ 。e的离子结构示意图为_______ ,元素 g在周期表中的位置为_______ 。
(2)仅由c、d组成,既含离子键又含非极性键的化合物的电子式为_______ 。
(3)非金属性,f_______ g(填“>”或“<”),能证明该结论的依据为_______ (列举一条)。
(4)写出三种简单离子a- 、d+、g- 半径由小到大的顺序:_______ (用相应的化学式表示)。
(5)写出h元素的低价氢氧化物露置在空气中发生反应的化学方程式_______ 。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | ||||||||||||||
h |
(1)元素a中,含有1个质子和1个中子的核素的原子符号为
(2)仅由c、d组成,既含离子键又含非极性键的化合物的电子式为
(3)非金属性,f
(4)写出三种简单离子a- 、d+、g- 半径由小到大的顺序:
(5)写出h元素的低价氢氧化物露置在空气中发生反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.用序号按要求回答下列问题:
(1)下列各种物质:①H2O②NH3③KOH④Na2O2⑤MgCl2⑥Ne,不存在化学键的是________ ;只存在离子键的是________ ;含有非极性键的离子化合物的是________ 。
(2)下列变化过程:①碘的升华②NaCl固体溶于水③O2溶于水④HCl气体溶于水⑤烧碱熔化⑥氯化铵受热分解,化学键没有被破坏的是________ ;仅破坏离子键的是________ ;仅破坏共价键的是________ ,既破坏离子键,又破坏共价键的是________ 。
(3)Na2O2的电子式为________________________ ,用电子式表示H2O的形成过程:________________________________________________ 。
Ⅱ.有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)写出这五种微粒的符号:
A______ ,B______ ,C______ ,D______ ,E______ 。
(2)B微粒的结构示意图为____________ ,C微粒的结构示意图为____________ 。
(3)A的单质与EB溶液反应的离子方程式为______________________________________ 。
(1)下列各种物质:①H2O②NH3③KOH④Na2O2⑤MgCl2⑥Ne,不存在化学键的是
(2)下列变化过程:①碘的升华②NaCl固体溶于水③O2溶于水④HCl气体溶于水⑤烧碱熔化⑥氯化铵受热分解,化学键没有被破坏的是
(3)Na2O2的电子式为
Ⅱ.有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)写出这五种微粒的符号:
A
(2)B微粒的结构示意图为
(3)A的单质与EB溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)地壳中含量最高的金属元素是________ 。
(2)根据金属的下列应用:①制电线,②制金属细丝,③制炊具,推断金属具有的物理性质是__________ 。
(3)人们每年要从金属矿物资源中提取大量的金属,根据所学化学知识,按要求写出两个生成金属的化学方程式:
①___________________________________________________ (置换反应);
②___________________________________________________ (分解反应)。
(1)地壳中含量最高的金属元素是
(2)根据金属的下列应用:①制电线,②制金属细丝,③制炊具,推断金属具有的物理性质是
(3)人们每年要从金属矿物资源中提取大量的金属,根据所学化学知识,按要求写出两个生成金属的化学方程式:
①
②
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】金属在人类社会发展进程中发挥了重要作用,钠、镁、铝、铁、铜是最重要的几种金属。
(1)上述五种金属中人们发现并最早制得其单质的是_____________ 。
(2)这五种金属单质都具有的性质是_________________ (填下列选项的序号)。
a.导电性 b.延展性 c.银白色 d.熔点高 e.硬度大
(3)钠、镁、铝、铁四种金属中,不能用于从氯化铜溶液中置换出铜的金属是_________ ,原因是 _________ (用必要的化学方程式表示)。
(4)上述金属中,有一种金属的氧化物能在另一种金属的氢氧化物的水溶液中溶解,写出反应的离子方程式:_________________ 。
(1)上述五种金属中人们发现并最早制得其单质的是
(2)这五种金属单质都具有的性质是
a.导电性 b.延展性 c.银白色 d.熔点高 e.硬度大
(3)钠、镁、铝、铁四种金属中,不能用于从氯化铜溶液中置换出铜的金属是
(4)上述金属中,有一种金属的氧化物能在另一种金属的氢氧化物的水溶液中溶解,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,回答下列有关问题:
(1)写出①原子结构示意图_______________
(2)在这些元素中,金属性最强的元素是_______ ,(填元素符号)元素⑦与元素⑧相比,非金属性较强的是 _____________ (填元素符号)
(3)⑤的最高价氧化物对应水化物与⑧的最高价氧化物对应水化物反应的离子方程式为:________________
(4)⑤的单质与③的最高价氧化物对应水化物反应的离子方程式为___________________________
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑦形成一种AB2型的化合物,请用电子式表示其形成过程:_____________________________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑪ | ⑫ |
(1)写出①原子结构示意图
(2)在这些元素中,金属性最强的元素是
(3)⑤的最高价氧化物对应水化物与⑧的最高价氧化物对应水化物反应的离子方程式为:
(4)⑤的单质与③的最高价氧化物对应水化物反应的离子方程式为
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑦形成一种AB2型的化合物,请用电子式表示其形成过程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表显示了元素周期表中的一部分。
请回答下列问题。
(1)硫元素的原子序数是_______ 。
(2)氟元素的原子结构示意图为_______ (填写字母)。
A.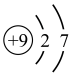 B.
B.
(3)镁元素在元素周期表的第_______ (填“二”或“三”)周期第_______ (填“ⅡA”或“ⅢA”)族。
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H_______ (填“<”或“>”)Na。
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是_______ (填“物理变化”或“化学变化”)。
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为_______ 。
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 第一周期 | 1 H 氢 | 2 He 氦 | ||||||
| 第二周期 | 3 Li 锂 | 4 Be 镀 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 第三周期1 | 1 Na 钠 | 12 Mg 镁 | 33 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 C 氯 | 18 Ar 氩 |
(1)硫元素的原子序数是
(2)氟元素的原子结构示意图为
A.
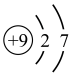 B.
B.
(3)镁元素在元素周期表的第
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】针对下面10种元素,完成以下各小题。
(1)地壳中含量最多的元素是_______ (填名称)。
(2)化学性质最不活泼的元素是_______ (填元素符号)。
(3)Al的原子结构示意图为_______ 。
(4)C与N相比,原子半径较小的是_______ 。
(5)最高价氧化物对应的水化物碱性最强的是_______ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是_______ 。
(7)S和Cl相比,元素非金属性较强的是_______ 。
(8)可用来制造光导纤维的物质是_______ ,晶体硅的主要用途是_______ (写出一种)。
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:_______ 。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)地壳中含量最多的元素是
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
(8)可用来制造光导纤维的物质是
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下图是元素周期表的一部分,根据元素在周期表中的位置回答下列问题,
(1)元素⑤在周期表中的位置描述为____________ ,元素⑧的元素符号__________________ 。
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是________________ (填化学式)。
(3)元素②的单质的电子式______________ ,元素②的简单氢化物与其最高价氧化物的水化物反应,生成物中含有的化学键________________ (填“离子键”、“极性键”或“非极性键”),元素①、②、③的简单氢化物的沸点由高到低 的顺序是___________________ (用化学式表示)。
(4)非金属性比较
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:_______ 。
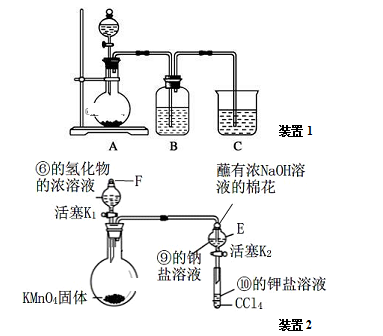
b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验_______ (填“能”或“不能”)证明非金属性⑥>⑨>⑩。
| ① | ② | ③ | |||||||||||||||
| ④ | ⑤ | ⑥ | |||||||||||||||
| ⑦ | ⑧ | ⑨ | |||||||||||||||
| ⑩ | |||||||||||||||||
(1)元素⑤在周期表中的位置描述为
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是
(3)元素②的单质的电子式
(4)非金属性比较
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:

b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】如图是元素周期表的一部分,请回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼的 是______________ (填元素符号)。
(2)③的气态氢化物的电子式______________ ,②④形成的可溶于水的气态化合物的结构式______________ 。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为______________ (填物质的化学式),酸性最强的含氧酸为______________ (填物质的化学式)。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质
(2)③的气态氢化物的电子式
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为
您最近一年使用:0次
【推荐3】研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:

(1)反应I中,主要能量转化形式为_______ 能转化为_______ 能。
(2)S在元素周期表中的位于第_______ 周期第_______ 族。
(3)下列事实能说明硫的非金属性比碳强的是_______(填标号)。
(4)反应II中检验生成的二氧化硫的方法是_______ 。
(5)反应I:2H2SO4(1)=2SO2(g)+2H2O(g)+O2(g) △H1=+551 kJ·mol-1
反应III:S(s)+O2(g=SO2(g) △H3=-297 kJ·mol-1
反应II的热化学方程式:_______ 。
(6)通过反应III也可以不经过热能转化过程而直接获取电能,化学上将实现这一直接转化的装置称为_______ 。
(7)若将反应I、II和III相加,会得到什么结果?说明什么?谈谈你的体会。_________

(1)反应I中,主要能量转化形式为
(2)S在元素周期表中的位于第
(3)下列事实能说明硫的非金属性比碳强的是_______(填标号)。
| A.H2SO3的酸性比H2CO3的酸性强 | B.在硫与碳的化合物CS2中S显负价 |
| C.硫的单质的硬度比金刚石低 | D.S的导电性比石墨的弱 |
(5)反应I:2H2SO4(1)=2SO2(g)+2H2O(g)+O2(g) △H1=+551 kJ·mol-1
反应III:S(s)+O2(g=SO2(g) △H3=-297 kJ·mol-1
反应II的热化学方程式:
(6)通过反应III也可以不经过热能转化过程而直接获取电能,化学上将实现这一直接转化的装置称为
(7)若将反应I、II和III相加,会得到什么结果?说明什么?谈谈你的体会。
您最近一年使用:0次



