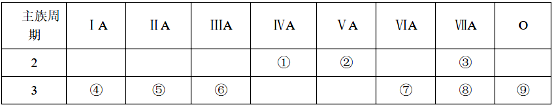
如图是元素周期表的一部分,请回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼的 是______________ (填元素符号)。
(2)③的气态氢化物的电子式______________ ,②④形成的可溶于水的气态化合物的结构式______________ 。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为______________ (填物质的化学式),酸性最强的含氧酸为______________ (填物质的化学式)。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质
(2)③的气态氢化物的电子式
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为
更新时间:2020-05-28 19:52:18
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】有A、B、C、D、E、F六种元素,它们的相关信息如下表:
请填写下列空格:
(1)A原子的电子式:_____ 。
(2)B离子的结构示意图:_______ 。
(3)C元素的名称:___ ,C原子中能量最高的电子位于第______ 层,与C离子质子数与电子数均相同的微粒可能是______ (用微粒符号表示)。
(4)D的二价阴离子的电子式:___ ,D元素的某种同位素原子质量数为34,该原子核内的中子数为_____ 。
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:_____________ 。
| 元素代号 | 相关信息 |
| A | 最外层的电子数是次外层电子数的3倍 |
| B | 海水中含量第一位的金属元素 |
| C | L层得1个电子后成为稳定结构 |
| D | 二价阴离子核外有18个电子 |
| E | 失去一个电子后就成为一个质子 |
| F | 单质为黄绿色气体,具有刺激性气味 |
请填写下列空格:
(1)A原子的电子式:
(2)B离子的结构示意图:
(3)C元素的名称:
(4)D的二价阴离子的电子式:
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学用语是中学化学基础知识的重要组成部分,是学习化学的重要工具。用化学用语回答下列问题:
(1)熔点最低的金属为___________ 。
(2)硫原子的结构示意图为___________ 。
(3)中子数为18的氯离子可表示为___________ 。
(4)空气中含量最多的气体的电子式为___________ 。
(5)短周期元素组成的最强的无机酸与 反应的离子方程式为
反应的离子方程式为___________ 。
(6)用电子式表示 的形成过程:
的形成过程:___________ 。
(1)熔点最低的金属为
(2)硫原子的结构示意图为
(3)中子数为18的氯离子可表示为
(4)空气中含量最多的气体的电子式为
(5)短周期元素组成的最强的无机酸与
 反应的离子方程式为
反应的离子方程式为(6)用电子式表示
 的形成过程:
的形成过程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下图是元素周期表的一部分,针对表中的①~⑥元素,回答下列问题
(1)最活泼的金属元素是_______________ (填元素符号)
(2)②和⑤两种元素原子半径较大的是_______________ (填元素符号),⑤和⑥两种元素最高价氧化物对应的水合物酸性较强的是_____________ (填元素符号);
(3)写出①的单质在⑥的单质中燃烧的化学方程式_______________________________________ 。
| 主族 周期 | ⅠA | 0族 | ||||||
一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
二 | ② | |||||||
三 | ③ | ④ | ⑤ | ⑥ | ||||
(1)最活泼的金属元素是
(2)②和⑤两种元素原子半径较大的是
(3)写出①的单质在⑥的单质中燃烧的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的周期性变化。
(1)下表中的实线是元素周期表的部分边界。请在表中用实线补全周期表的边界___________

(2) 元素甲是第三周期第VIA族元素,请在右边方框中按上图中氦元素的样式写出元素甲的原子序数、元素符号、元素名称和相对原子质量(取整数)___________ 。
(3)元素乙的M层电子数比K层电子数多1,甲、乙的最高价氧化物对应的水化物的酸性强弱为___________ >___________ (用化学式表示)。
(4)请写出55号元素在元素周期表中的位置:___________
(1)下表中的实线是元素周期表的部分边界。请在表中用实线补全周期表的边界

(2) 元素甲是第三周期第VIA族元素,请在右边方框中按上图中氦元素的样式写出元素甲的原子序数、元素符号、元素名称和相对原子质量(取整数)
(3)元素乙的M层电子数比K层电子数多1,甲、乙的最高价氧化物对应的水化物的酸性强弱为
(4)请写出55号元素在元素周期表中的位置:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题。
(1)今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸。其中:
ⅰ.能导电的是(填序号,下同)___________ ;
ⅱ.属于电解质的是___________ ;
ⅲ.属于非电解质的是___________ ;
ⅳ.既不是电解质又不是非电解质的是___________ 。
(2)下表是元素周期表的一部分。
ⅰ.⑧的简单离子的结构示意图为___________ 。
ⅱ.①~⑧元素形成的单质氧化性最强的是___________ (填化学式,下同),还原性最强的是___________ 。
ⅲ.②、③、⑦三种元素最高价氧化物对应的水化物中酸性最强的是___________ (填化学式,下同),②、③、④三种元素形成的简单氢化物中最稳定的是___________ 。
ⅳ.将④、⑤、⑥三种元素的简单离子半径按由大到小顺序排列:___________ (用离子符号表示)。
ⅴ.⑥的单质与⑤的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(1)今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸。其中:
ⅰ.能导电的是(填序号,下同)
ⅱ.属于电解质的是
ⅲ.属于非电解质的是
ⅳ.既不是电解质又不是非电解质的是
(2)下表是元素周期表的一部分。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
ⅱ.①~⑧元素形成的单质氧化性最强的是
ⅲ.②、③、⑦三种元素最高价氧化物对应的水化物中酸性最强的是
ⅳ.将④、⑤、⑥三种元素的简单离子半径按由大到小顺序排列:
ⅴ.⑥的单质与⑤的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】前面学习碱金属化学性质的比较时,通过金属钠、钾分别与氧气、水的反应,对比金属钠与金属钾的化学性质,再对比金属钠与金属钾的原子结构,认识原子半径对物质性质的影响,最终预测金属锂分别与氧气和水反应的现象。学习卤族元素化学性质的比较时,通过氟、氯、溴、碘与氢气的反应及卤素单质间的置换反应,对比卤族元素的性质。对于第三周期元素,电子层数相同,最外层电子数不同、原子半径不同,因此比较第三周期元素的性质时,需综合考虑最外层电子数与原子半径。
(1)问题一:可从哪些方面设计实验方案比较Na、Mg、Al金属性的强弱___ ?
(2)问题二:可从哪些方面设计实验方案比较Si、P、S、Cl非金属性的强弱___ ?
(1)问题一:可从哪些方面设计实验方案比较Na、Mg、Al金属性的强弱
(2)问题二:可从哪些方面设计实验方案比较Si、P、S、Cl非金属性的强弱
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】元素在周期表中的位置反映了元素的原子结构和性质,矿物白云母是一种重要的化工原料,其化学式的氧化物形式为:K2O·3Al2O3·6SiO2·2H2O。就其组成元素完成下列填空:
(1)Al元素在元素周期表中的位置为_____ ,K2O的电子式为_____ 。
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为_____ 。
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第_____ 族。
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是_____ 。
(1)Al元素在元素周期表中的位置为
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】镓(Ga)的原子序数为31,其合金是半导体材料。
(1)写出镓原子的电子排布式,说明镓元素在元素周期表中的位置。______
(2)写出镓元素的最高价氧化物、氯化物的化学式。______
(1)写出镓原子的电子排布式,说明镓元素在元素周期表中的位置。
(2)写出镓元素的最高价氧化物、氯化物的化学式。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】图中是元素周期表的一部分,用表中①~⑨的元素符号或物质化学式回答问题:
(1)⑦在元素周期表中的位置是___________ ;
(2)化学性质最不活泼的元素的原子结构示意图为___________ ;
(3)①~⑧中,元素原子半径最大的是___________ (填元素符号),这些元素的最高价氧化物对应的水化物中,酸性最强的酸是___________ (填化学式);
(4)请写出元素⑤的过氧化物的电子式___________ ;
(5)写出⑤与水溶液反应的离子方程式___________ ;
(6)写出⑧与氢氧化钠溶液反应的化学方程式___________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)⑦在元素周期表中的位置是
(2)化学性质最不活泼的元素的原子结构示意图为
(3)①~⑧中,元素原子半径最大的是
(4)请写出元素⑤的过氧化物的电子式
(5)写出⑤与水溶液反应的离子方程式
(6)写出⑧与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次

 电子数相同的微粒的化学式
电子数相同的微粒的化学式