有A、B、C、D、E、F六种元素,它们的相关信息如下表:
请填写下列空格:
(1)A原子的电子式:_____ 。
(2)B离子的结构示意图:_______ 。
(3)C元素的名称:___ ,C原子中能量最高的电子位于第______ 层,与C离子质子数与电子数均相同的微粒可能是______ (用微粒符号表示)。
(4)D的二价阴离子的电子式:___ ,D元素的某种同位素原子质量数为34,该原子核内的中子数为_____ 。
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:_____________ 。
| 元素代号 | 相关信息 |
| A | 最外层的电子数是次外层电子数的3倍 |
| B | 海水中含量第一位的金属元素 |
| C | L层得1个电子后成为稳定结构 |
| D | 二价阴离子核外有18个电子 |
| E | 失去一个电子后就成为一个质子 |
| F | 单质为黄绿色气体,具有刺激性气味 |
请填写下列空格:
(1)A原子的电子式:
(2)B离子的结构示意图:
(3)C元素的名称:
(4)D的二价阴离子的电子式:
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:
更新时间:2019-10-26 15:25:52
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,根据要求回答问题。
(1)④,⑥的元素符号分别是_______ ,_______ ;
(2)②的原子结构示意图是_______ ;
(3)由①和③两种元素组成的化合物的化学式是_______ ;
(4)④的最高价氧化物水化物的化学式为_______ ;
(5)④和⑤两种元素的金属性强弱顺序是④_______ ⑤(填“<”或“>”)。
族 周期 | IA | II A | IIIA | IV A | VA | VIA | VIIA | |
| 1 | ① | |||||||
| 2 | ② | ③ | Ne | |||||
| 3 | ④ | ⑤ | Al | S | ⑥ |
(1)④,⑥的元素符号分别是
(2)②的原子结构示意图是
(3)由①和③两种元素组成的化合物的化学式是
(4)④的最高价氧化物水化物的化学式为
(5)④和⑤两种元素的金属性强弱顺序是④
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】有以下物质:
①CO2 ②Al2O3 ③胆矾 ④酒精 ⑤稀硫酸 ⑥NaHCO3 ⑦石墨 ⑧
(1)属于电解质的是:___________ (填序号,下同);属于非电解质的是:___________ 。
(2)①的结构式___________ ,O2-结构示意图___________ 。
(3)②和NaOH溶液反应的化学方程式___________ 。
①CO2 ②Al2O3 ③胆矾 ④酒精 ⑤稀硫酸 ⑥NaHCO3 ⑦石墨 ⑧

(1)属于电解质的是:
(2)①的结构式
(3)②和NaOH溶液反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】表中列出了A~R这9种元素在周期表中的位置:
请回答下列问题。
(1)表中部分元素的元素符号分别是:E____ ,H___ 。
(2)R的原子结构示意图为___ 。
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___ 。
(4)A、B、C三种元素按原子半径由大到小的顺序排列为___ 。
(5)F元素与氢元素组成10个电子的分子的化学式为___ ,在常温下该分子可与B发生反应,所得溶液的pH____ 7(填“>”、“<”、“=”)。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
请回答下列问题。
(1)表中部分元素的元素符号分别是:E
(2)R的原子结构示意图为
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(4)A、B、C三种元素按原子半径由大到小的顺序排列为
(5)F元素与氢元素组成10个电子的分子的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】写出下列物质的电子式:
(1)NaCl_______ 。
(2)H2_______ 。
(3)Cl2_______ 。
(4)HCl_______ 。
(1)NaCl
(2)H2
(3)Cl2
(4)HCl
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列物质的电子式或结构式

___________ 
___________
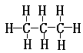
___________ 
___________


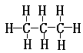

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据物质结构有关性质和特点,回答下列问题:
(1)Ti基态原子核外电子排布式为_______ ,碳原子的价电子 轨道表示式为_______ 。
(2)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积_______ (填“膨胀”或“收缩”)。
(3)SO2的空间构型为_______ 。
(4)丙烯腈(CH2=CH—CN)分子中σ键和π键的个数比为_______ ,分子中碳原子轨道杂化类型是_______ 。
(5)FeCl3熔点282℃,而FeCl2熔点674℃,二者熔点差异的原因是_______ 。
(1)Ti基态原子核外电子排布式为
(2)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积
(3)SO2的空间构型为
(4)丙烯腈(CH2=CH—CN)分子中σ键和π键的个数比为
(5)FeCl3熔点282℃,而FeCl2熔点674℃,二者熔点差异的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某种水性钠离子电池电极材料属于配位化合物,使用过程中电极 嵌入或脱嵌,变化如下:
嵌入或脱嵌,变化如下: ,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略
,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略 的晶胞示意图如图1,嵌入和脱嵌过程中
的晶胞示意图如图1,嵌入和脱嵌过程中 均填充在小立方体的体心,X为三种晶体中的其中一种,如果不考虑
均填充在小立方体的体心,X为三种晶体中的其中一种,如果不考虑 ,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示:
,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示:

回答下列问题:
(1)原子中电子有两种自旋状态,可分别用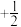 和
和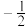 表示,称为电子的自旋磁量子数。则
表示,称为电子的自旋磁量子数。则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为_______ ;从结构上分析基态 、
、 ,
,_______ 更稳定,原因是_______ 。
(2)配位化合物X中,N原子的杂化类型是_______ , 的配位数是
的配位数是_______ ,X中 键和
键和 键的数目之比为
键的数目之比为_______ 。
(3)脱嵌过程该电极发生_______ 反应(填“氧化”或“还原”),作_______ 极(填“阴”或“阳”);格林绿、普鲁士蓝、普鲁士白的化学式可用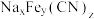 表示,后两者的化学式依次是
表示,后两者的化学式依次是_______ 、_______ 。
 嵌入或脱嵌,变化如下:
嵌入或脱嵌,变化如下: ,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略
,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略 的晶胞示意图如图1,嵌入和脱嵌过程中
的晶胞示意图如图1,嵌入和脱嵌过程中 均填充在小立方体的体心,X为三种晶体中的其中一种,如果不考虑
均填充在小立方体的体心,X为三种晶体中的其中一种,如果不考虑 ,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示:
,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示:
回答下列问题:
(1)原子中电子有两种自旋状态,可分别用
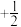 和
和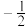 表示,称为电子的自旋磁量子数。则
表示,称为电子的自旋磁量子数。则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为 、
、 ,
,(2)配位化合物X中,N原子的杂化类型是
 的配位数是
的配位数是 键和
键和 键的数目之比为
键的数目之比为(3)脱嵌过程该电极发生
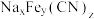 表示,后两者的化学式依次是
表示,后两者的化学式依次是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】在下列各题的横线上选择正确选项(A.“>”、B.“<”、C.“=”、D.“不确定”)。
(1)键能:
___________ Cl-Cl。
(2)分子极性:H2O___________ CH4。
(3)硬度:Si___________ SiC。
(4)键角:SO2___________ SO3。
(5)最外层电子数:B___________ Mn。
(6)熔沸点:MgO___________ NaCl。
(7)单电子数:Cr___________ Co。
(8)酸性:H3AsO4___________ H3AsO3。
(9)与NaOH反应中和热:HAc___________ HCl。
(10)晶体中阳离子配位数:CaF2___________ NaCl。
(11)晶胞空间利用率:Na___________ K。
(12)中心原子孤电子对:SO2___________ XeF2。
(13)第一电离能:I1(S)___________ I1(P)。
(14)分解温度:MgCO3___________ BaCO3。
(15)配位数:Mg___________ Cu。
(1)键能:

(2)分子极性:H2O
(3)硬度:Si
(4)键角:SO2
(5)最外层电子数:B
(6)熔沸点:MgO
(7)单电子数:Cr
(8)酸性:H3AsO4
(9)与NaOH反应中和热:HAc
(10)晶体中阳离子配位数:CaF2
(11)晶胞空间利用率:Na
(12)中心原子孤电子对:SO2
(13)第一电离能:I1(S)
(14)分解温度:MgCO3
(15)配位数:Mg
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的两种元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)X与L形成的常见阴离子的电子式为____________________ 。
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,用电子式表示A的形成过程______ ,B的结构式_______________________ 。
(3)硒是人体必须的微量元素,与L同一主族,硒原子比L原子多两个电子层,则硒在周期表的位置为_______________ ,其最高价氧化物水化物的化学式为_____________ 。
(1)X与L形成的常见阴离子的电子式为
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,用电子式表示A的形成过程
(3)硒是人体必须的微量元素,与L同一主族,硒原子比L原子多两个电子层,则硒在周期表的位置为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】分析核电荷数为1 ~ 18的元素原子的核外电子层数和最外层电子数,回答下列问题:
(1)核电荷数为6和14的元素原子,它们的____________ 相同,____________ 不相同;核电荷数为15和16的元素原子,它们的____________ 相同,____________ 不相同;核电荷数为10和18的元素原子,它们的最外层电子数均为____________ ,它们的元素符号分别是____________ 、____________ 。
(2)某元素的原子核外有三个电子层,最外层电子数是核外电子总数的 ,该元素的元素符号是
,该元素的元素符号是____________ ,原子结构示意图是____________ 。
(1)核电荷数为6和14的元素原子,它们的
(2)某元素的原子核外有三个电子层,最外层电子数是核外电子总数的
 ,该元素的元素符号是
,该元素的元素符号是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】有A、B、C、D、E五种单原子微粒:①当A微粒失去3个电子后,电子层结构与氖原子的相同;②B微粒得到一个电子后,其电子层结构与氩原子相同;③C微粒带两个单位正电荷,核电荷数为12;④D微粒有18个电子,带两个单位负电荷;⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)D元素和E元素形成的化合物的电离方程式为___ 。
(2)B元素和C元素形成的化合物是___ 化合物(填“离子”或“共价”),该化合物的电子式为___ 。
(3)A和B原子间通过___ 键(填“离子”或“共价”)结合成___ 化合物。
(4)B与E原子形成的化合物的电子式为___ 。
(1)D元素和E元素形成的化合物的电离方程式为
(2)B元素和C元素形成的化合物是
(3)A和B原子间通过
(4)B与E原子形成的化合物的电子式为
您最近一年使用:0次



