有A、B、C、D、E五种单原子微粒:①当A微粒失去3个电子后,电子层结构与氖原子的相同;②B微粒得到一个电子后,其电子层结构与氩原子相同;③C微粒带两个单位正电荷,核电荷数为12;④D微粒有18个电子,带两个单位负电荷;⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)D元素和E元素形成的化合物的电离方程式为___ 。
(2)B元素和C元素形成的化合物是___ 化合物(填“离子”或“共价”),该化合物的电子式为___ 。
(3)A和B原子间通过___ 键(填“离子”或“共价”)结合成___ 化合物。
(4)B与E原子形成的化合物的电子式为___ 。
(1)D元素和E元素形成的化合物的电离方程式为
(2)B元素和C元素形成的化合物是
(3)A和B原子间通过
(4)B与E原子形成的化合物的电子式为
20-21高二上·上海·课时练习 查看更多[1]
(已下线)9.2 元素周期表-2020-2021学年秋季班高二上学期化学教材知识点精讲练(沪科版)
更新时间:2021-09-09 18:51:56
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】根据题目要求填空:
(1)Mg2+的结构示意图为__________ ;Cl的结构示意图___________ ,O的电子式为____________ ; S2-的电子式为_____________ 。
(2)氯化钠溶于水发生电离的电离方程式为________________ 。
(1)Mg2+的结构示意图为
(2)氯化钠溶于水发生电离的电离方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】填空
(1)写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)用电子式表示NaCl的形成过程___________ 。
(1)写出
 在水中的电离方程式
在水中的电离方程式(2)用电子式表示NaCl的形成过程
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:非金属元素在生产生活中扮演着重要角色。石英、焦炭在高温的氮气流中发生反应: 。
。
(1)该反应的还原剂是_______ ,反应所涉及的元素中,非金属性最强的是_______ ;硅元素在元素周期表中的位置_________________ ,N2的电子式是________________ 。
(2)氮化硅(Si3N4)是一种性能优异的无机非金属材料,Si3N4中氮元素的化合价为_____ ;SiO2是一种酸性氧化物,与NaOH溶液反应的离子方程式为_____________ 。
 。
。(1)该反应的还原剂是
(2)氮化硅(Si3N4)是一种性能优异的无机非金属材料,Si3N4中氮元素的化合价为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】I.在1~18号元素中,回答下列问题,答案要求写出化学式。
(1)最高价氧化物的水化物碱性最强的物质是______________ ,最高价氧化物的水化物酸性最强的物质是______________ ,气态氢化物最稳定的是______________ 。
Ⅱ.已知X、Y、Z是三种短周期元素,且原子序数按X、Y、Z的顺序依次增大,且原子序数之和为33,最外层电子数之和为11,在周期表中,X、Z上下相邻,Y、Z左右相邻。
(2)X、Y、Z的元素符号分别为___________ 、___________ 、___________ 。
(3)X和Z分别能与氧形成XO2和ZO2,XO2在固态时属于___________ 晶体,ZO2在固态时属于___________ 晶体。
(1)最高价氧化物的水化物碱性最强的物质是
Ⅱ.已知X、Y、Z是三种短周期元素,且原子序数按X、Y、Z的顺序依次增大,且原子序数之和为33,最外层电子数之和为11,在周期表中,X、Z上下相邻,Y、Z左右相邻。
(2)X、Y、Z的元素符号分别为
(3)X和Z分别能与氧形成XO2和ZO2,XO2在固态时属于
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下面是A~G七种元素的电子排布:
试根据由上述元素构成的物质的化学式回答下列问题。
(1)写出一种常见的由非极性键形成的双原子分子:____________________ 。
(2)写出一种由极性键形成的双原子分子:____________________ 。
(3)写出一种由极性键形成的三原子分子:____________________ 。
(4)写出一种由三种元素形成的既含离子键又含共价键的化合物:__________ ,其电子式为____________________ 。
(5)写出一种既含离子键又含非极性键的化合物:__________ ,其电子式为__________ 。
元素 电子排布 电子层 | A | B | C | D | E | F | G |
K | 1 | 2 | 2 | 2 | 2 | 2 | 2 |
L | 4 | 5 | 6 | 8 | 8 | 8 | |
M | 1 | 3 | 7 |
试根据由上述元素构成的物质的化学式回答下列问题。
(1)写出一种常见的由非极性键形成的双原子分子:
(2)写出一种由极性键形成的双原子分子:
(3)写出一种由极性键形成的三原子分子:
(4)写出一种由三种元素形成的既含离子键又含共价键的化合物:
(5)写出一种既含离子键又含非极性键的化合物:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】有A、B、C、D四种元素,已知A元素原子的K层和M层电子数相同;B元素原子的L层比K层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的最外层电子数是次外层电子数的3倍。
(1)写出元素符号:A________ ,D________ 。
(2)A的原子结构示意图_______________ ,B的离子结构示意图______________ ,C的离子结构示意图______________________ 。
(3)D原子的电子式________________ 。
(4)A和B元素组成的物质的化学式为________ ,它是由________ (选填“原子”、“离子”或“分子”)构成的物质。
(5)由C和D可组成CD2-离子,一个CD2-离子所带电子数为________ 。
(1)写出元素符号:A
(2)A的原子结构示意图
(3)D原子的电子式
(4)A和B元素组成的物质的化学式为
(5)由C和D可组成CD2-离子,一个CD2-离子所带电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)比较下列粒子的半径大小
①Na Mg O F__________
②Na+ Mg2+ O2- F-__________
③Fe Fe2+ Fe3+__________
④Na+ Mg2+ S2- Cl-__________
(2)下列物质中:只存在共价键的是__________ (填序号,下同),只存在离子键的是__________ ,既存在离子键又存在极性共价键的是__________ ,既存在离子键又存在非极性共价键的是__________ 。
①Ar ②CO2③Na2O2 ④KOH ⑤MgBr2⑥NH4Cl ⑦CaO ⑧H2SO4
(3)氢气可由天然气和水反应制备,其主要反应为:CH4(g)+ 2H2O(g) ===CO2(g)+4H2(g) 反应过程中能量变化如图所示,则该反应为__________ 反应(填“吸热”或“放热”)。若已知,破坏1mol化学键需要吸收的热量如代数式表示:
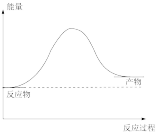
则根据该反应制取1mol H2要吸收或放出热量为___________ kJ(用含a、b、c、d字母表示)。
①Na Mg O F
②Na+ Mg2+ O2- F-
③Fe Fe2+ Fe3+
④Na+ Mg2+ S2- Cl-
(2)下列物质中:只存在共价键的是
①Ar ②CO2③Na2O2 ④KOH ⑤MgBr2⑥NH4Cl ⑦CaO ⑧H2SO4
(3)氢气可由天然气和水反应制备,其主要反应为:CH4(g)+ 2H2O(g) ===CO2(g)+4H2(g) 反应过程中能量变化如图所示,则该反应为
| 化学键 | C—H | O—H | C=O | H—H |
| 吸收热量(kJ/mol) | a | b | c | d |

则根据该反应制取1mol H2要吸收或放出热量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)请用下列4种物质的序号填空:
①O2 ②NH4NO3 ③K2O2 ④NH3,既有离子键又有非极性键的是________ 。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为____________________ 。
(3)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃(2.02×105 Pa),但在180℃就开始升华。据此判断,氯化铝是________ (填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是_________________________________________ 。
(4)现有a~g 7种短周期元素,它们在元素周期表中的位置如图,请据此回答下列问题:

①元素的原子间反应最容易形成离子键的是________ 。
A.c和f B.b和g
C.d和g D.b和e
②d与g元素形成的分子中所有原子________ (填“是”或“不是”)都满足最外层为8电子结构。
①O2 ②NH4NO3 ③K2O2 ④NH3,既有离子键又有非极性键的是
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为
(3)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃(2.02×105 Pa),但在180℃就开始升华。据此判断,氯化铝是
(4)现有a~g 7种短周期元素,它们在元素周期表中的位置如图,请据此回答下列问题:

①元素的原子间反应最容易形成离子键的是
A.c和f B.b和g
C.d和g D.b和e
②d与g元素形成的分子中所有原子
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】用电子式表示下列化合物:
(1)NaCl_____ 。
(2)H2______ 。
(3)MgCl2______ 。
(4)CH4______ 。
(5)CO2______ 。
(6)Na2O______ 。
把其中只含共价键的物质的电子式改成结构式:______ 、 ______ 、 ______ 。
(1)NaCl
(2)H2
(3)MgCl2
(4)CH4
(5)CO2
(6)Na2O
把其中只含共价键的物质的电子式改成结构式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在下列化合物中:H2O、Na2O、I2、NaCl、KOH、CO2、NH4Cl、Na2O2,请填空:
(1)含有极性共价键的离子化合物有___________ 。
(2)请写出Na2O2的电子式__________ 。
(1)含有极性共价键的离子化合物有
(2)请写出Na2O2的电子式
您最近一年使用:0次



