如下图所示,此装置可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。填写下列空白:
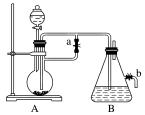
(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是_______ 。A中反应的离子方程式是_______ 。
(2)实验开始时先将止水夹a_______ (填“打开”或“关闭”)。
(3)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生反应的化学方程式为_______ 。

(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是
(2)实验开始时先将止水夹a
(3)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中发生反应的化学方程式为
更新时间:2022-12-08 18:54:39
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入___________ 。
(2)除去蒸馏水中溶解的O2常采用___________ 的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是___________ 。
(4)生成的白色Fe(OH)2沉淀遇空气后发生反应的化学方程式为:___________ 。
方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。

(1)在试管I里加入的试剂是___________ 。
(2)在试管Ⅱ里加入的试剂是___________ 。
(3)为了制得白色Fe(OH)2沉淀,在试管I和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是___________ 。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入
(2)除去蒸馏水中溶解的O2常采用
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是
(4)生成的白色Fe(OH)2沉淀遇空气后发生反应的化学方程式为:
方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。

(1)在试管I里加入的试剂是
(2)在试管Ⅱ里加入的试剂是
(3)为了制得白色Fe(OH)2沉淀,在试管I和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】两同学为制得纯净的Fe(OH)2,使用如图所示的装置,用NaOH溶液、铁粉、稀H2SO4试剂制备。
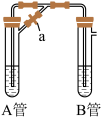
(1)试管A里装的试剂是___________ 。
(2)试管B里装的试剂是___________ 。
(3)同学甲:加入试剂后,先夹紧止水夹a,开始反应,在B试管中观察到的现象是___________ 。
(4)同学乙:打开止水夹a,使A管中反应一段时间后,再夹紧止水夹a,实验中在B管中观察到的现象是___________ ,B中发生反应的离子方程式为___________ 。
(5)这样的Fe(OH)2沉淀能较长时间保持白色,其理由是___________ 。
(6)反应结束,若打开B试管橡皮塞一段时间后,观察到的现象是___________ ,其化学方程式为___________ 。

(1)试管A里装的试剂是
(2)试管B里装的试剂是
(3)同学甲:加入试剂后,先夹紧止水夹a,开始反应,在B试管中观察到的现象是
(4)同学乙:打开止水夹a,使A管中反应一段时间后,再夹紧止水夹a,实验中在B管中观察到的现象是
(5)这样的Fe(OH)2沉淀能较长时间保持白色,其理由是
(6)反应结束,若打开B试管橡皮塞一段时间后,观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】氢氧化亚铁在空气中很容易被氧化而变质,制备时须严格控制条件。如图所示,此装置可用来制备 并验证其还原性,填写下列空白:
并验证其还原性,填写下列空白:___________ 。
(2)本实验的关键之处是巧妙控制止水夹a的开与关——实验开始前,应___________ (填“打开”或“关闭”)止水夹a,待到导管Y出口处气体纯度较高时,可立即___________ (填“打开”或“关闭”)止水夹a。
(3)检验反应后圆底烧瓶中是否有 生成所需试剂为
生成所需试剂为___________ 。
(4)实验完毕,B瓶中产生 ,为验证其还原性,打开b处止水夹,充入一段时间空气,此时B瓶中发生的反应为
,为验证其还原性,打开b处止水夹,充入一段时间空气,此时B瓶中发生的反应为___________ (写化学方程式),现象:___________ 。
 并验证其还原性,填写下列空白:
并验证其还原性,填写下列空白: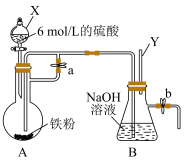
(2)本实验的关键之处是巧妙控制止水夹a的开与关——实验开始前,应
(3)检验反应后圆底烧瓶中是否有
 生成所需试剂为
生成所需试剂为(4)实验完毕,B瓶中产生
 ,为验证其还原性,打开b处止水夹,充入一段时间空气,此时B瓶中发生的反应为
,为验证其还原性,打开b处止水夹,充入一段时间空气,此时B瓶中发生的反应为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】以黄铜矿(CuFeS2)为主要原料的炼铜方法有火法炼铜、氧化浸出、生物浸出、配位浸出、电化学浸出法等。
Ⅰ.火法炼铜:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2 ΔH<0
8Cu+4FeO+2Fe2O3+16SO2 ΔH<0
(1)反应中被氧化的元素是________________ (填元素符号)。
(2)实际生产是在沸腾炉中进行,反应温度为 600~620℃。控制反应温度的方法是________________ 。
(3)冶炼过程中产生大量SO2,下列处理方案中合理的是________ (填字母)。
A.高空排放 B.制备硫酸
C.用纯碱溶液吸收制Na2SO3 D.用浓硫酸吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有 生成。
生成。
(4)配平该反应方程式:___ CuFeS2+___ H2O2+___ H+
___ Cu2++___ Fe3++___  +
+___ H2O。
(5)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是__________________________________________________ 。
Ⅲ.生物浸出:
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
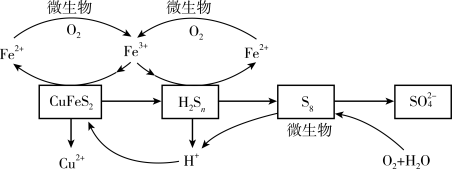
(6)在微生物的作用下,可以循环使用的物质有_________ (填化学式)。
(7)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2 mol 生成时,理论上消耗O2的物质的量为
生成时,理论上消耗O2的物质的量为_______________________ 。
Ⅰ.火法炼铜:8CuFeS2+21O2
 8Cu+4FeO+2Fe2O3+16SO2 ΔH<0
8Cu+4FeO+2Fe2O3+16SO2 ΔH<0(1)反应中被氧化的元素是
(2)实际生产是在沸腾炉中进行,反应温度为 600~620℃。控制反应温度的方法是
(3)冶炼过程中产生大量SO2,下列处理方案中合理的是
A.高空排放 B.制备硫酸
C.用纯碱溶液吸收制Na2SO3 D.用浓硫酸吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有
 生成。
生成。(4)配平该反应方程式:

 +
+(5)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是
Ⅲ.生物浸出:
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。

(6)在微生物的作用下,可以循环使用的物质有
(7)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2 mol
 生成时,理论上消耗O2的物质的量为
生成时,理论上消耗O2的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4·7H2O),流程如下:
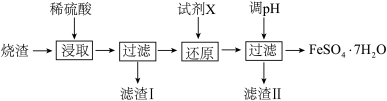
(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为__________________ 。能提高烧渣浸取速率的措施有__________________ (填字母)。
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
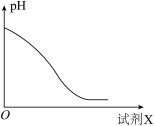
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是________ (填字母)。还原结束时,溶液中的主要阴离子有_____________ 。
A.Fe粉 B.SO2 C.NaI
(3)滤渣Ⅱ主要成分的化学式为__________________ ;由分离出滤渣Ⅱ后的溶液得到产品,进行的操作是_______________________________ 、过滤、洗涤、干燥。

(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是
A.Fe粉 B.SO2 C.NaI

(3)滤渣Ⅱ主要成分的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】轻质碳酸钙广泛应用于橡胶、塑料、油漆,水性涂料以及造纸等行业,日常生活中的牙膏也常用它作摩擦剂。目前轻质碳酸钙的生产主要用碳化法,工艺流程如图所示:
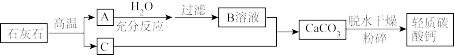
请分析轻质碳酸钙的生产流程,回答下列问题:
(1)B的化学式为_______ 。
(2)在A→B溶液的过程中,过滤操作的目的是_________ 。
(3)在B溶液+C→CaCO3的过程中,应控制C的量,原因是_________ (用化学方程式表示)。
(4)生产轻质碳酸钙的方法很多,请再设计一种制备方法________ (用化学方程式表示)。
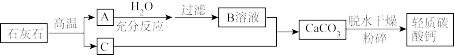
请分析轻质碳酸钙的生产流程,回答下列问题:
(1)B的化学式为
(2)在A→B溶液的过程中,过滤操作的目的是
(3)在B溶液+C→CaCO3的过程中,应控制C的量,原因是
(4)生产轻质碳酸钙的方法很多,请再设计一种制备方法
您最近一年使用:0次



