碘化钾和碘酸钾(KIO3)在食品工业中常用作营养增补剂(碘值强化剂),我国从1994年起在食盐中添加碘酸钾作为补碘剂。
(1)为检验某食盐中所加碘强化剂是碘化钾或碘酸钾,现进行分步实验:
已知:Ⅰ.氧化性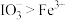 ;
;
Ⅱ.实验中可选用的试剂有:FeCl3溶液、FeSO4溶液、淀粉溶液
①补充完整检验食盐中是否含有I-的实验方案:取少量食盐,加水溶解,_______ 。
②补充完整检验食盐中是否含有 的实验方案:取少量食盐,加水溶解,
的实验方案:取少量食盐,加水溶解,_______ 。
(2)工业可用“氯酸钾氧化法”分两步制备KIO3,其中第一步反应方程式为: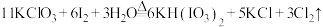
①用单线桥表示该反应电子转移的方向和数目:_______ 。
②每生成标准状况下11.2LCl2,反应转移电子的物质的量是_______ 。
③第二步反应时应向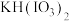 中加入的物质是
中加入的物质是_______ 。
(1)为检验某食盐中所加碘强化剂是碘化钾或碘酸钾,现进行分步实验:
已知:Ⅰ.氧化性
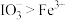 ;
;Ⅱ.实验中可选用的试剂有:FeCl3溶液、FeSO4溶液、淀粉溶液
①补充完整检验食盐中是否含有I-的实验方案:取少量食盐,加水溶解,
②补充完整检验食盐中是否含有
 的实验方案:取少量食盐,加水溶解,
的实验方案:取少量食盐,加水溶解,(2)工业可用“氯酸钾氧化法”分两步制备KIO3,其中第一步反应方程式为:
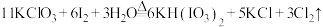
①用单线桥表示该反应电子转移的方向和数目:
②每生成标准状况下11.2LCl2,反应转移电子的物质的量是
③第二步反应时应向
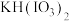 中加入的物质是
中加入的物质是
22-23高一上·江苏南通·期中 查看更多[3]
(已下线)江苏省南通市如皋市2022-2023学年高一上学期期中教学质量调研化学试题江苏省盐城市射阳县第二中学2022-2023学年高一上学期11月期中考试化学试题江苏省南京市第九中学2023-2024学年高一上学期10月阶段学情调研化学试题
更新时间:2022-12-22 23:29:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)用双线桥分析下述氧化还原反应中电子转移的方向和数目以及氧化还原的关系,并指出氧化剂。Cu+2AgNO3=Cu(NO3)2+2Ag____________________ ,氧化剂是____________________ 。
(2)用单线桥分析下述氧化还原反应中电子转移的方向和数目,并完成填空。
2NaBr+Cl2=Br2+2NaCl______________________ ,氧化产物和还原产物的物质的量之比为__________ 。
(2)用单线桥分析下述氧化还原反应中电子转移的方向和数目,并完成填空。
2NaBr+Cl2=Br2+2NaCl
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用双线桥标出下列氧化还原反应中电子转移的方向和数目
①5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O
_______________________________________________
②I2+SO2+2H2O=2HI+H2SO4
___________________________________________
③2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O
_______________________________________
①5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O
②I2+SO2+2H2O=2HI+H2SO4
③2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
(1)Na2FeO4中铁元素的化合价是______ 价,Na2FeO4能给水消毒利用的是________ 性。
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原理是______________ (用简要的文字叙述)。
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,配平反应的离子方程式:_____Fe3+ +_____OH-+____ClO- =_____FeO42-+ _____ + ______Cl- ,
+ ______Cl- ,____________ 氧化剂为________ ,若反应过程中转移了0.5 mol电子,则还原产物的物质的量为________ mol。
(1)Na2FeO4中铁元素的化合价是
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原理是
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,配平反应的离子方程式:_____Fe3+ +_____OH-+____ClO- =_____FeO42-+ _____
 + ______Cl- ,
+ ______Cl- ,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空
(1)在S2-、Fe2+、Fe、Mg2+、H2S、I-、H+中,既有氧化性又有还原性的是________ 。
(2)实验室可用以下反应制备氯气:KClO3+6HCl(浓)= KCl+ 3Cl2↑+3H2O。反应中有1 mol电子转移时制得氯气44g,则反应物可能的组合是_______________
A.K35ClO3+6H35Cl B.K35ClO3+6H37Cl
C.K37ClO3+6H35Cl D.K37ClO3+6H37Cl
(3)将57.6 g的Cu片加入50 mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为_________ (填“>”、“=”、“<”)0.45 mol
(4)火箭发射时以肼(N2H4)为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为_______ 。
(5)已知溶液中含有以下离子: 、
、 、
、 、
、 、
、 、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是___________ 。
(1)在S2-、Fe2+、Fe、Mg2+、H2S、I-、H+中,既有氧化性又有还原性的是
(2)实验室可用以下反应制备氯气:KClO3+6HCl(浓)= KCl+ 3Cl2↑+3H2O。反应中有1 mol电子转移时制得氯气44g,则反应物可能的组合是
A.K35ClO3+6H35Cl B.K35ClO3+6H37Cl
C.K37ClO3+6H35Cl D.K37ClO3+6H37Cl
(3)将57.6 g的Cu片加入50 mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为
(4)火箭发射时以肼(N2H4)为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为
(5)已知溶液中含有以下离子:
 、
、 、
、 、
、 、
、 、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】淀粉和纤维素是常见的多糖,在一定条件下它们都可以水解生成葡萄糖。
(1)淀粉在浓硫酸作用下水解生成葡萄糖的化学方程式为___________ 。
(2)某学生设计了如下实验方案用以检验淀粉水解的情况:

下列结论正确的是_______ 。
A.淀粉尚有部分未水解 B.淀粉已完全水解
C.淀粉没有水解 D.淀粉已水解,但不知是否完全水解
(3)一种测定饮料中糖类物质含量(所有糖类物质以葡萄糖计算)的方法如下:
取某无色饮料20.00mL加入稀硫酸煮沸,充分反应后,冷却,加入适量的氢氧化钠溶液并稀释至100.00mL。取10. 00mL稀释液,加入30. 00mL0. 0150mol/L标准溶液,置于暗处15分钟。然后滴加2 ~3滴淀粉溶液作指示剂,再用0.01200mol/LNa2S2O3标准溶液滴定反应所剩余的I2,当溶液由蓝色变为无色且半分钟不变时,反应达到终点,共消耗Na2S2O3标推溶液25. 00mL。已知:
a.I2在碱性条件下能与葡萄糖反应:C6H12O6 +I2 +3NaOH=C6H11O7Na +2NaI+ 2H2O
b. Na2S2O3与I2能发牛如下反应:I2 +2Na2S2O3=2NaI + Na2S4O6
①配制100.00mL0.01500mol/LI2标准溶液,所必需的玻璃仪器有烧杯、玻璃棒、胶头滴管和____ 。
②向饮料中加入稀硫酸并充分煮沸的目的是___________ 。
③计算该饮料中糖类物质的含量(单位mg/mL)(写出计算过程)。______________________ 。
(1)淀粉在浓硫酸作用下水解生成葡萄糖的化学方程式为
(2)某学生设计了如下实验方案用以检验淀粉水解的情况:

下列结论正确的是
A.淀粉尚有部分未水解 B.淀粉已完全水解
C.淀粉没有水解 D.淀粉已水解,但不知是否完全水解
(3)一种测定饮料中糖类物质含量(所有糖类物质以葡萄糖计算)的方法如下:
取某无色饮料20.00mL加入稀硫酸煮沸,充分反应后,冷却,加入适量的氢氧化钠溶液并稀释至100.00mL。取10. 00mL稀释液,加入30. 00mL0. 0150mol/L标准溶液,置于暗处15分钟。然后滴加2 ~3滴淀粉溶液作指示剂,再用0.01200mol/LNa2S2O3标准溶液滴定反应所剩余的I2,当溶液由蓝色变为无色且半分钟不变时,反应达到终点,共消耗Na2S2O3标推溶液25. 00mL。已知:
a.I2在碱性条件下能与葡萄糖反应:C6H12O6 +I2 +3NaOH=C6H11O7Na +2NaI+ 2H2O
b. Na2S2O3与I2能发牛如下反应:I2 +2Na2S2O3=2NaI + Na2S4O6
①配制100.00mL0.01500mol/LI2标准溶液,所必需的玻璃仪器有烧杯、玻璃棒、胶头滴管和
②向饮料中加入稀硫酸并充分煮沸的目的是
③计算该饮料中糖类物质的含量(单位mg/mL)(写出计算过程)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出A中反应的化学方程式为_______ 。装置B的作用是_______


您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某同学设计下图所示装置,用粗铁粒与189g·L-1硝酸反应制取NO气体。

完全反应后,A装置烧杯里含铁的价态可能是________________ 。
现有仪器和药品:试管和胶头滴管,0.1mol·L-1KSCN溶液、0.1mol·L-1KI溶液、0.2mol·L-1酸性KMnO4溶液、氯水等。
请你设计一个简单实验,探究上述判断,填写下列实验报告:

完全反应后,A装置烧杯里含铁的价态可能是
现有仪器和药品:试管和胶头滴管,0.1mol·L-1KSCN溶液、0.1mol·L-1KI溶液、0.2mol·L-1酸性KMnO4溶液、氯水等。
请你设计一个简单实验,探究上述判断,填写下列实验报告:
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量溶液装于试管,向试管中滴入几滴KSCN溶液 | |
| 第二步 | 若溶液紫色退去,则说明含有Fe2+,若无明显变化,则说明不含Fe2+ |
您最近一年使用:0次




