以下有十种物质:①氨水 ②稀硫酸 ③氯化氢 ④ ⑤蔗糖 ⑥二氧化碳 ⑦石墨 ⑧熔融氯化钠 ⑨氢氧化钠 ⑩碳酸钙,请回答下列问题:
⑤蔗糖 ⑥二氧化碳 ⑦石墨 ⑧熔融氯化钠 ⑨氢氧化钠 ⑩碳酸钙,请回答下列问题:
(1)属于混合物的是_______ ;
(2)属于电解质,但熔融状态下不导电的是_______ ;
(3)属于电解质,且难溶于水的是_______ ;
(4)属于化合物,但不是电解质的是_______ ;
(5)不是电解质,但可以导电的是_______ ;
(6)上述物质中有两种物质之间可发生离子反应: ,该离子反应对应的化学方程式为
,该离子反应对应的化学方程式为_______ 、_______ ;
 ⑤蔗糖 ⑥二氧化碳 ⑦石墨 ⑧熔融氯化钠 ⑨氢氧化钠 ⑩碳酸钙,请回答下列问题:
⑤蔗糖 ⑥二氧化碳 ⑦石墨 ⑧熔融氯化钠 ⑨氢氧化钠 ⑩碳酸钙,请回答下列问题:(1)属于混合物的是
(2)属于电解质,但熔融状态下不导电的是
(3)属于电解质,且难溶于水的是
(4)属于化合物,但不是电解质的是
(5)不是电解质,但可以导电的是
(6)上述物质中有两种物质之间可发生离子反应:
 ,该离子反应对应的化学方程式为
,该离子反应对应的化学方程式为
更新时间:2022-12-18 16:48:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化。从下列8种物质中按要求回答问题:
① ②液态氯化氢③
②液态氯化氢③ ④熔融氢氧化钠⑤
④熔融氢氧化钠⑤ 固体⑥氯化钠溶液⑦浓硝酸⑧单质铁
固体⑥氯化钠溶液⑦浓硝酸⑧单质铁
(1)以上物质中能导电的是___________ (填序号)属于电解质的是___________ (填序号);属于非电解质的是___________ (填序号)
(2)④的电离方程式为___________ ;
(3)已知 和
和 均为酸性氧化物,根据类别转换思维写出
均为酸性氧化物,根据类别转换思维写出 与NaOH溶液反应的化学方程式
与NaOH溶液反应的化学方程式___________ 。
(4)向沸水中逐滴滴加饱和 溶液,至液体呈透明的红褐色,用激光侧面照射,在垂直与光线的方向看到光亮的通路,则该分散系中分散质粒子直径的范围是
溶液,至液体呈透明的红褐色,用激光侧面照射,在垂直与光线的方向看到光亮的通路,则该分散系中分散质粒子直径的范围是___________ nm。
①
 ②液态氯化氢③
②液态氯化氢③ ④熔融氢氧化钠⑤
④熔融氢氧化钠⑤ 固体⑥氯化钠溶液⑦浓硝酸⑧单质铁
固体⑥氯化钠溶液⑦浓硝酸⑧单质铁(1)以上物质中能导电的是
(2)④的电离方程式为
(3)已知
 和
和 均为酸性氧化物,根据类别转换思维写出
均为酸性氧化物,根据类别转换思维写出 与NaOH溶液反应的化学方程式
与NaOH溶液反应的化学方程式(4)向沸水中逐滴滴加饱和
 溶液,至液体呈透明的红褐色,用激光侧面照射,在垂直与光线的方向看到光亮的通路,则该分散系中分散质粒子直径的范围是
溶液,至液体呈透明的红褐色,用激光侧面照射,在垂直与光线的方向看到光亮的通路,则该分散系中分散质粒子直径的范围是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】①Cu ②CO2 ③Fe2O3 ④液氨 ⑤液态CH3COOH ⑥熔融Ba(OH)2 ⑦蔗糖 ⑧NaOH溶液 ⑨冰水混合物 ⑩固体CaCO3
(1)上述物质中属于电解质的是_______ (填序号,下同),属于非电解质是_______ ,既是电解质又能导电的是_________ 。
(2)常温下,②⑨⑩这三种物质相互作用可生成一种新物质Ca(HCO3)2,该反应_______ (“是”或“不是”)氧化还原反应。
(3)写出下列反应的离子方程式
A.物质③与足量稀硫酸溶液反应的离子方程式:________________________________ 。
B.物质⑩与足量⑤溶液反应的离子方程式:_________________________________ 。
C.足量的NaHCO3溶液与少量Ca(OH)2的溶液反应_______________________________ 。
(1)上述物质中属于电解质的是
(2)常温下,②⑨⑩这三种物质相互作用可生成一种新物质Ca(HCO3)2,该反应
(3)写出下列反应的离子方程式
A.物质③与足量稀硫酸溶液反应的离子方程式:
B.物质⑩与足量⑤溶液反应的离子方程式:
C.足量的NaHCO3溶液与少量Ca(OH)2的溶液反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】高铁酸钾(① )是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于②水而形成暗紫色溶液,静置后会分解并释放出大量③氧气,同时生成④KOH和⑤
)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于②水而形成暗紫色溶液,静置后会分解并释放出大量③氧气,同时生成④KOH和⑤ 。高铁酸钾具有很强的氧化能力,可以处理池塘塘底泥生成的⑥
。高铁酸钾具有很强的氧化能力,可以处理池塘塘底泥生成的⑥ 、⑦
、⑦ 等。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法。
等。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法。
(1)在上述有标号的物质中,属于电解质的是_______ (填标号,下同),属于酸的是_______ ,属于盐的是_______ 。
(2)电解法:通过电解得到 ,然后向
,然后向 溶液中加入适量饱和KOH溶液,沉淀结晶,过滤得到较纯的
溶液中加入适量饱和KOH溶液,沉淀结晶,过滤得到较纯的 固体。“沉淀结晶”的离子方程式为
固体。“沉淀结晶”的离子方程式为_______ 。
(3)次氯酸盐氧化法: _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。
。
①请配平上述离子方程式____ 。
②上述反应中的还原剂为_______ ,氧化性:
_______ (填“大于”或“小于”) 。
。
(4)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠:
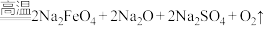 ,再加入适量饱和KOH溶液反应得到
,再加入适量饱和KOH溶液反应得到 。
。
①上述反应在熔融状态下进行,而不在水溶液中进行的原因是_______ (用化学方程式表示)。
②每生成3.2g ,理论上被氧化的
,理论上被氧化的 的质量为
的质量为_______ g。
 )是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于②水而形成暗紫色溶液,静置后会分解并释放出大量③氧气,同时生成④KOH和⑤
)是一种高效多功能的新型非氯绿色消毒剂,为暗紫色有光泽粉末,极易溶于②水而形成暗紫色溶液,静置后会分解并释放出大量③氧气,同时生成④KOH和⑤ 。高铁酸钾具有很强的氧化能力,可以处理池塘塘底泥生成的⑥
。高铁酸钾具有很强的氧化能力,可以处理池塘塘底泥生成的⑥ 、⑦
、⑦ 等。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法。
等。工业上常用于制备高铁酸钾的方法有电解法、次氯酸盐氧化法和熔融法。(1)在上述有标号的物质中,属于电解质的是
(2)电解法:通过电解得到
 ,然后向
,然后向 溶液中加入适量饱和KOH溶液,沉淀结晶,过滤得到较纯的
溶液中加入适量饱和KOH溶液,沉淀结晶,过滤得到较纯的 固体。“沉淀结晶”的离子方程式为
固体。“沉淀结晶”的离子方程式为(3)次氯酸盐氧化法:
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。
。①请配平上述离子方程式
②上述反应中的还原剂为

 。
。(4)熔融法:在苛性碱存在的环境中,铁盐被过氧化钠高温氧化成高铁酸钠:

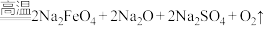 ,再加入适量饱和KOH溶液反应得到
,再加入适量饱和KOH溶液反应得到 。
。①上述反应在熔融状态下进行,而不在水溶液中进行的原因是
②每生成3.2g
 ,理论上被氧化的
,理论上被氧化的 的质量为
的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读下列关于燃料电池的短文并填空。
燃料电池具有能量转化率高、对环境友好等优点。燃料电池在工作时,从负极连续通入①H2、②酒精等燃料,从正极连续通入③O2,二者在电池内部(还有④KOH或⑤H2SO4等物质的溶液)发生反应生成⑥H2O、⑦CO2或⑧K2CO3溶液等,同时产生电能。
(1)在上述短文标有序号的物质中,属于电解质的是___________ (填序号,下同);属于非电解质的是___________ 。O2和O3互为___________ 。
(2)写出上文有序号物质中一种盐的电离方程式___________ 。
(3)少量⑤溶液滴到⑧溶液中的离子方程式___________ ,向⑧溶液中通入⑦的化学方程式___________ 。
(4)Al—空气燃料电池是一种高能电池,其反应原理是:负极的金属Al在氯化钠溶液中与空气中的O2发生反应生成Al(OH)3,若负极有4N个Al参加反应,则消耗O2的个数为___________ N。
燃料电池具有能量转化率高、对环境友好等优点。燃料电池在工作时,从负极连续通入①H2、②酒精等燃料,从正极连续通入③O2,二者在电池内部(还有④KOH或⑤H2SO4等物质的溶液)发生反应生成⑥H2O、⑦CO2或⑧K2CO3溶液等,同时产生电能。
(1)在上述短文标有序号的物质中,属于电解质的是
(2)写出上文有序号物质中一种盐的电离方程式
(3)少量⑤溶液滴到⑧溶液中的离子方程式
(4)Al—空气燃料电池是一种高能电池,其反应原理是:负极的金属Al在氯化钠溶液中与空气中的O2发生反应生成Al(OH)3,若负极有4N个Al参加反应,则消耗O2的个数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列10种物质:①铝 ②蔗糖 ③CO2 ④稀硫酸 ⑤Ba(OH)2固体 ⑥氧气 ⑦HCl ⑧食盐水 ⑨红褐色的氢氧化铁胶体 ⑩熔融CaO
(1)上述物质能导电的是____ (填序号,下同),属于电解质是____ ,属于非电解质的是____ 。
(2)向⑨中逐渐滴加⑦的水溶液,看到的现象是____ 。
(1)上述物质能导电的是
(2)向⑨中逐渐滴加⑦的水溶液,看到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】分类是研究物质性质的重要方法,图中对某些物质进行分类。

回答下列问题:
(1)图2的分类方法是_______ 分类法。
(2)写出 的电离方程式
的电离方程式_______ 。
(3)写出 的电离方程式
的电离方程式_______ 。
(4)写出 与
与 反应的离子方程式
反应的离子方程式_______ ,由该反应可推断 为
为_______ 氧化物(填“酸性”或“碱性”)。
(5)写出 与足量
与足量 反应的离子方程式
反应的离子方程式_______ 。
(6)化合物可以依据水溶液或熔融状态是否导电分为电解质和非电解质。下列物质属于电解质的有_______ (填物质序号下同);下列物质能导电的有_______ 。
①铜 ② 气体 ③
气体 ③ ④
④ 固体 ⑤
固体 ⑤ 固体 ⑥
固体 ⑥ 溶液 ⑦熔融态
溶液 ⑦熔融态

回答下列问题:
(1)图2的分类方法是
(2)写出
 的电离方程式
的电离方程式(3)写出
 的电离方程式
的电离方程式(4)写出
 与
与 反应的离子方程式
反应的离子方程式 为
为(5)写出
 与足量
与足量 反应的离子方程式
反应的离子方程式(6)化合物可以依据水溶液或熔融状态是否导电分为电解质和非电解质。下列物质属于电解质的有
①铜 ②
 气体 ③
气体 ③ ④
④ 固体 ⑤
固体 ⑤ 固体 ⑥
固体 ⑥ 溶液 ⑦熔融态
溶液 ⑦熔融态
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有以下物质:①石墨 ②铁 ③蔗糖(C12H22O11) ④一氧化碳 ⑤氯化铁固体 ⑥硫酸氢钠固体 ⑦氢氧化钡溶液 ⑧纯醋酸 ⑨熔融氯化钠 ⑩液态氯化氢
(1)以上物质属于电解质的是_______ ;能导电的是_______ 。
(2)⑥在水溶液中的电离方程式为_______ 。
(3)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:_______ 。
(4)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸(H3PO2)都是重要的化工产品。已知:磷酸、亚磷酸、次磷酸与其最多消耗NaOH的个数之比依次为1:3;1:2、1:1,则NaH2PO4、NaH2PO2、NaH2PO3中属于正盐的是_______ (填化学式)。
(1)以上物质属于电解质的是
(2)⑥在水溶液中的电离方程式为
(3)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:
(4)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸(H3PO2)都是重要的化工产品。已知:磷酸、亚磷酸、次磷酸与其最多消耗NaOH的个数之比依次为1:3;1:2、1:1,则NaH2PO4、NaH2PO2、NaH2PO3中属于正盐的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下有10种物质:①铜;②醋酸;③盐酸;④液氨;⑤空气;⑥二氧化碳;⑦氨水;⑧碳酸氢钠;⑨熔融的AgCl;⑩氢氧化钡。
(1)按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
(2)写出②⑦⑧在水溶液中的电离方程式(不考虑水的电离)。
②___________ ;⑦___________ ;⑧___________ 。
(1)按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
| 序号 | 符合的条件 | 物质的序号 |
| (1) | 能导电的物质 | |
| (2) | 电解质,但熔融状并不导电 | |
| (3) | 非电解质 | |
| (4) | 强电解质 | |
| (5) | 弱电解质 |
②
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】大气臭氧层可以保护地球生物免受紫外线的伤害,但低空臭氧的浓度过高时对人体有害。
(1)在紫外线作用下,氧气可转化臭氧:
①该反应所属类型为_______ (填“氧化还原”或“非氧化还原”)反应。
②若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为_______ 。
③某区域收集到 和
和 混合气体10g,标准状况下体积为5.6L,其中
混合气体10g,标准状况下体积为5.6L,其中 与
与 的体积之比为
的体积之比为_______ 。
(2)实验室中常用碘量法检测臭氧,其中以淀粉为指示剂,将臭氧通入含有硫酸的碘化钾溶液中进行反应,反应后生成能使带火星的木条复燃的气体,溶液变蓝,则反应的离子方程式为_______ 。
(3)现需450mL 的
的 溶液,用
溶液,用 固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。
固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。
①还缺少的仪器有_______ 、_______ 。
②在配制过程中,下列操作会导致所配制溶液的浓度偏小的是_______ (填字母)。
A.未洗涤烧杯和玻璃棒
B.使用前,容量瓶中有少量蒸馏水
C.定容时俯视凹液面
D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线
(1)在紫外线作用下,氧气可转化臭氧:

①该反应所属类型为
②若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为
③某区域收集到
 和
和 混合气体10g,标准状况下体积为5.6L,其中
混合气体10g,标准状况下体积为5.6L,其中 与
与 的体积之比为
的体积之比为(2)实验室中常用碘量法检测臭氧,其中以淀粉为指示剂,将臭氧通入含有硫酸的碘化钾溶液中进行反应,反应后生成能使带火星的木条复燃的气体,溶液变蓝,则反应的离子方程式为
(3)现需450mL
 的
的 溶液,用
溶液,用 固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。
固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒、细口试剂瓶。①还缺少的仪器有
②在配制过程中,下列操作会导致所配制溶液的浓度偏小的是
A.未洗涤烧杯和玻璃棒
B.使用前,容量瓶中有少量蒸馏水
C.定容时俯视凹液面
D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】物质的分类有多种方法,下列对无机化合物分类如图:

(1)如图所示的物质分类方法的名称是________ 。
(2)以元素 Na、Ba、H、O、S、N 中任意两种或三种元素组成合适的物质,将化学式分别填在下表中④、⑥的后面________ 、__________
(3)⑦和⑧的水溶液可导电,它们________ (填“是”或“不是”)电解质;相同质量的两气体所含氧原子的个数比为________ ;标准状况下等体积两气体的质量比为________ 。
(4)少量⑧与足量④的溶液反应的离子方程式为________ 。
(5)写出⑦与⑨反应的化学方程式________ 。
(6)写出工业制造硝酸过程中⑩NH3 与氧气反应的化学方程式为________ ,若 16g 氧气全部被还原,则转移电子________ mol。
(7)现有由①与②混合的稀溶液 100mL,其中①的物质的量浓度为 2.0mol·L-1,②的物质的量浓度为 1.0mol·L-1。则该溶液能溶解铜的最大质量为________ g,同时,反应生成的气体在标准状况下的体积为________ L。

(1)如图所示的物质分类方法的名称是
(2)以元素 Na、Ba、H、O、S、N 中任意两种或三种元素组成合适的物质,将化学式分别填在下表中④、⑥的后面
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①H2SO4 ②HNO3 | ③NH3· H2O ④ | ⑤NaNO₃ ⑥ | ⑦CO2 ⑧SO2 ⑨Na2O2 | ⑩NH3 |
(4)少量⑧与足量④的溶液反应的离子方程式为
(5)写出⑦与⑨反应的化学方程式
(6)写出工业制造硝酸过程中⑩NH3 与氧气反应的化学方程式为
(7)现有由①与②混合的稀溶液 100mL,其中①的物质的量浓度为 2.0mol·L-1,②的物质的量浓度为 1.0mol·L-1。则该溶液能溶解铜的最大质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)在一个充满CO2的铝制易拉罐中加入适量的NaOH溶液,并密封,易拉罐会慢慢变瘪,原因是____________ (用化学方程式表示,下同)后又慢慢鼓起来,原因是________________ 。
(2)写出还原铁粉与水蒸气反应的化学方程式_____________________ 。
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:___________ ;常用澄清石灰水检验CO2气体的离子方程式是__________________________________ 。将表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是________________________________ ;反应片刻后,可观察到有气体产生,其离子方程式是________________________ 。
(4)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为___________________________________________ 。
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为________________________________________________________________________ 。
(2)写出还原铁粉与水蒸气反应的化学方程式
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:
(4)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
您最近一年使用:0次



