离子反应是中学化学中重要的反应类型。请回答下列问题:
有一瓶澄清的溶液其中可能含有 H+、Mg2+、Ba2+、 、
、 、
、 ,取该溶液进行以下实验:
,取该溶液进行以下实验:
(1)用pH试纸检验,表明溶液呈强酸性,可以排除_____________ 的存在。
(2)取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀产生,则可证明________ 的存在,产生白色沉淀的离子方程式为______________ 。
(3)取部分上述碱性溶液加 Na2CO3溶液,有白色沉淀生成,证明________ 的存在,又可以排除_______ 的存在,产生白色沉淀的离子方程式为__________________ 。
(4)根据上述实验事实还能确定溶液中肯定存在的离子是____________ 。
有一瓶澄清的溶液其中可能含有 H+、Mg2+、Ba2+、
 、
、 、
、 ,取该溶液进行以下实验:
,取该溶液进行以下实验:(1)用pH试纸检验,表明溶液呈强酸性,可以排除
(2)取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀产生,则可证明
(3)取部分上述碱性溶液加 Na2CO3溶液,有白色沉淀生成,证明
(4)根据上述实验事实还能确定溶液中肯定存在的离子是
更新时间:2022-12-18 20:45:33
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分,请回答有关问题:
(1)①形成的单质的电子式为___________ 。
(2)表中最活泼的金属是___________ ,非金属性最强的元素是___________ (填写元素符号)。
(3)表中能形成两性氧化物的元素是___________ ,写出该元素的氢氧化物分别与⑦、⑧最高价氧化物的水化物反应的离子方程式:___________ 、___________ 。
(4)请设计一个实验方案,比较⑦⑨单质氧化性的强弱:___________ 。(用离子方程式表示)
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | ① | ② | |||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 4 | ⑧ | ⑨ |
(2)表中最活泼的金属是
(3)表中能形成两性氧化物的元素是
(4)请设计一个实验方案,比较⑦⑨单质氧化性的强弱:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】高铁酸钾( )是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
)是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
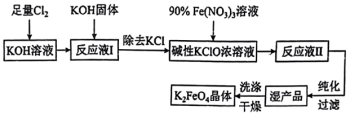
(1)高铁酸钾( )中铁元素的化合价为
)中铁元素的化合价为_______ 。
(2)写出 与KOH溶液反应的化学方程式
与KOH溶液反应的化学方程式_______ 。
(3)写出 溶液与碱性KClO溶液反应的离子方程式
溶液与碱性KClO溶液反应的离子方程式_______ 。
(4) 可作为新型多功能水处理剂的原因是
可作为新型多功能水处理剂的原因是_______ 。
(5)从“反应液Ⅱ”中分离出 后,副产品有
后,副产品有_______ (写化学式)。
(6)该工艺每得到1.98kg ,理论上消耗
,理论上消耗 的物质的量为
的物质的量为_______ mol。
 )是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
)是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
(1)高铁酸钾(
 )中铁元素的化合价为
)中铁元素的化合价为(2)写出
 与KOH溶液反应的化学方程式
与KOH溶液反应的化学方程式(3)写出
 溶液与碱性KClO溶液反应的离子方程式
溶液与碱性KClO溶液反应的离子方程式(4)
 可作为新型多功能水处理剂的原因是
可作为新型多功能水处理剂的原因是(5)从“反应液Ⅱ”中分离出
 后,副产品有
后,副产品有(6)该工艺每得到1.98kg
 ,理论上消耗
,理论上消耗 的物质的量为
的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】碘主要用于制药物、染料和碘化合物等,海带、紫菜等藻类植物中富含碘元素。实验室中从海带中提取碘的流程如图。

已知:碘元素在海带中以碘化物的形式存在;碘单质与NaOH浓溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O
回答下列问题:
(1)“灼烧”时,应将干海带放在_______ (填仪器名称)进行加热。
(2)步骤④发生反应的离子方程式为_______ 。
(3)操作Ⅰ中,实验室可用如图仪器将I2富集到有机溶液X,该仪器名称为_______ ,该步操作的名称为_______ ;图示的有机溶剂可以是_______ (填编号)。

a.酒精 b.醋酸 c.四氯化碳 d.苯
(4)加入45%的硫酸后发生反应的离子方程式为_______ 。
(5)为寻找MnO2的替代品,某同学设计了如下实验来证明H2O2能否代替MnO2。实验操作和现象是:_______ ,则证明H2O2能代替MnO2。

已知:碘元素在海带中以碘化物的形式存在;碘单质与NaOH浓溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O
回答下列问题:
(1)“灼烧”时,应将干海带放在
(2)步骤④发生反应的离子方程式为
(3)操作Ⅰ中,实验室可用如图仪器将I2富集到有机溶液X,该仪器名称为

a.酒精 b.醋酸 c.四氯化碳 d.苯
(4)加入45%的硫酸后发生反应的离子方程式为
(5)为寻找MnO2的替代品,某同学设计了如下实验来证明H2O2能否代替MnO2。实验操作和现象是:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】草木灰中含有可溶性钾盐(主要成分是K2SO4、K2CO3、KCl)。某学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤,取滤液;③蒸发滤液;④冷却结晶。
(1)在①、②、③、④的操作中需要用到玻璃棒是_______ (填序号)。
(2)为检验草木灰中的离子,取少量晶体溶于水,并把溶液分成四份,完成以下实验报告(在横线上填写相关的内容):
(3)步骤ⅲ所得的结论,你认为是否正确?_______ (填是或否);为什么?_______ 。
(4)写出步骤ⅱ有关现象的离子方程式_______ 。
(1)在①、②、③、④的操作中需要用到玻璃棒是
(2)为检验草木灰中的离子,取少量晶体溶于水,并把溶液分成四份,完成以下实验报告(在横线上填写相关的内容):
| 实验步骤 | 实验现象 | 实验结论 |
i.取第一份溶液和适量稀盐酸加入下列装置的试管中,把澄清的石灰水加入烧杯中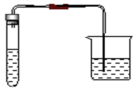 | 证明含有碳酸根离子 | |
| ii.取第二份溶液,分别滴加 | 证明含有硫酸根离子 | |
iii.取第三份溶液加入过量BaCl2溶液,过滤,除去 和CO 和CO ,再滴加AgNO3溶液和稀硝酸 ,再滴加AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 证明含有氯离子 |
| iv.取第四份溶液进行焰色反应 | 透过蓝色钴玻璃火焰呈紫色 | 证明含有K+ |
(3)步骤ⅲ所得的结论,你认为是否正确?
(4)写出步骤ⅱ有关现象的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】根据实验室制取蒸馏水的实验,回答下列问题:
(1)在试管中加入少量自来水,滴加几滴稀硝酸和几滴硝酸银溶液,观察到的实验现象是____________ ,由此说明自来水中含有的离子是__________________ 。
(2)实验室制取蒸馏水的装置如下图所示,请写出装置图中序号所示各仪器的名称____________ 。

(3)若取仪器⑤中收集得到的液体少许,加入到试管中,然后滴加几滴稀硝酸和几滴硝酸银溶液,观察到的现象是____________ ,原因是________________________ 。
(4)通过上述实验,你认为蒸馏实验的应用是____________________________________ 。
(1)在试管中加入少量自来水,滴加几滴稀硝酸和几滴硝酸银溶液,观察到的实验现象是
(2)实验室制取蒸馏水的装置如下图所示,请写出装置图中序号所示各仪器的名称

(3)若取仪器⑤中收集得到的液体少许,加入到试管中,然后滴加几滴稀硝酸和几滴硝酸银溶液,观察到的现象是
(4)通过上述实验,你认为蒸馏实验的应用是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】有A、B、C、D四种可溶性盐,其中阴、阳离子分别是 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有6mL蒸馏水的四支试管中,只有B盐溶液呈黄色。②分别向4支试管中加入1mL稀盐酸,发现A盐溶液中产生白色沉淀、C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有6mL蒸馏水的四支试管中,只有B盐溶液呈黄色。②分别向4支试管中加入1mL稀盐酸,发现A盐溶液中产生白色沉淀、C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述事实,写出化学式:A___________ B___________ C___________ D___________ 。
(2)写出下列反应的离子方程式:
①A+D→:___________
②C+HCl→气体:___________
(3)检验钾盐与钡盐可以通过做___________ 来区别,透过蓝色钴玻璃看,呈现___________ 色火焰的是钾盐
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有6mL蒸馏水的四支试管中,只有B盐溶液呈黄色。②分别向4支试管中加入1mL稀盐酸,发现A盐溶液中产生白色沉淀、C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有6mL蒸馏水的四支试管中,只有B盐溶液呈黄色。②分别向4支试管中加入1mL稀盐酸,发现A盐溶液中产生白色沉淀、C盐溶液中有较多气泡产生,而D盐溶液无明显现象。(1)根据上述事实,写出化学式:A
(2)写出下列反应的离子方程式:
①A+D→:
②C+HCl→气体:
(3)检验钾盐与钡盐可以通过做
您最近一年使用:0次



