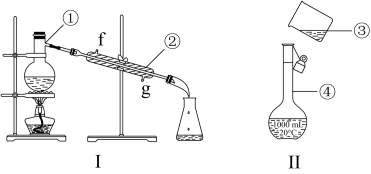
根据实验室制取蒸馏水的实验,回答下列问题:
(1)在试管中加入少量自来水,滴加几滴稀硝酸和几滴硝酸银溶液,观察到的实验现象是____________ ,由此说明自来水中含有的离子是__________________ 。
(2)实验室制取蒸馏水的装置如下图所示,请写出装置图中序号所示各仪器的名称____________ 。

(3)若取仪器⑤中收集得到的液体少许,加入到试管中,然后滴加几滴稀硝酸和几滴硝酸银溶液,观察到的现象是____________ ,原因是________________________ 。
(4)通过上述实验,你认为蒸馏实验的应用是____________________________________ 。
(1)在试管中加入少量自来水,滴加几滴稀硝酸和几滴硝酸银溶液,观察到的实验现象是
(2)实验室制取蒸馏水的装置如下图所示,请写出装置图中序号所示各仪器的名称

(3)若取仪器⑤中收集得到的液体少许,加入到试管中,然后滴加几滴稀硝酸和几滴硝酸银溶液,观察到的现象是
(4)通过上述实验,你认为蒸馏实验的应用是
更新时间:2018-12-15 16:04:59
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】欲配制1.0mol/L 的NaOH溶液250mL,回答下列问题:
(1)用托盘天平称取NaOH固体_____ g,药品应放在_____ 中称量.
(2)称量后,配制此溶液最主要的仪器名称是_____ .
(1)用托盘天平称取NaOH固体
(2)称量后,配制此溶液最主要的仪器名称是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某实验小组同学用图1所示装置制取氨,并探究其性质。
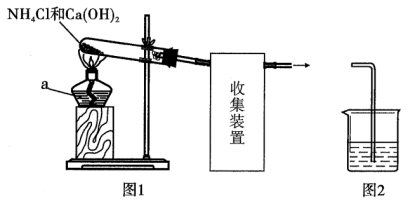
回答下列问题:
(1)仪器 的名称是
的名称是_______ 。
(2)图1中,试管内发生反应的化学方程式是_______ 。
(3)图1方框中的收集装置应为_______ (填下图中字母标号)。
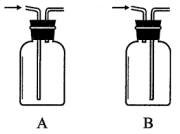
(4)将蘸有浓盐酸的棉球放入收集满 的集气瓶中,迅速盖上玻璃片,可观察到的实验现象是
的集气瓶中,迅速盖上玻璃片,可观察到的实验现象是_______ 。
(5)甲同学设计了图2所示的装置进行尾气处理,乙同学认为该设计不合理,其理由是_______ 。

回答下列问题:
(1)仪器
 的名称是
的名称是(2)图1中,试管内发生反应的化学方程式是
(3)图1方框中的收集装置应为

(4)将蘸有浓盐酸的棉球放入收集满
 的集气瓶中,迅速盖上玻璃片,可观察到的实验现象是
的集气瓶中,迅速盖上玻璃片,可观察到的实验现象是(5)甲同学设计了图2所示的装置进行尾气处理,乙同学认为该设计不合理,其理由是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】配合物乙二胺四乙酸铁钠(NaFeY )可溶于水,常见于铁强化盐中,下图是制备乙二胺四乙酸铁钠晶体的实验,回答下列问题:
实验原理:2Fe(OH)3+Na2CO3+2H4Y=2[NaFeY·3H2O]+CO2↑+H2O
实验步骤:①称取2.7 g FeCl3·6H2O于烧杯中溶解,分批次加入适量浓氨水,搅拌,过滤,洗涤,干燥。
②将Fe(OH)3、乙二胺四乙酸(H4Y)、H2O加入仪器a中,搅拌,80 ℃水浴反应1 h,用Na2CO3溶液调节pH,经过一系列操作,过滤洗涤,晾干得到产品。

(1)仪器a的名称是_______ 。
(2)请简述“步骤①”中洗涤沉淀的操作_______ 。
(3)相对于分液漏斗,滴液漏斗所具有的优点是_______ 。
(4)“步骤②”中的“一系列操作”为_______ (填标号)。
A.蒸发浓缩,趁热结晶
B.蒸发浓缩至大量晶体析出,停止加热
C.蒸发浓缩至溶液表面出现晶膜,停止加热
实验原理:2Fe(OH)3+Na2CO3+2H4Y=2[NaFeY·3H2O]+CO2↑+H2O
实验步骤:①称取2.7 g FeCl3·6H2O于烧杯中溶解,分批次加入适量浓氨水,搅拌,过滤,洗涤,干燥。
②将Fe(OH)3、乙二胺四乙酸(H4Y)、H2O加入仪器a中,搅拌,80 ℃水浴反应1 h,用Na2CO3溶液调节pH,经过一系列操作,过滤洗涤,晾干得到产品。

(1)仪器a的名称是
(2)请简述“步骤①”中洗涤沉淀的操作
(3)相对于分液漏斗,滴液漏斗所具有的优点是
(4)“步骤②”中的“一系列操作”为
A.蒸发浓缩,趁热结晶
B.蒸发浓缩至大量晶体析出,停止加热
C.蒸发浓缩至溶液表面出现晶膜,停止加热
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1)______ 分离饱和食盐水与沙子的混合物。
(2)______ 从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)______ 分离水和汽油的混合物。
(4)______ 从碘水中提取碘。
A.萃取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1)
(2)
(3)
(4)
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】过氧化钙晶体(CaO2 8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
轻质CaCO3粉末 滤液
滤液 白色结晶体
白色结晶体 目标产物
目标产物
回答下列问题:
(1)CaO2电子式:_________________ 。
(2)反应①的离子方程式为_________________ ;过滤过程中用到的玻璃仪器有_________ 。
(3)用上述方法制取CaO2 8H2O的化学方程式为
8H2O的化学方程式为___________________________________ 。
(4)操作②温度不宜过高,其可能原因是___________________________________________ 。
(5)实验室常采用以酸为介质,用高锰酸钾溶液测定过氧化钙的含量。其原理为:5CaO2+8H2SO4+2KMnO4=5CaSO4+2MnSO4+5O2 +8H2O+K2SO4
+8H2O+K2SO4
,某同学准确称取ag产品于有塞锥形瓶中,用适量酸溶解,加入cmLbmol L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为________ (用含a、b、c的代数式表示)。
 8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。轻质CaCO3粉末
 滤液
滤液 白色结晶体
白色结晶体 目标产物
目标产物回答下列问题:
(1)CaO2电子式:
(2)反应①的离子方程式为
(3)用上述方法制取CaO2
 8H2O的化学方程式为
8H2O的化学方程式为(4)操作②温度不宜过高,其可能原因是
(5)实验室常采用以酸为介质,用高锰酸钾溶液测定过氧化钙的含量。其原理为:5CaO2+8H2SO4+2KMnO4=5CaSO4+2MnSO4+5O2
 +8H2O+K2SO4
+8H2O+K2SO4,某同学准确称取ag产品于有塞锥形瓶中,用适量酸溶解,加入cmLbmol
 L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
L-1的高锰酸钾溶液恰好完全反应,则该样品中过氧化钙的百分含量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】请根据要求回答问题,

(1)从氯化钾溶液中得到氯化钾固体,选择装置_____ (填代表装置的字母,下同)
(2)除去自来水中Cl- 等杂质,选择装置_____
(3)从油水混合物中分离出植物油,选择装置____ ,该分离方法的名称为 ____ 。
(4)分离饱和食盐水与沙子的混合物时选用装置_______
(5)装置A中①的名称是_____ ,进水的方向是从 ______ 口进水。
(6)装置B在分液打开活塞前需进行的一步操作是_____ ,下层液体从___ ,上层液体从__ 。

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)除去自来水中Cl- 等杂质,选择装置
(3)从油水混合物中分离出植物油,选择装置
(4)分离饱和食盐水与沙子的混合物时选用装置
(5)装置A中①的名称是
(6)装置B在分液打开活塞前需进行的一步操作是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】已知:溴苯的沸点为156℃,苯的沸点为80℃。实验室用苯和液溴制取溴苯并验证反应类型的实验装置如图:
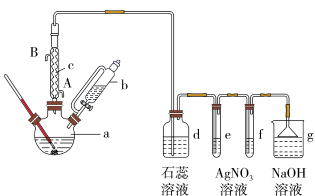
按以下要求回答问题:
(1)冷凝管的进水口为_______ (填“A”或“B”);冷凝管的作用:_______ 。
(2)d中盛放的试剂是_______
(3)有同学认为苯与溴的反应为取代反应,请根据该实验装置特点和实验现象。叙述得出这一结论的实验现象:_______ 。
(4)分离提纯:
①反应后a瓶中的溴苯中因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴可加入_______ 溶液,振荡,再通过_______ (填分离方法)分离提纯;
②苯与溴还可能发生副反应生成对二溴苯(沸点220℃)和邻二溴苯(沸点224℃),因此最后再经_______ (填分离方法)即可得到较纯净的溴苯,该过程中为了受热均匀和易于控制温度,可采用_______ (填“水浴”或“油浴”)加热。
(5)检验鉴别:充分反应后,三颈烧瓶中的粗产品经水洗、分液后得到水洗液,为验证水洗液中是否存在 不能选用的试剂是
不能选用的试剂是_______ (填字母)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液

按以下要求回答问题:
(1)冷凝管的进水口为
(2)d中盛放的试剂是
(3)有同学认为苯与溴的反应为取代反应,请根据该实验装置特点和实验现象。叙述得出这一结论的实验现象:
(4)分离提纯:
①反应后a瓶中的溴苯中因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴可加入
②苯与溴还可能发生副反应生成对二溴苯(沸点220℃)和邻二溴苯(沸点224℃),因此最后再经
(5)检验鉴别:充分反应后,三颈烧瓶中的粗产品经水洗、分液后得到水洗液,为验证水洗液中是否存在
 不能选用的试剂是
不能选用的试剂是A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】蒸馏是实验室制备蒸馏水的常用方法。
(1)图I是实验室制取蒸馏水的常用装置,图中明显的错误是_________________ 。
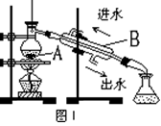
(2)仪器B的名称是______________ 。
(3)实验时A中除加入少量自来水外,还需加入少量__________ 。
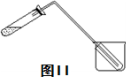
(4)图II装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图I完全相同。该装置中使用的玻璃导管较长,其作用是______________________ ;烧杯中还应盛有的物质是______________________ 。
(1)图I是实验室制取蒸馏水的常用装置,图中明显的错误是


(2)仪器B的名称是
(3)实验时A中除加入少量自来水外,还需加入少量
(4)图II装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图I完全相同。该装置中使用的玻璃导管较长,其作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】为除去粗盐中的钙离子、镁离子、硫酸根离子及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
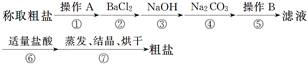
(1)第①步中,操作A是__________ ,第⑤步中,操作B是__________ 。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)____________________________ 。
(3)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因是_________________________ 。
(4)判断氯化钡已过量的方法是____________________ 。

(1)第①步中,操作A是
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)
(3)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因是
(4)判断氯化钡已过量的方法是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D是四种盐,它们的阳离子可能分别是Ca2+、Ag+、Na+、Cu2+中的某一种,阴离子可能分别是NO 、SO
、SO 、Cl-、CO
、Cl-、CO 中的某一种。
中的某一种。
①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有C盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,B溶液中有沉淀产生,D溶液中有无色无味气体逸出。
(1)根据①②的实验事实推断B、C的化学式:B:___ ,C:___ 。
(2)写出A与D反应的化学方程式___ 。
(3)假设A与D恰好反应,若想从A与D反应后的混合物中分别提取得到两种固体产物,需要进行的实验操作是___ 和___ 。这两个操作中都要用到玻璃棒,玻璃棒在这两个操作中的作用是___ 。
 、SO
、SO 、Cl-、CO
、Cl-、CO 中的某一种。
中的某一种。①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有C盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,B溶液中有沉淀产生,D溶液中有无色无味气体逸出。
(1)根据①②的实验事实推断B、C的化学式:B:
(2)写出A与D反应的化学方程式
(3)假设A与D恰好反应,若想从A与D反应后的混合物中分别提取得到两种固体产物,需要进行的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】常见的化肥有氨水、NH4Cl、NH4HCO3、(NH4)2SO4、K2CO3、尿素[CO(NH2)2]等。为确定某种化肥的组成,进行下列实验:
①取少量化肥与烧碱共热,放出可使湿润的红色石蕊试纸变蓝的气体。此气体为______ ,证明化肥中含___ 离子(填写离子符号)。
②向上述反应后的溶液中注入过量盐酸,生成的无色无味气体可使澄清石灰水变浑浊。此气体为________ ,证明化肥中含有_______ 或_________ 离子(填写离子符号)。
③另取少量化肥溶于水,加入CaCl2溶液无明显反应现象。由上可知该化肥的化学式为________ 。
①取少量化肥与烧碱共热,放出可使湿润的红色石蕊试纸变蓝的气体。此气体为
②向上述反应后的溶液中注入过量盐酸,生成的无色无味气体可使澄清石灰水变浑浊。此气体为
③另取少量化肥溶于水,加入CaCl2溶液无明显反应现象。由上可知该化肥的化学式为
您最近一年使用:0次