(1)氯气用于漂白、消毒时,能起漂白、消毒作用的物质是
(2)铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但是该氧化膜易被酸碱破坏,若将氧化铝与氢氧化钠溶液作用,反应的化学方程式为
(3)缺铁性贫血患者应补充Fe元素,通常以硫酸亚铁的形式给药,而硫酸铁则没有这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是
(4)FeSO4·7H2O是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。
①现用绿矾对某工厂酸性废水(含有强氧化性离子
 )进行处理,写出该过程的离子方程式
)进行处理,写出该过程的离子方程式②绿矾除用铁粉与硫酸反应生成外,工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取。已知该反应除生成硫酸亚铁,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:
相似题推荐
 、
、 和少量
和少量 、
、 等物质)为原料,从中回收
等物质)为原料,从中回收 的工艺流程如下:
的工艺流程如下: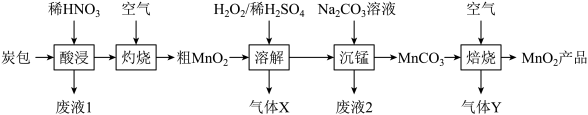
(1)“酸浸”时需将结块的炭包粉碎,目的是
(2)“酸浸”过程中,
 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为(3)“溶解”时加入
 的作用是
的作用是 的实际消耗量比理论值高的原因
的实际消耗量比理论值高的原因(4)写出“焙烧”过程的化学反应方程式为
(5)碱性锌锰干电池是一种使用广泛的便携式电源,结构如图所示。其电池总反应为
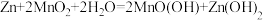 。
。
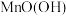 中
中 的化合价为
的化合价为②该电池工作时,负极的反应式为
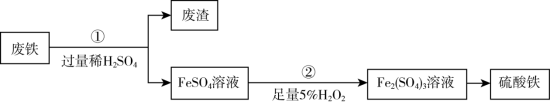
(1)步骤①中主要反应的离子方程式是
(2)分离废渣与FeSO4溶液的操作是
(3)步骤②中加入H2O2溶液发生的反应类型是
(4)检验SO42-的实验操作是
(5)废铁中含有少量硫化物,反应产生的副产物与H2S,可用
A.稀硫酸 B.氢氧化钠溶液 C.硫酸钠溶液
 ,含少量
,含少量 、
、 、
、 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示:
已知:
①“浸取”时,
 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。②
 时,
时, ,
,
③深度除杂标准:溶液中
 ≤2.0×10-6。
≤2.0×10-6。(1)“浸取”温度为
 ,锌的浸出率可达
,锌的浸出率可达 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为(2)“滤渣1”的主要成分为
 、
、(3)“深度除锰”是将残留的
 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比
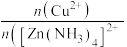 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。
①由图可知,当
 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是②“深度除铜”时
 加入量最优选择
加入量最优选择A.100% B.110% C.120% D.130%
(5)
 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图: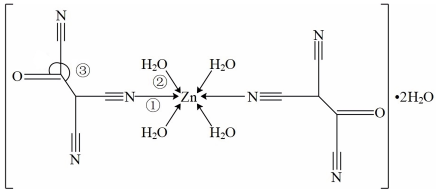
①配位键①和②相比,较稳定的是
②基态
 原子的价电子排布式为
原子的价电子排布式为③键角③
 (填“>”“<”或“=”)
(填“>”“<”或“=”)
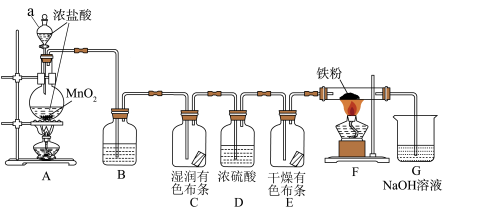
回答下列问题:
(1)仪器a的名称为
(2)B中的试剂为
(3)C、E中有色布条褪色的是
(4)F装置中发生反应的化学方程式为
(5)若将氯气通入冷的石灰乳中,可以制得漂白粉,漂白粉的有效成分是
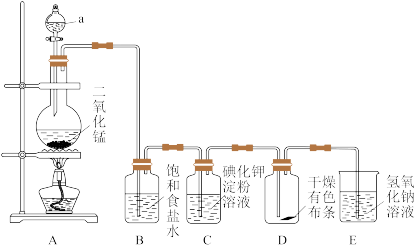
回答下列问题:
(1)写出装置A中发生反应的化学方程式:
(2)当有少量
 通过后,观察到装置C中现象为
通过后,观察到装置C中现象为(3)当
 持续通过时,装置D中现象为
持续通过时,装置D中现象为(4)若要证明
 无漂白性,则必须在装置
无漂白性,则必须在装置(5)装置E的作用是
(6)有一种“地康法”制取氯气的反应原理如图所示:
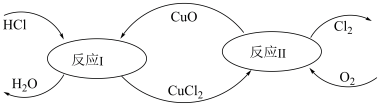
①反应Ⅰ属于
②在450℃条件下,反应Ⅱ的化学方程式为
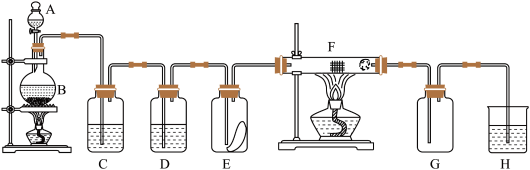
请回答下列问题:
(1)仪器A的名称是
(2)写出实验室制氯气的化学方程式
(3)装置C中盛装的溶液是
(4)在空气中点燃纯净的氢气,然后把导管缓慢伸入盛满氯气的集气瓶中,请描述实验现象
(5)E中的红色布条是否褪色?
(6)H中的试剂为
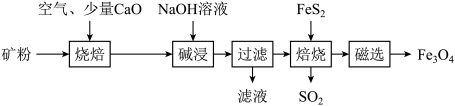
(1)粉碎高硫铝土矿石的目的是
(2)焙烧时发生氧化还原反应:
 ______Fe2O3+______SO2↑,配平该方程式。
______Fe2O3+______SO2↑,配平该方程式。(3)碱浸时发生反应的化学方程式为
(4)过滤后向滤液中通入过量的CO2气体,反应的离子方程式为
(5)“过滤”得到的滤渣中含有大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素在周期表中的位置
(2)写出反应①、⑤、⑥的化学方程式和反应④的离子方程式。
反应①:
反应⑤:
反应⑥:
反应④:
(3)从能量变化的角度看,①、②、③反应中,ΔH<0的是
【推荐3】氮化镓(GaN)是一种重要的半导体材料。某工厂利用铝土矿(成分为Al2O3、Ga2O3、Fe2O3等)为原料制备GaN的流程如下图所示:
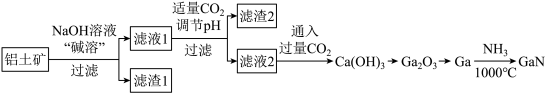
已知:镓与铝同主族,镓的熔点是29.8°C,沸点是2403°C;其氧化物和氢氧化物均为两性化合物;氢氧化物的电离常数如下:
两性氢氧化物 | Al( OH)3 | Ga( OH)3 |
酸式电离常数Ka | 2×10-11 | 1×10-7 |
碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
回答下列问题:
(1)为了提高 “碱溶”效率应采用的措施是
(2)滤渣1的成分是
(3)滤液2中通入过量CO2的理由是
(4)流程中利用镓与NH3在1000℃反应生成固体半导体材料 GaN,每生成l molGaN时放出15. 45 kJ热量,写出该反应的热化学方程式
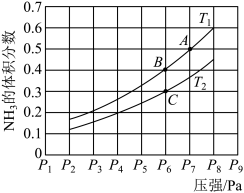
(5)在密闭容器中,充入一定量的Ga与NH3发生反应 ,测得反应平衡体系中NH3的体积分数与压强 P和温度T 的关系曲线如下图所示。图中A 点和C点化学平衡常数的大小关系: KA
(6)已知铝土矿中Ga2O3的质量分数为 a%,某工厂使用 w 吨铝土矿经过一系列反应, 反应过程中镓元素的总利用率为 b%能制得
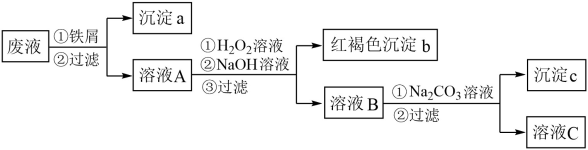
请回答:
(1)沉淀a中含有的单质是
(2)生成沉淀a的离子方程式是
(3)沉淀b的化学式是
(4)沉淀c的化学式是
(5)溶液A与H2O2溶液在酸性条件下反应的离子方程式是
(6)废铁屑提取到的铁盐可以制备高铁酸钾(K2FeO4),其是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
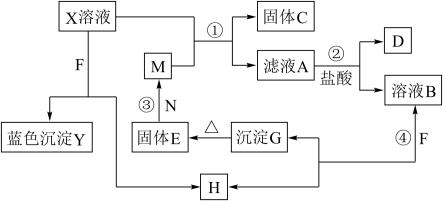
请回答下列问题;
(1)E的化学式为
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是:
(3)在反应①②③④中属于置换反应的是
(4)反应②的离子方程式为
(5)用石墨作电极电解500mL X溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1. 6g.请回答下列问题:
①写出电解时的阳极反应式
②电解后溶液的pH为
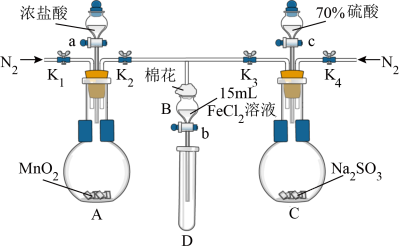
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
Ⅶ.实验结束后,打开弹簧夹K1~K4,再通入一段时间N2,然后拆卸,洗涤,整理仪器。
(1)过程Ⅰ的目的是
(2)棉花中浸润的溶液为
(3)C中发生反应的化学方程式为
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是
(5)甲、乙、丙三位同学分别完成了上述实验,结论如表所示。他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 项目 | 过程Ⅳ中B溶液中含有的离子 | 过程Ⅵ中B溶液中含有的离子 |
| 甲 | 有Fe3+无Fe2+ | 有 |
| 乙 | 既有Fe3+又有Fe2+ | 有 |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |



