室温时,将20mL某气态烃与过量的氧气混合,充分燃烧后冷却至室温,发现混合气体的体积减少60mL,将所得混合气体通过氢氧化钠溶液后,体积又减少80mL。
(1)通过计算确定气态烃分子式_______
(2)已知该烃在一定的温度、压强和催化剂的作用下,可以生成一种高聚物,写出其可能的一种结构_______ 。
(1)通过计算确定气态烃分子式
(2)已知该烃在一定的温度、压强和催化剂的作用下,可以生成一种高聚物,写出其可能的一种结构
更新时间:2022-12-20 12:16:53
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】镁合金及镁的化合物在生产、生活中有着广泛的应用。
(1)镁在元素周期表中的位置是__________________ 。
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

该工艺中可循环使用的物质有______________ 。
(3)储氢材料Mg(AlH4)2在110~200 ℃的反应为Mg(AlH4)2=MgH2+2Al+3H2↑,每转移6 mol电子生成氢气的物质的量为________ mol。
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000 g产品用适量硝酸溶解,经稀释等步骤最终配得500 mL的溶液。
a.准确量取25.00 mL 待测液,用0.100 0 mol/L AgNO3标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为________ mL。

b.
参照上表数据及信息分析,滴定时可以作指示剂的是________ (填数字序号)。
①CaCl2 ②NaBr ③NaI ④K2CrO4
(1)镁在元素周期表中的位置是
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

该工艺中可循环使用的物质有
(3)储氢材料Mg(AlH4)2在110~200 ℃的反应为Mg(AlH4)2=MgH2+2Al+3H2↑,每转移6 mol电子生成氢气的物质的量为
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000 g产品用适量硝酸溶解,经稀释等步骤最终配得500 mL的溶液。
a.准确量取25.00 mL 待测液,用0.100 0 mol/L AgNO3标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为

b.
| AgCl | AgBr | AgI | Ag2CrO4 | |
| Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白 | 淡黄 | 黄 | 砖红 |
①CaCl2 ②NaBr ③NaI ④K2CrO4
您最近一年使用:0次
【推荐2】I.向含有 、
、 、
、 (已知还原性
(已知还原性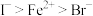 )的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。

(1)当通入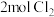 时,溶液中发生反应的离子方程式是:
时,溶液中发生反应的离子方程式是:_______ 。
(2)BC段表示_______ 的物质的量变化情况。
(3)原溶液中
_______ 。
Ⅱ.“化学——我们的生活,我们的未来。”学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(4)生活中若将“84”消毒液(有效成分是 )和洁厕灵(主要成分是
)和洁厕灵(主要成分是 )混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:
)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:_______ 。
(5)某补铁剂(有效成分为 )因长期放置被氧化而失效,为检验其氧化产物
)因长期放置被氧化而失效,为检验其氧化产物 ,同学们取上述样品制成溶液进行如下实验。
,同学们取上述样品制成溶液进行如下实验。
①甲同学取少许溶液,加入_______ 溶液,出现血红色溶液,证明氧化产物为 。
。
②乙同学另取少许溶液,加入淀粉 溶液,溶液变为蓝色,证明氧化产物为
溶液,溶液变为蓝色,证明氧化产物为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
 、
、 、
、 (已知还原性
(已知还原性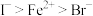 )的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
(1)当通入
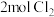 时,溶液中发生反应的离子方程式是:
时,溶液中发生反应的离子方程式是:(2)BC段表示
(3)原溶液中

Ⅱ.“化学——我们的生活,我们的未来。”学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(4)生活中若将“84”消毒液(有效成分是
 )和洁厕灵(主要成分是
)和洁厕灵(主要成分是 )混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:
)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:(5)某补铁剂(有效成分为
 )因长期放置被氧化而失效,为检验其氧化产物
)因长期放置被氧化而失效,为检验其氧化产物 ,同学们取上述样品制成溶液进行如下实验。
,同学们取上述样品制成溶液进行如下实验。①甲同学取少许溶液,加入
 。
。②乙同学另取少许溶液,加入淀粉
 溶液,溶液变为蓝色,证明氧化产物为
溶液,溶液变为蓝色,证明氧化产物为 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】过氧化钙(CaO2)是一种白色、难溶于水的固体,能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。工业生产过程如下:
①在NH4Cl溶液中加入Ca(OH)2;
②不断搅拌的同时加入30%H2O2,反应生成CaO2·8H2O沉淀;
③经过陈化、过滤,水洗得到CaO2·8H2O,再脱水干燥得到CaO2。
已知CaO2在350℃迅速分解生成CaO和O2。下图是实验室测定产品中CaO2含量的装置(夹持装置省略)。

(1)第②步反应的化学方程式为_______ 。
(2)检验CaO2·8H2O是否洗净的方法是:_______ 。
(3)CaO2·8H2O加热脱水的过程中,需不断通入不含二氧化碳的氧气,目的是_______ 、_______ 。
(4)过氧化钙的含量也可用氧化还原滴定法测定,过程如下。准确称取0.1g CaO2产品于锥形瓶中,加入30 mL蒸馏水和10mL 2 mol·L-1 HCl,完全溶解后加入几滴0.1mol·L-1 MnSO4溶液,用0.02mol·L-1 KMnO4标准溶液滴定至终点。平行三次,所得实验数据如下表所示:
①滴定的终点现象是_______ 。
②滴定过程中加入标准溶液发生反应的离子方程式为_______ ,过氧化钙的质量分数为_______ (保留两位有效数字)。
①在NH4Cl溶液中加入Ca(OH)2;
②不断搅拌的同时加入30%H2O2,反应生成CaO2·8H2O沉淀;
③经过陈化、过滤,水洗得到CaO2·8H2O,再脱水干燥得到CaO2。
已知CaO2在350℃迅速分解生成CaO和O2。下图是实验室测定产品中CaO2含量的装置(夹持装置省略)。

(1)第②步反应的化学方程式为
(2)检验CaO2·8H2O是否洗净的方法是:
(3)CaO2·8H2O加热脱水的过程中,需不断通入不含二氧化碳的氧气,目的是
(4)过氧化钙的含量也可用氧化还原滴定法测定,过程如下。准确称取0.1g CaO2产品于锥形瓶中,加入30 mL蒸馏水和10mL 2 mol·L-1 HCl,完全溶解后加入几滴0.1mol·L-1 MnSO4溶液,用0.02mol·L-1 KMnO4标准溶液滴定至终点。平行三次,所得实验数据如下表所示:
| 试验次数 | 一 | 二 | 三 |
| V(KMnO4)/mL | 23.02 | 23.05 | 23.04 |
②滴定过程中加入标准溶液发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和粘合剂等高聚物。为研究X的组成与结构,进行了如下实验:
(1)已知有机物X相对分子质量为100,将10.0g X在足量 中充分燃烧,并使其产物依次通过足量的无水
中充分燃烧,并使其产物依次通过足量的无水 和KOH浓溶液,发现无水
和KOH浓溶液,发现无水 增重7.2g,KOH浓溶液增重22.0g。有机物X的分子式是
增重7.2g,KOH浓溶液增重22.0g。有机物X的分子式是_______ 。
(2)经红外光谱测定有机物X分子中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3:1,有机物X的结构简式是_______ 。
(3)已知:1mol有机物Y在铜催化加热条件下可以生成1mol X和2mol ,请写出由Y生成X的化学方程式
,请写出由Y生成X的化学方程式_______ 。
(4)为检验Y中的官能团的类型和数目,选择的药品是_______ (填字母)。
检验该官能团的实验中,发生反应的化学方程式是_______ 。
(1)已知有机物X相对分子质量为100,将10.0g X在足量
 中充分燃烧,并使其产物依次通过足量的无水
中充分燃烧,并使其产物依次通过足量的无水 和KOH浓溶液,发现无水
和KOH浓溶液,发现无水 增重7.2g,KOH浓溶液增重22.0g。有机物X的分子式是
增重7.2g,KOH浓溶液增重22.0g。有机物X的分子式是(2)经红外光谱测定有机物X分子中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3:1,有机物X的结构简式是
(3)已知:1mol有机物Y在铜催化加热条件下可以生成1mol X和2mol
 ,请写出由Y生成X的化学方程式
,请写出由Y生成X的化学方程式(4)为检验Y中的官能团的类型和数目,选择的药品是
| a.金属钠 | b.10%氢氧化钠溶液 |
| c.2%硝酸银溶液 | d.饱和碳酸钠溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.某种苯的同系物0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。该有机物的分子式为______ 。
Ⅱ.为了证明溴乙烷中存在溴原子,某同学设计如下实验:
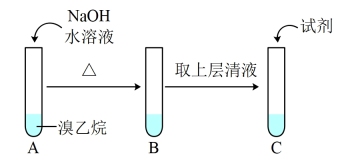
①将试管C中加入的试剂及相应的实验现象补充完整:_________ 。
②溴乙烷在NaOH水溶液中反应的化学方程式是_____________ 。
Ⅲ.为实现以下各步转化,请在下列括号中填入适当试剂。______ 、______
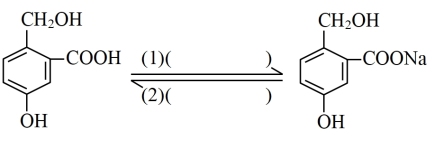
Ⅱ.为了证明溴乙烷中存在溴原子,某同学设计如下实验:

①将试管C中加入的试剂及相应的实验现象补充完整:
②溴乙烷在NaOH水溶液中反应的化学方程式是
Ⅲ.为实现以下各步转化,请在下列括号中填入适当试剂。
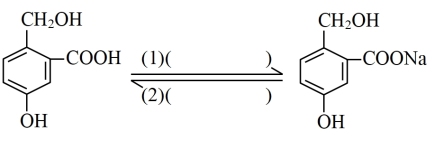
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】有机物M(只含C、H、O三种元素中的两种或三种)具有令人愉悦的牛奶香气,主要用于配制奶油、乳品、酸奶和草莓等型香精,是我国批准使用的香料产品,其沸点为148℃。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:将粗品用蒸馏法进行纯化。
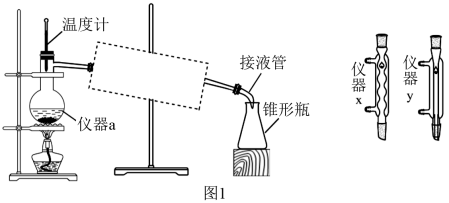
(1)如图1所示,仪器a的名称是_______ ,图中虚线框内应选用右侧的_______ (填“仪器x”或“仪器y”)。
(2)利用元素分析仪测得有机物M中碳的质量分数为54.5%,氢的质量分数为9.1%。
①M的实验式为_______ 。
②已知M的密度是同温同压下CO2密度的2倍,则M的分子式为_______ 。
步骤三:确定M的结构简式。
(3)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示。_______ ,M的结构简式为_______ (填键线式)。
②写出两种含有酯基的M的同分异构体的结构简式:_______ 。
步骤一:将粗品用蒸馏法进行纯化。
(1)如图1所示,仪器a的名称是
(2)利用元素分析仪测得有机物M中碳的质量分数为54.5%,氢的质量分数为9.1%。
①M的实验式为
②已知M的密度是同温同压下CO2密度的2倍,则M的分子式为
步骤三:确定M的结构简式。
(3)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示。
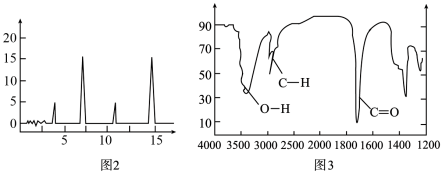
②写出两种含有酯基的M的同分异构体的结构简式:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】有机物B 是相对分子质量为 28 的气态烃,能使溴水褪色。有关物质的转化关系如图:
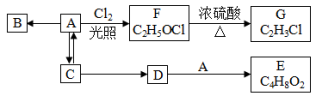
(1)B 分子的空间构型是_______ 。
(2)A→F 的反应类型为_______ ;A→C 的化学方程式为_______ 。
(3)下列说法正确的是_______ 。
a.可用紫色石蕊试液鉴别A 和 D
b.有机物A 和D 都能与Na2CO3 反应
c.等物质的量的A 和B 完全燃烧时消耗等量氧气
(4)物质G 在一定条件下生成的高分子化合物的结构简式是_______ 。
(5)物质E与NaOH 溶液发生反应的化学方程式为_______ 。

(1)B 分子的空间构型是
(2)A→F 的反应类型为
(3)下列说法正确的是
a.可用紫色石蕊试液鉴别A 和 D
b.有机物A 和D 都能与Na2CO3 反应
c.等物质的量的A 和B 完全燃烧时消耗等量氧气
(4)物质G 在一定条件下生成的高分子化合物的结构简式是
(5)物质E与NaOH 溶液发生反应的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】已知>C=C<可被酸性高锰酸钾溶液氧化成二元醇,如:
现以甲基丙烯为原料合成有机玻璃和环状化合物E(C8H12O4):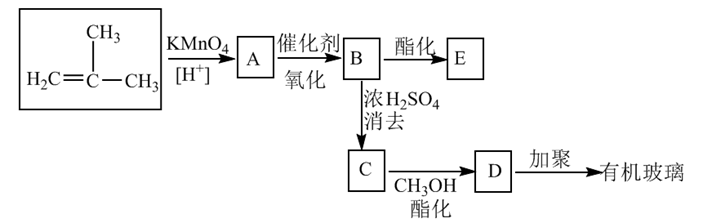
(1) 试写出下列的结构简式:
B______________ C _____________ E _______________
(2) 反应方程式:
B → E_______________________________________________________ ;
B → C_______________________________________________________ ;
C → D_______________________________________________________ 。
现以甲基丙烯为原料合成有机玻璃和环状化合物E(C8H12O4):

(1) 试写出下列的结构简式:
B
(2) 反应方程式:
B → E
B → C
C → D
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】(Ⅰ)如表是A、B两种有机物的有关信息:
根据表中信息回答下列问题:
(1)关于A的下列说法中,不正确的是_____ (填标号)。
a.分子里含有碳碳双键 b.分子里所有的原子共平面 c.结构简式为CH2-CH2
(2)A与H2发生加成反应后生成X,与X在分子组成和结构上相似的有机物有一大类,它们的通式为CnH2n+2。当n=___ 时,这类机物开始出现同分异构体。
(Ⅱ)已知有机物A~F有如图转化关系:
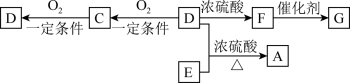
已知:①2CH3CHO+O2 2CH3COOH+2H2O;
2CH3COOH+2H2O;
②CH3CH2OH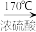 CH2=CH2↑+H2O(该反应属于消去反应)。
CH2=CH2↑+H2O(该反应属于消去反应)。
③A的分子式为C10H20O2; ④B分子中含2个甲基;⑤D、E互为具有相同官能团的同分异构体,D能与碳酸氢钠反应放出CO2,E分子烃基上的氢原子若被Cl取代,其一氯代物有3种;⑥F可以使溴的四氯化碳溶液褪色,G为高分子化合物。请填写以下空白:
(1)B可以发生的反应有_____ (填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D分子所含有的官能团的名称是________ 。
(3)写出与D、E具有相同官能团的同分异构体(D、E除外)可能的结构简式______ 。
(4)写出下列转化的化学方程式:
B+E→A:_______ ;
B→C:___________ ;
F→G:__________ 。
| A | B |
①分子模型为: ; ;②能使溴的四氯化碳溶液褪色; ③其产量是衡量石油化工水平的标志。 | ①由C、H、O三种元素组成,是厨房中的常见调味剂; ②水溶液能使紫色石蕊试液变红。 |
(1)关于A的下列说法中,不正确的是
a.分子里含有碳碳双键 b.分子里所有的原子共平面 c.结构简式为CH2-CH2
(2)A与H2发生加成反应后生成X,与X在分子组成和结构上相似的有机物有一大类,它们的通式为CnH2n+2。当n=
(Ⅱ)已知有机物A~F有如图转化关系:

已知:①2CH3CHO+O2
 2CH3COOH+2H2O;
2CH3COOH+2H2O;②CH3CH2OH
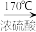 CH2=CH2↑+H2O(该反应属于消去反应)。
CH2=CH2↑+H2O(该反应属于消去反应)。③A的分子式为C10H20O2; ④B分子中含2个甲基;⑤D、E互为具有相同官能团的同分异构体,D能与碳酸氢钠反应放出CO2,E分子烃基上的氢原子若被Cl取代,其一氯代物有3种;⑥F可以使溴的四氯化碳溶液褪色,G为高分子化合物。请填写以下空白:
(1)B可以发生的反应有
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D分子所含有的官能团的名称是
(3)写出与D、E具有相同官能团的同分异构体(D、E除外)可能的结构简式
(4)写出下列转化的化学方程式:
B+E→A:
B→C:
F→G:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】I.依据A~E几种烃分子的示意图或结构填空。

(1)分子中所有原子共平面的是______ (填序号)。
(2)等物质的量的上述烃完全燃烧时消耗O2最多的是______ (填序号);等质量的上述烃完全燃烧时消耗O2最多的是_________ (填序号)。
(3)在120℃,1.01× l05 Pa 下,取气态的上述分烃别与足O2量混合点燃,完全燃烧后恢复至初始状态,气体体积没有变化的是______ (填序号)。
II.现有以下几种有机物:
① CH4 ②CH3CH2CH2OH ③ ④癸烷 ⑤CH3COOH ⑥
④癸烷 ⑤CH3COOH ⑥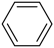 ⑦
⑦ ⑧
⑧ ⑨丙烷
⑨丙烷
请根据上述给出的物质按要求回答下列问题:
(4)与⑧互为同分异构体的是__________ ( 填序号);
(5)用 “>” 表示 ①③④⑨密度从高到低排列顺序:__________ ;
(6)具有特殊气味, 常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一取代反应的化学方程式___________ ;
(7)有机物②在加热条件下和CuO反应的化学方程式__________ ;

(1)分子中所有原子共平面的是
(2)等物质的量的上述烃完全燃烧时消耗O2最多的是
(3)在120℃,1.01× l05 Pa 下,取气态的上述分烃别与足O2量混合点燃,完全燃烧后恢复至初始状态,气体体积没有变化的是
II.现有以下几种有机物:
① CH4 ②CH3CH2CH2OH ③
 ④癸烷 ⑤CH3COOH ⑥
④癸烷 ⑤CH3COOH ⑥ ⑦
⑦ ⑧
⑧ ⑨丙烷
⑨丙烷请根据上述给出的物质按要求回答下列问题:
(4)与⑧互为同分异构体的是
(5)用 “>” 表示 ①③④⑨密度从高到低排列顺序:
(6)具有特殊气味, 常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一取代反应的化学方程式
(7)有机物②在加热条件下和CuO反应的化学方程式
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】现有甲、乙、丙、丁四种有机物,其中甲、乙、丁均属于烃类,丙中只含C、H、O三种元素。甲是一种烷烃且碳原子数是乙的两倍;常温下乙的密度与 的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12:1,回答下列问题:
的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12:1,回答下列问题:
(1)①若甲的结构中无支链,则甲的结构简式为___________ ,其分子中所有碳原子___________ (填标号)在一条直线上。
A.一定在 B.可能在 C.一定不在 D.无法判断是否在
②向某集气瓶内充满甲和 的混合气体,装置如图:
的混合气体,装置如图:
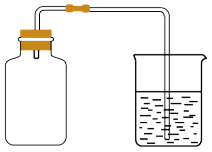
光照足够长时间后,可观察到烧杯中的水被吸入集气瓶中,还能观察到的现象有___________ 、___________ (任意写出两条)。
(2)乙的电子式为___________ ;乙与水在一定条件下反应生成丙的化学方程式为___________ 。
(3)将光亮的铜丝放到酒精灯上灼烧后再插入丙中,并重复几次,可观察到的现象为___________ ,在铜作催化剂并加热的条件下,丙与氧气发生反应的化学方程式为___________ 。
(4)等物质的量的甲、乙、丙、丁完全燃烧时消耗氧气的物质的量大小顺序是___________ (用甲、乙、丙、丁表示)。
 的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12:1,回答下列问题:
的相等;丙是一种具有特殊香味的液体,可由乙与水在一定条件下反应制得;丁的结构中只含有1个环且不含官能团,其相对分子质量为78,分子中碳元素与氢元素的质量比为12:1,回答下列问题:(1)①若甲的结构中无支链,则甲的结构简式为
A.一定在 B.可能在 C.一定不在 D.无法判断是否在
②向某集气瓶内充满甲和
 的混合气体,装置如图:
的混合气体,装置如图:
光照足够长时间后,可观察到烧杯中的水被吸入集气瓶中,还能观察到的现象有
(2)乙的电子式为
(3)将光亮的铜丝放到酒精灯上灼烧后再插入丙中,并重复几次,可观察到的现象为
(4)等物质的量的甲、乙、丙、丁完全燃烧时消耗氧气的物质的量大小顺序是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】饱和烃A和不饱和烃B在常温下均为气体,其中A含的碳原子数多于B。将A、B按一定比例混合,1L混合气体完全燃烧后在同温同压下得到3.6LCO2。
(1)试推断该混合气体的可能组成及A、B混合时的体积比,将结果填入表中。_______________________
(2)1mol该混合气体恰好能使含0.2mol溴的四氯化碳溶液完全褪色,则A和B的化学式分别为________ 和_________ 。
(3)1mol该混合气体在氧气中完全燃烧,得到68.4g水,则A和B的化学式分别为_________ 和__________ 。
(4)120℃时,1LA和1LB与足量O2混合后点燃,在同温同压下体积增大2L,则A和B的化学式分别为_________ 和_________ 。
(1)试推断该混合气体的可能组成及A、B混合时的体积比,将结果填入表中。
| A的化学式 | B的化学式 | VA:VB |
(3)1mol该混合气体在氧气中完全燃烧,得到68.4g水,则A和B的化学式分别为
(4)120℃时,1LA和1LB与足量O2混合后点燃,在同温同压下体积增大2L,则A和B的化学式分别为
您最近一年使用:0次



