开发和利用海洋资源是当前科学研究的一项重要任务,如图是某化工厂对海洋资源综合利用的流程图:
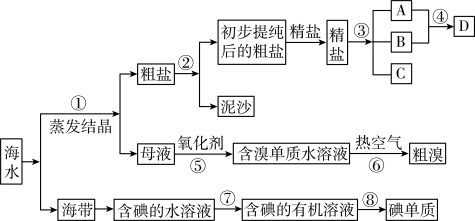
请根据以上信息回答下列问题:
(1)写出流程中⑦所用的方法:_______ 。
(2)初步提纯后的粗盐中含有Ca2+、Mg2+、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:

加入的试剂①、②分别是:_______ 、_______ 。
(3)步骤③的条件是通直流电,其离子方程式为_______ 。D具有杀菌消毒的作用,在喷洒前需要在空气中晾置一会,这样做的原因是_______ 。
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力(即得电子数)相当于多少克Cl2的氧化能力(氯元素均被还原至-1价)。则亚氯酸钠NaClO2的有效氯含量为_______ (保留两位小数)。
(5)若用来提取Br2,反应⑤所用的氧化剂的来源较合理的是_______ 。
A.从外地购买 B.在当地新建生产厂 C.从本厂生产烧碱处循环
(6)流程⑥将溴单质从水溶液中分离出来是基于溴单质具有_______ 性。对粗溴一般做如下处理:
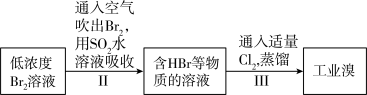
其中步骤Ⅱ、Ⅲ起到的作用是_______ 。
向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应。
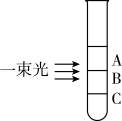
(7)写出制备氯化银胶体的方程式:_______ 。
(8)具有明显的丁达尔效应的是区域_______ (填字母),该区域中分散质的粒径大小为_______ 。
(9)分离出C区域的分散质的方法是_______ 。

请根据以上信息回答下列问题:
(1)写出流程中⑦所用的方法:
(2)初步提纯后的粗盐中含有Ca2+、Mg2+、
 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
加入的试剂①、②分别是:
(3)步骤③的条件是通直流电,其离子方程式为
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力(即得电子数)相当于多少克Cl2的氧化能力(氯元素均被还原至-1价)。则亚氯酸钠NaClO2的有效氯含量为
(5)若用来提取Br2,反应⑤所用的氧化剂的来源较合理的是
A.从外地购买 B.在当地新建生产厂 C.从本厂生产烧碱处循环
(6)流程⑥将溴单质从水溶液中分离出来是基于溴单质具有

其中步骤Ⅱ、Ⅲ起到的作用是
向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应。

(7)写出制备氯化银胶体的方程式:
(8)具有明显的丁达尔效应的是区域
(9)分离出C区域的分散质的方法是
更新时间:2023-01-04 08:32:49
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】明矾[ ]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为
]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为 和
和 ,还含有少量的
,还含有少量的 和
和 的氧化物)为原料制备明矾的工艺流程如图:
的氧化物)为原料制备明矾的工艺流程如图:
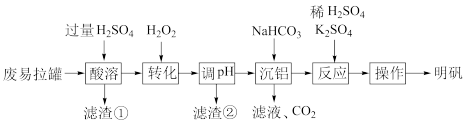
已知:不同温度下 的溶解度如表。
的溶解度如表。
回答下列问题:
(1)明矾在水溶液中的电离方程式为_____________________________ 。
(2)“酸溶”时溶液中主要的金属离子有 、
、__________ 、__________ 。
(3)从物质的分类角度考虑,上述流程中出现的物质,属于酸性氧化物的是_________ (填化学式)。
(4)写出“酸溶”时氧化铝与稀硫酸反应的化学方程式:________________________________ 。
(5)“转化”“调 ”的目的是将铁元素转化为
”的目的是将铁元素转化为 沉淀除去,实际生产中
沉淀除去,实际生产中 易形成胶体,鉴定是否产生
易形成胶体,鉴定是否产生 胶体,可采用的方法是
胶体,可采用的方法是____________ 。
(6)“沉铝”中加入 的目的是将
的目的是将 转化为
转化为 ,补全该反应的离子方程式:
,补全该反应的离子方程式: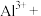

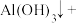

_______________________ 。
(7)“操作”包括____________ 、___________ 、过滤、洗涤、干燥可得到明矾晶体。
(8)某工厂用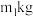 废易拉罐(含
废易拉罐(含 )制备
)制备 (相对分子质量为474),最终得到产品
(相对分子质量为474),最终得到产品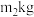 ,产率为
,产率为_________ 。
 ]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为
]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为 和
和 ,还含有少量的
,还含有少量的 和
和 的氧化物)为原料制备明矾的工艺流程如图:
的氧化物)为原料制备明矾的工艺流程如图:
已知:不同温度下
 的溶解度如表。
的溶解度如表。温度 | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
 的溶解度 的溶解度 | 3.00 | 3.99 | 5.90 | 8.39 | 11.0 | 24.80 | 71.00 | 109.00 |
(1)明矾在水溶液中的电离方程式为
(2)“酸溶”时溶液中主要的金属离子有
 、
、(3)从物质的分类角度考虑,上述流程中出现的物质,属于酸性氧化物的是
(4)写出“酸溶”时氧化铝与稀硫酸反应的化学方程式:
(5)“转化”“调
 ”的目的是将铁元素转化为
”的目的是将铁元素转化为 沉淀除去,实际生产中
沉淀除去,实际生产中 易形成胶体,鉴定是否产生
易形成胶体,鉴定是否产生 胶体,可采用的方法是
胶体,可采用的方法是(6)“沉铝”中加入
 的目的是将
的目的是将 转化为
转化为 ,补全该反应的离子方程式:
,补全该反应的离子方程式: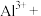

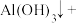

(7)“操作”包括
(8)某工厂用
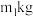 废易拉罐(含
废易拉罐(含 )制备
)制备 (相对分子质量为474),最终得到产品
(相对分子质量为474),最终得到产品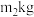 ,产率为
,产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)某温度,100mL饱和FeCl3溶液中含氯离子(Cl-)1.5mol,则该FeCl3溶液的物质的量浓度为_____ 。若将该饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是_____ (选填字母)。
A. 冷水 B. 沸水 C. NaOH浓溶液 D. NaCl浓溶液
(2)制备Fe(OH)3胶体的化学方程式为___________ 。
(3)鉴别FeCl3溶液与Fe(OH)3胶体的实验方法是_______ 。
(4)向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为__________ ;继续滴加,沉淀最终消失且得棕黄色溶液,写出化学方程式_______ 。
(5)可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若___________ (填实验现象),则说明该Fe(OH)3胶体中的杂质离子已经完全除去。

(1)某温度,100mL饱和FeCl3溶液中含氯离子(Cl-)1.5mol,则该FeCl3溶液的物质的量浓度为
A. 冷水 B. 沸水 C. NaOH浓溶液 D. NaCl浓溶液
(2)制备Fe(OH)3胶体的化学方程式为
(3)鉴别FeCl3溶液与Fe(OH)3胶体的实验方法是
(4)向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
(5)可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】某学校组织学生进行实验探究活动,根据所学知识回答下列问题:
Ⅰ.某无色溶液中可能含有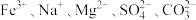 中的某几种离子。为确认该溶液中的离子组成,甲组同学进行实验:取
中的某几种离子。为确认该溶液中的离子组成,甲组同学进行实验:取 上述溶液,加入足量的
上述溶液,加入足量的 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀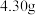 。若向该沉淀中加入过量的稀盐酸,仍有
。若向该沉淀中加入过量的稀盐酸,仍有 沉淀不溶。
沉淀不溶。
(1)该无色溶液中一定不存在的离子为_______ (填离子符号)。
(2)加入稀盐酸后溶解的沉淀为_______ (填化学式,下同),不溶解的沉淀为_______ 。
Ⅱ. 胶体可用于净水。
胶体可用于净水。
乙组同学设计实验制备 胶体,向
胶体,向 沸水中逐滴加入5~6滴
沸水中逐滴加入5~6滴 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
(3)证明有 胶体生成的实验操作是
胶体生成的实验操作是_______ ,利用的胶体性质是_______ 。
Ⅲ.高铁酸钾 可用于自来水消毒、净化。
可用于自来水消毒、净化。
(4)丙组同学在碱性条件下,利用 与
与 反应制备高铁酸钾,其反应的化学方程式为
反应制备高铁酸钾,其反应的化学方程式为 。在上述反应中,氧化剂与还原剂的物质的量之比为
。在上述反应中,氧化剂与还原剂的物质的量之比为_______ ,被氧化的元素为_______ (填元素符号)。
Ⅰ.某无色溶液中可能含有
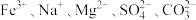 中的某几种离子。为确认该溶液中的离子组成,甲组同学进行实验:取
中的某几种离子。为确认该溶液中的离子组成,甲组同学进行实验:取 上述溶液,加入足量的
上述溶液,加入足量的 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀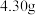 。若向该沉淀中加入过量的稀盐酸,仍有
。若向该沉淀中加入过量的稀盐酸,仍有 沉淀不溶。
沉淀不溶。(1)该无色溶液中一定不存在的离子为
(2)加入稀盐酸后溶解的沉淀为
Ⅱ.
 胶体可用于净水。
胶体可用于净水。乙组同学设计实验制备
 胶体,向
胶体,向 沸水中逐滴加入5~6滴
沸水中逐滴加入5~6滴 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
饱和溶液,继续煮沸至溶液呈红褐色,停止加热。(3)证明有
 胶体生成的实验操作是
胶体生成的实验操作是Ⅲ.高铁酸钾
 可用于自来水消毒、净化。
可用于自来水消毒、净化。(4)丙组同学在碱性条件下,利用
 与
与 反应制备高铁酸钾,其反应的化学方程式为
反应制备高铁酸钾,其反应的化学方程式为 。在上述反应中,氧化剂与还原剂的物质的量之比为
。在上述反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】海水经过晒盐后得到粗盐和苦卤,粗盐中除含有Ca2+,Mg2+,SO42﹣等可溶性杂质外,还含有泥沙等不溶性杂质,食用的精盐是用粗盐提纯得到,流程如图所示:
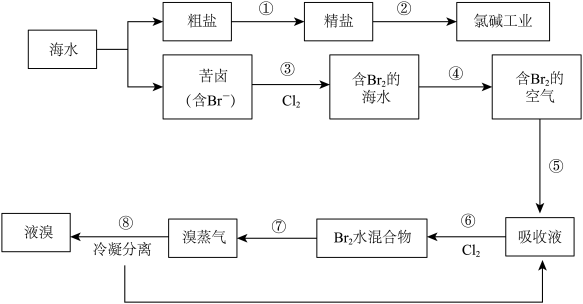
(1)为了除去粗盐中的Ca2+,Mg2+,SO42﹣,采取以下措施:
a.粗盐中含有的 Ca2+、Mg2+,精制过程中为除去这两种离子,发生的离子反应方程式分别为:_____ ,_____ 。
b.若粗盐中SO42﹣含量较高,必须添加钡试剂除去SO42﹣,该钡试剂可以是_____
A.Ba(OH)2
B.Ba(NO3)2
C.BaCl2
D.BaSO4
滴加钡试剂时,需注意(滴加试剂的先后顺序):_____ 。
(2)分离出粗盐后的苦卤还可用于溴元素的提取,在实验室中如何验证苦卤液中含有 Br﹣:_____ 。
(3)在苦卤提溴的过程中,第⑤步骤中可用亚硫酸钠溶液来吸收,则所发生的离子反应方程式为:_____ ,步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度 相差很大的特点进行分离。若在实验室分离上述混合物的分离仪器的名称是_____ ,分离时液 溴从分离器的_____ (填“上口”或“下口”)排出。

(1)为了除去粗盐中的Ca2+,Mg2+,SO42﹣,采取以下措施:
a.粗盐中含有的 Ca2+、Mg2+,精制过程中为除去这两种离子,发生的离子反应方程式分别为:
b.若粗盐中SO42﹣含量较高,必须添加钡试剂除去SO42﹣,该钡试剂可以是
A.Ba(OH)2
B.Ba(NO3)2
C.BaCl2
D.BaSO4
滴加钡试剂时,需注意(滴加试剂的先后顺序):
(2)分离出粗盐后的苦卤还可用于溴元素的提取,在实验室中如何验证苦卤液中含有 Br﹣:
(3)在苦卤提溴的过程中,第⑤步骤中可用亚硫酸钠溶液来吸收,则所发生的离子反应方程式为:
您最近一年使用:0次
【推荐2】某厂排放的废液中含有大量的K+、Cl-、Br-,还含有少量的Ca2+、Mg2+、SO42-.某研究性学习小组拟取这种工业废水来制取较纯净的氯化钾晶体及液溴,他们设计了如下的流程:(已知:若用实际参加反应的离子表示化学反应,则溶液中可能发生如下反应:
H2O2+2Br- =H2O+Br2;10Br-+2MnO4-+16H+ =2Mn2++5Br2+8H2O)
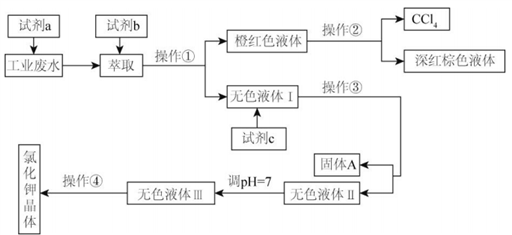
可供试剂a、b、c选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2 溶液、苯、CCl4、H2O2溶液、KMnO4(H+)溶液.
根据以上流程回答相关问题:
⑴试剂a、b分别是_________ 、___________ .
⑵操作①②③④的名称是__________ (填字母代号)
a. 过滤、分液、过滤、蒸发结晶
b. 分液、蒸馏、过滤、蒸发结晶
c. 分液、过滤、过滤、蒸发结晶
d. 分液、分液、过滤、蒸发结晶
⑶除去无色液体Ⅰ中的 Ca2+、 Mg2+、 SO42-,选出 c 所代表的试剂,按滴加顺序依次是_________ (只填化学式).
⑷调节 pH 的作用是___________________________________ .
H2O2+2Br- =H2O+Br2;10Br-+2MnO4-+16H+ =2Mn2++5Br2+8H2O)

可供试剂a、b、c选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2 溶液、苯、CCl4、H2O2溶液、KMnO4(H+)溶液.
根据以上流程回答相关问题:
⑴试剂a、b分别是
⑵操作①②③④的名称是
a. 过滤、分液、过滤、蒸发结晶
b. 分液、蒸馏、过滤、蒸发结晶
c. 分液、过滤、过滤、蒸发结晶
d. 分液、分液、过滤、蒸发结晶
⑶除去无色液体Ⅰ中的 Ca2+、 Mg2+、 SO42-,选出 c 所代表的试剂,按滴加顺序依次是
⑷调节 pH 的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】浩瀚的大海具有丰富的可以开发和利用的化学资源。根据如图所示流程回答下列问题:
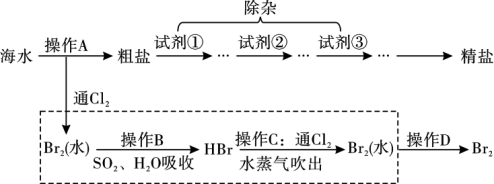
(1)操作A是___________ (填实验操作名称)和过滤。
(2)粗盐中常含有少量泥沙及Ca2+、Mg2+、 等杂质离子,除杂步骤中试剂①~③可行的添加顺序有___________。
等杂质离子,除杂步骤中试剂①~③可行的添加顺序有___________。
(3)写出操作C中通Cl2发生反应的离子方程式:___________ ;可以用水蒸气将Br2吹出的原因是___________ ;图中虚线框内流程的主要目的是___________ 。
(4)操作D中用到的装置为___________ 。

(1)操作A是
(2)粗盐中常含有少量泥沙及Ca2+、Mg2+、
 等杂质离子,除杂步骤中试剂①~③可行的添加顺序有___________。
等杂质离子,除杂步骤中试剂①~③可行的添加顺序有___________。| A.①Na2CO3②BaCl2③NaOH | B.①BaCl2②NaOH③Na2CO3 |
| C.①NaOH②Na2CO3③BaCl2 | D.①BaCl2②Na2CO3③NaOH |
(4)操作D中用到的装置为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海洋是巨大的资源宝库,可以提取到我们需要的食盐、溴和碘。从海水中提取食盐和溴的过程如下:_______ 。
(2)步骤II用SO2水溶液吸收Br2,吸收率可达95%,有关反应的化学方程式为:_______ 。

(2)步骤II用SO2水溶液吸收Br2,吸收率可达95%,有关反应的化学方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海洋资源的开发与利用 海洋资源具有广阔的应用场景。请结合下图,回答以下问题:
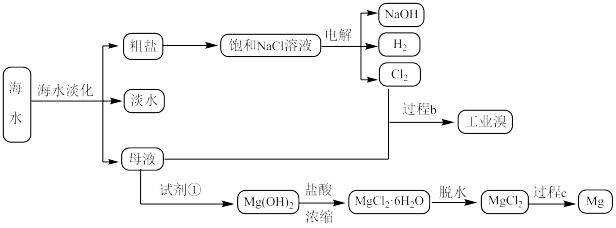
(1)海水晒盐使用的盐田法,相当于化学中的_______ 。
(2)粗盐中存在 Ca2+、Mg2+、SO 等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是
等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是_______ (填序号)。①过量的 Na2CO3溶液 ②过量的 BaCl2溶液 ③过量的NaOH 溶液
A.①②③ B. ②①③ C. ③②①
(3)某同学利用食盐进行化学实验,按照图 1 连接好线路发现灯泡不亮,按照图 2连接好线路发现灯泡亮,由此得出的结论正确的是_______。


(4)我国著名实业家吴蕴初建设的天原化工厂为我国第一个氯碱厂,其生产原理即为电解饱和食盐水,阴极产物为_______ 。
(5)过程b用于海水提溴。主要工业生产流程如下图所示。

①吹出塔中通入热空气吹出 Br2,利用了 Br2的_______ ,吸收塔中吸收Br2,利用了 Br2的_______ (填序号)。
A.氧化性 B.还原性 C.挥发性 D.易溶于水
②吸收塔中反应的离子方程式是_______ 。
③母液可用于海水提镁。试用电子式表示氯化镁的形成_______ 。
(6)海带中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
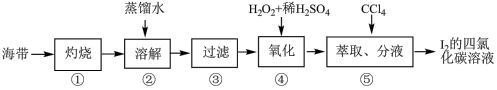
①向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_______ 。
②选择 CCl4作萃取剂的原因是_______ ,现象为_______ 。

(1)海水晒盐使用的盐田法,相当于化学中的
(2)粗盐中存在 Ca2+、Mg2+、SO
 等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是
等可溶性杂质离子,要除去这些离子加入沉淀剂的顺序正确的是A.①②③ B. ②①③ C. ③②①
(3)某同学利用食盐进行化学实验,按照图 1 连接好线路发现灯泡不亮,按照图 2连接好线路发现灯泡亮,由此得出的结论正确的是_______。


| A.NaCl 固体不导电,不是电解质 |
| B.图 2 中 NaCl 在电流作用下电离出了大量自由移动的离子 |
| C.图 2 中水是电解质,电离产生大量的H+和 OH- |
| D.电解质本身不一定能导电 |
(4)我国著名实业家吴蕴初建设的天原化工厂为我国第一个氯碱厂,其生产原理即为电解饱和食盐水,阴极产物为
(5)过程b用于海水提溴。主要工业生产流程如下图所示。

①吹出塔中通入热空气吹出 Br2,利用了 Br2的
A.氧化性 B.还原性 C.挥发性 D.易溶于水
②吸收塔中反应的离子方程式是
③母液可用于海水提镁。试用电子式表示氯化镁的形成
(6)海带中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
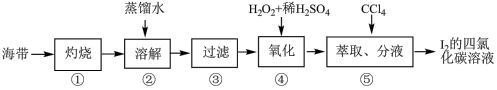
①向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
②选择 CCl4作萃取剂的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海洋蕴藏着丰富的资源,以海水为原料可以制取Na、NaOH 、Mg、Cl2、Br2等。下图是某化工厂对海水资源综合利用的示意图。
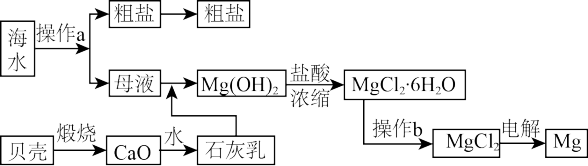
回答下列问题:
(1)流程图中操作a的名称为_______________ 。
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③Ba(OH)2,这3种试剂添加的合理顺序是
等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③Ba(OH)2,这3种试剂添加的合理顺序是____________ (填序号)。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。电解所得的镁蒸气需在特定的环境中冷却,不能用CO2 作冷却剂的原因是___________________ (用化学方程式表示)。
(4)上述流程没有涉及到的四大基本反应类型是________________
A 化合反应 B 分解反应 C 置换反应 D 复分解反应
(5)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入氯气,又制取了重要的化工原料溴单质,生成溴单质反应的离子方程式是______________________ 。

回答下列问题:
(1)流程图中操作a的名称为
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、
 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③Ba(OH)2,这3种试剂添加的合理顺序是
等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③Ba(OH)2,这3种试剂添加的合理顺序是(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。电解所得的镁蒸气需在特定的环境中冷却,不能用CO2 作冷却剂的原因是
(4)上述流程没有涉及到的四大基本反应类型是
A 化合反应 B 分解反应 C 置换反应 D 复分解反应
(5)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入氯气,又制取了重要的化工原料溴单质,生成溴单质反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】海洋植物如海带海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:

(1)指出提取的过程中有关实验操作名称:①________ ;③________ ;写出过程②中有关反应的化学方程式:________________ 。
(2)提取碘的过程中,可供选择的有机溶剂是________ 。
A.水、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、酒精
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是________ 。
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏。指出下图所示实验装置中的错误之处;①________ ;②________ ;③________ 。

(5)进行上述蒸馏操作时,使用水浴的原因是________________ ;最后碘晶体在________ 里聚集。

(1)指出提取的过程中有关实验操作名称:①
(2)提取碘的过程中,可供选择的有机溶剂是
A.水、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、酒精
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏。指出下图所示实验装置中的错误之处;①

(5)进行上述蒸馏操作时,使用水浴的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
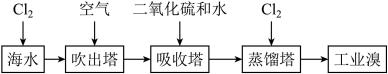
(1)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:_____ 。
(2)蒸馏塔的蒸馏温度应控制在80-90℃最有利于生产,原因可能为:温度过高,_____ ;温度过低,_____ 。
Ⅱ.海水提镁
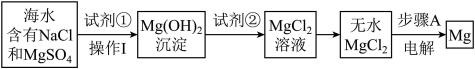
(3)工业上常用于沉淀Mg2+的廉价试剂①的俗名是_____ 。
(4)步骤A的化学方程式为_____ 。
Ⅲ.海带提碘
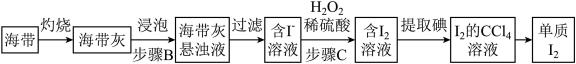
(5)步骤C中反应的离子方程式为_____ 。
Ⅰ.海水提溴

(1)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:
(2)蒸馏塔的蒸馏温度应控制在80-90℃最有利于生产,原因可能为:温度过高,
Ⅱ.海水提镁

(3)工业上常用于沉淀Mg2+的廉价试剂①的俗名是
(4)步骤A的化学方程式为
Ⅲ.海带提碘

(5)步骤C中反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的。
I、结合如下实验装置图回答下列问题:
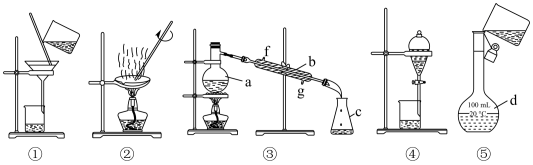
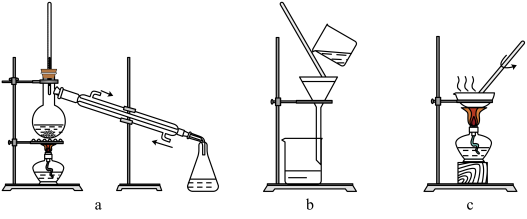
(1)仪器a的名称是___________ , 仪器 b的名称___________ ,
(2)实验④的操作名称是___________ ,
(3)若利用装置③分离乙酸(沸点118 ℃) 和乙酸乙酯(沸点77.1 ℃)的混合物,还缺少的仪器有___________ ,将仪器补充完整后进行的实验操作的名称为___________ ;实验时仪器b中冷却水的进水口为___________ (填“f”或“g”)。
Ⅱ、海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:

(4)提取碘的过程中有关的实验操作名称:①___________ ③___________ ;
(5)提取碘的过程中,可供选择的有机试剂是___________。
I、结合如下实验装置图回答下列问题:

(1)仪器a的名称是
(2)实验④的操作名称是
(3)若利用装置③分离乙酸(沸点118 ℃) 和乙酸乙酯(沸点77.1 ℃)的混合物,还缺少的仪器有
Ⅱ、海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:

(4)提取碘的过程中有关的实验操作名称:①
(5)提取碘的过程中,可供选择的有机试剂是___________。
| A.四氯化碳 | B.汽油 | C.酒精 | D.醋酸 |
您最近一年使用:0次



