化学与生产、生活息息相关。请回答以下问题。
(1)小苏打可用于治疗胃酸过多,写出该反应的离子方程式_______ 。
(2)合成氨工业化,对人类影响深远。工业上合成氨的化学方程式为_______ 。
(3)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为_______ 。
(4)用碘水、淀粉等试剂检测葡萄酒中 的含量,写出相应的离子方程式
的含量,写出相应的离子方程式_______ 。
(5)洁厕剂的主要成分为盐酸。欲配制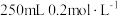 的盐酸,需要HCl的物质的量为
的盐酸,需要HCl的物质的量为_______ 。
(1)小苏打可用于治疗胃酸过多,写出该反应的离子方程式
(2)合成氨工业化,对人类影响深远。工业上合成氨的化学方程式为
(3)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(4)用碘水、淀粉等试剂检测葡萄酒中
 的含量,写出相应的离子方程式
的含量,写出相应的离子方程式(5)洁厕剂的主要成分为盐酸。欲配制
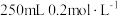 的盐酸,需要HCl的物质的量为
的盐酸,需要HCl的物质的量为
更新时间:2023-01-06 15:48:41
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】有下列物质:①氢氧化钡固体、②KHSO4、③HNO3、④稀硫酸、⑤二氧化碳气体、⑥铜、⑦碳酸钠粉末、⑧蔗糖晶体、⑨熔融氯化钠、⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是_______________ 。
(2)属于电解质的是_______________ 。
(3)属于非电解质的是_______________ 。
(4)②在水溶液中的电离方程式为_______________ 。①与②在溶液中反应使溶液呈中性的离子方程式为_______________ 。
(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)②在水溶液中的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯是一种重要的“成盐元素”,如图是几种常见的含氯产品。回答下列问题:

(1)舍勒发现氯气的方法至今还是实验室制备氯气的主要方法之一,写出该反应的离子方程式:_______ 。
(2)已知 与浓盐酸反应的化学方程式:
与浓盐酸反应的化学方程式:
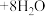 ,该反应也可以用来制取氯气,请用单线桥法标出该反应电子转移的方向和数目:
,该反应也可以用来制取氯气,请用单线桥法标出该反应电子转移的方向和数目:_____ 。
(3)实验室还可以利用反应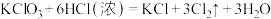 制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为
制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为_______ (以 表示阿伏加德罗常数值)。
表示阿伏加德罗常数值)。
(4)已知“84消毒液”的主要成分是次氯酸钠,在清洗卫生间时,若将“洁厕灵”(主要成分是稀盐酸)与“84消毒液”混合使用可能会发生氯气中毒事件。请从氧化还原反应的角度分析原因:_______ (用离子方程式表示)。
(5)某温度下,将氯气通入NaOH溶液中,反应得到NaCl,NaClO和 的混合溶液,经测定
的混合溶液,经测定 与
与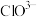 的物质的量之比为1:1,写出该反应的化学方程式:
的物质的量之比为1:1,写出该反应的化学方程式:_______ 。
(6)漂白粉的有效成分是:_______ (填化学式),新买的漂白粉没有保存说明书,请你为漂白粉设计一份保存注意事项:_______ 。

(1)舍勒发现氯气的方法至今还是实验室制备氯气的主要方法之一,写出该反应的离子方程式:
(2)已知
 与浓盐酸反应的化学方程式:
与浓盐酸反应的化学方程式:
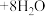 ,该反应也可以用来制取氯气,请用单线桥法标出该反应电子转移的方向和数目:
,该反应也可以用来制取氯气,请用单线桥法标出该反应电子转移的方向和数目:(3)实验室还可以利用反应
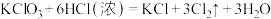 制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为
制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为 表示阿伏加德罗常数值)。
表示阿伏加德罗常数值)。(4)已知“84消毒液”的主要成分是次氯酸钠,在清洗卫生间时,若将“洁厕灵”(主要成分是稀盐酸)与“84消毒液”混合使用可能会发生氯气中毒事件。请从氧化还原反应的角度分析原因:
(5)某温度下,将氯气通入NaOH溶液中,反应得到NaCl,NaClO和
 的混合溶液,经测定
的混合溶液,经测定 与
与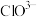 的物质的量之比为1:1,写出该反应的化学方程式:
的物质的量之比为1:1,写出该反应的化学方程式:(6)漂白粉的有效成分是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】SO2在生产、生活中具有重要的作用,据所学知识回答相关问题。
(1) SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有___________ (填“酸性”、“氧化性”、“还原性”或“漂白性”,下同),SO2通入品红溶液中,品红溶液褪色,说明SO2具有___________ 。
(2)已知SO2通入FeCl3溶液会发生反应,该反应的现象为___________ ,请写出该反应的离子方程式___________ 。
(3)向含锌粉的悬浊液中通入SO2可制备ZnS2O4
①该反应的化学方程式为___________ ,若反应中有0.1mol电子转移,则生成ZnS2O4___________ g。
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为___________ 。
(1) SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有
(2)已知SO2通入FeCl3溶液会发生反应,该反应的现象为
(3)向含锌粉的悬浊液中通入SO2可制备ZnS2O4
①该反应的化学方程式为
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知铜和浓硫酸可以在加热条件下发生反应(已配平): 。试通过计算和推理完成下面的问题
。试通过计算和推理完成下面的问题
(1)此反应中,硫酸体现了___________ 性和___________ 性。
(2)A物质可以导致酸雨的形成。A应该属于___________ 。(用字母代号填写)
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO4溶液褪色,此褪色反应中(填写化学式,下同)___________ 失去电子,氧化剂是___________ 。
 。试通过计算和推理完成下面的问题
。试通过计算和推理完成下面的问题(1)此反应中,硫酸体现了
(2)A物质可以导致酸雨的形成。A应该属于
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO4溶液褪色,此褪色反应中(填写化学式,下同)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素在周期表中的位置反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。回答下列问题:
(1)N在元素周期表中的位置为第__________ 周期__________ 族。根据元素周期律,预测酸性强弱:
______ (填“>”或“<”) 。
。
(2)S的最高化合价和最低化合价的代数和为_______ ,Se与 的反应比S与
的反应比S与 的反应
的反应______ (填“难”或“易”)。
(3) 具有较强的氧化性,
具有较强的氧化性, 具有较强的还原性,将
具有较强的还原性,将 气体通入溴水后,溶液中主要存在的离子是
气体通入溴水后,溶液中主要存在的离子是________ (填离子符号)。
(4)下列说法错误的是___________ (填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③由元素周期律可直接推断出酸性:
④HF、HCl、HBr、HI的稳定性逐渐减弱
| C | N | O | F | ||
| Si | P | S | Cl | ||
| Ge | As | Se | Br | ||
| Sn | Sb | Te | I | ||
| Pb | Bi | Po | At |

 。
。(2)S的最高化合价和最低化合价的代数和为
 的反应比S与
的反应比S与 的反应
的反应(3)
 具有较强的氧化性,
具有较强的氧化性, 具有较强的还原性,将
具有较强的还原性,将 气体通入溴水后,溶液中主要存在的离子是
气体通入溴水后,溶液中主要存在的离子是(4)下列说法错误的是
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③由元素周期律可直接推断出酸性:

④HF、HCl、HBr、HI的稳定性逐渐减弱
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求写出下列反应的化学方程式或离子方程式
(1)钢铁工业是国家工业的基础。请回答:
①写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:________________ 。
②在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。
写出铁粉和水蒸气反应的化学方程式:___________________ 。
(2)铝片放入NaOH溶液中有气体生成,写出反应的离子方程式:__________ 。
(1)钢铁工业是国家工业的基础。请回答:
①写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
②在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。
写出铁粉和水蒸气反应的化学方程式:
(2)铝片放入NaOH溶液中有气体生成,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:___________ ;
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:___________ ;
(3)制漂白粉原理:___________ ;
(4)高温下Fe与水蒸气反应:___________ 。
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:___________ ;
(6)Al粉与NaOH溶液反应:___________ ;
(7)酸性条件下,向含铬废水中加FeSO4,将 还原为Cr3+:
还原为Cr3+:___________ ;
(8)制Fe(OH)3胶体:___________ 。
I.写出下列化学方程式:
(1)向Na2O2中通入CO2:
(2)制Fe(OH)2时,白色沉淀迅速变灰绿色,最终变红褐色的反应原理:
(3)制漂白粉原理:
(4)高温下Fe与水蒸气反应:
Ⅱ.写出下列离子方程式:
(5)SO2通入碘水中:
(6)Al粉与NaOH溶液反应:
(7)酸性条件下,向含铬废水中加FeSO4,将
 还原为Cr3+:
还原为Cr3+:(8)制Fe(OH)3胶体:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钠、镁、铝、铁是四种重要的金属。请回答:
(1)钠的金属活动性比铝的______ (填“强”或“弱”)。
(2)钠与水反应,观察不到的实验现象是______ (填编号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3) 跟S在加热条件下反应,生成物的化学式为
跟S在加热条件下反应,生成物的化学式为______ 。
(4)铁在高温时与水蒸气反应的化学方程式为______ 。
(5)将镁铝合金与过量NaOH溶液反应,所得溶液中不存在的离子是______ 。
A.Na+ B.Mg2+ C.OH- D.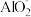
(1)钠的金属活动性比铝的
(2)钠与水反应,观察不到的实验现象是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)
 跟S在加热条件下反应,生成物的化学式为
跟S在加热条件下反应,生成物的化学式为(4)铁在高温时与水蒸气反应的化学方程式为
(5)将镁铝合金与过量NaOH溶液反应,所得溶液中不存在的离子是
A.Na+ B.Mg2+ C.OH- D.
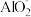
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】天然固氮的方式有生物固氮和大气固氮。大气固氮是在放电或高温下,空气中的N2转化为HNO3的过程。
(1)将下列N2转化为HNO3的过程补充完整。
N2 ①
① NO2
NO2 HNO3
HNO3
①为_______ ,②为_______ 。
A.NH3 B.NO C.N2O5 D.H2O
(2)NH4HCO3是常用的氮肥,在施用时若受热会释放出氨气而降低肥效。检验 的方法是将待检物加入到试管中,然后_______。
的方法是将待检物加入到试管中,然后_______。
(3)中国科学院科研团队研究发现,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如图。该过程实现了太阳能转化为化学能,该过程_______ (填“属于”或“不属于”)氮的固定。
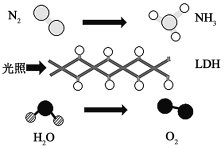
(4)上述反应中氧化剂是_______ ,被氧化的元素是_______ 。反应的化学方程式为_______ 。
(1)将下列N2转化为HNO3的过程补充完整。
N2
 ①
① NO2
NO2 HNO3
HNO3①为
A.NH3 B.NO C.N2O5 D.H2O
(2)NH4HCO3是常用的氮肥,在施用时若受热会释放出氨气而降低肥效。检验
 的方法是将待检物加入到试管中,然后_______。
的方法是将待检物加入到试管中,然后_______。| A.加热,用湿润的红色石蕊试纸放入试管口检验 |
| B.加水溶解,用红色石蕊检验其酸碱性 |
| C.加入碱溶液,加热,再滴入酚酞试液 |
| D.加入苛性钠溶液,加热,用湿润的红色石蕊试纸在试管口检验 |

(4)上述反应中氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】自然界的氮循环如图所示,回答下列问题。_____ 。
(2)如图为N2转化为HNO3的流程。
N2 NO
NO NO2
NO2 HNO3
HNO3
①上述物质颜色为红棕色的是_____ (用化学式表示)
②NO2转化为HNO3的反应中,NO2体现_____ 性。
(3)N2也可以转化为NH3,写出工业合成氨的化学方程式_____ 。
(4)稀硝酸与铜反应的还原产物为_____ 。
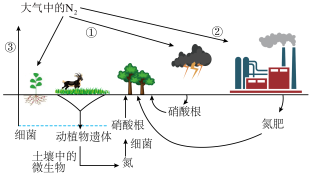
(2)如图为N2转化为HNO3的流程。
N2
 NO
NO NO2
NO2 HNO3
HNO3①上述物质颜色为红棕色的是
②NO2转化为HNO3的反应中,NO2体现
(3)N2也可以转化为NH3,写出工业合成氨的化学方程式
(4)稀硝酸与铜反应的还原产物为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:

(1)合成塔中生成NH3,说明N2具有_____ (填“氧化性”或“还原性”)。
(2)下列有关NH3的说法中,正确的是_____(填字母)。
(3)氨气在氧化炉中发生反应的化学方程式为_____ 。
(4)工厂生产出的浓硝酸可用铝槽车或铁槽车来运输,是因为在常温下,浓硝酸能使铝、铁等发生_____ 现象,说明浓硝酸具有很强的_____ 性。
(5)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出:
①下列环境问题与氮的氧化物排放有关的是_____ ;
A.酸雨 B.白色污染 C.光化学烟雾 D.温室效应
②为消除它们对环境的污染,可用NH3处理,已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为_____ 。

(1)合成塔中生成NH3,说明N2具有
(2)下列有关NH3的说法中,正确的是_____(填字母)。
| A.工业合成NH3需要在高温、高压、催化剂下进行 |
| B.NH3可用来生产碳铵和尿素等化肥 |
| C.NH3可用浓硫酸或无水氯化钙干燥 |
| D.NH3受热易分解,须置于冷暗处保存 |
(3)氨气在氧化炉中发生反应的化学方程式为
(4)工厂生产出的浓硝酸可用铝槽车或铁槽车来运输,是因为在常温下,浓硝酸能使铝、铁等发生
(5)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出:
①下列环境问题与氮的氧化物排放有关的是
A.酸雨 B.白色污染 C.光化学烟雾 D.温室效应
②为消除它们对环境的污染,可用NH3处理,已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
您最近一年使用:0次

 的系统命名为
的系统命名为 ;⑥NaH,熔化时破坏共价键的有
;⑥NaH,熔化时破坏共价键的有

