某研究小组用微生物电池模拟淡化海水,同时做电解实验,实验装置如下图所示,C、D是铂电极。
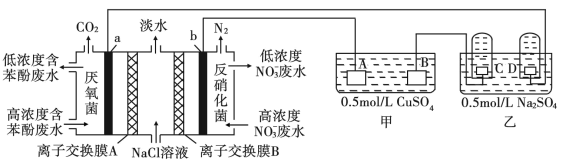
(1)若A、B是惰性电极
①D电极为_______ 极;写出C极的电极反应式_______ 。
②写出甲中总反应的离子方程式_______ 。
(2)若甲是铁片镀铜装置,A、B质量相同。A电极材料是_______ ;当B和A的质量差为12.8g时,C极产生的气体在标准状况下的体积是_______ L。

(1)若A、B是惰性电极
①D电极为
②写出甲中总反应的离子方程式
(2)若甲是铁片镀铜装置,A、B质量相同。A电极材料是
22-23高二上·山东泰安·期末 查看更多[2]
更新时间:2023/01/12 21:03:34
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请仔细观察下列几种装置的构造示意图,完成下列问题:

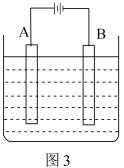
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。结合图1图2,从影响反应速率的因素分析其原因是___________ 。
(2)①已知粗锌中含有的杂质有铝、铁和铜,图3若为电解精炼锌,则A极应接____ (填“粗锌”或“纯锌”),电解一段时间后,电解质溶液中含有的金属阳离子有________ ;
②图3若为铜上镀银装置,已知电镀前A、B电极质量相等,电镀完成后两电极质量差为6.48g时,则电路中通过的电子数为___________ 。
③若图3使用的电源为一种高效耐用的新型可充电电池,其放电反应为:3Zn + 2K2FeO4 + 8H2O = 3Zn(OH)2 +2Fe(OH)3 +4KOH写出该电池放电时正极电极方程式_________ ;
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。图中a极接电源的___________ (填“正”或“负”)极,SO 放电的电极反应式为
放电的电极反应式为___________ 。




(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。结合图1图2,从影响反应速率的因素分析其原因是
(2)①已知粗锌中含有的杂质有铝、铁和铜,图3若为电解精炼锌,则A极应接
②图3若为铜上镀银装置,已知电镀前A、B电极质量相等,电镀完成后两电极质量差为6.48g时,则电路中通过的电子数为
③若图3使用的电源为一种高效耐用的新型可充电电池,其放电反应为:3Zn + 2K2FeO4 + 8H2O = 3Zn(OH)2 +2Fe(OH)3 +4KOH写出该电池放电时正极电极方程式
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。图中a极接电源的
 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,U形管内盛有100 mL 的溶液,按要求回答下列问题:

(1)打开K2,闭合K1,若所盛溶液为CuSO4溶液:则A为________ 极,A极的电极反应式为______________________ 。若所盛溶液为KCl溶液,则B极的电极反应式为________________ 。
(2)打开K1,闭合K2,若所盛溶液为滴有酚酞的NaCl溶液,则A电极附近可观察到的现象是____________________ ,Na+移向________ 极(填A、B);总反应化学方程式是____________________ 。
(3)如果要用电解的方法精炼粗铜,打开K1,闭合K2,电解液选用CuSO4溶液,则A电极的材料应换成是________ (填“粗铜”或“纯铜”),反应一段时间后电解质溶液中Cu2+的浓度将会________ (填“增大”、“减小”、“不变”)。

(1)打开K2,闭合K1,若所盛溶液为CuSO4溶液:则A为
(2)打开K1,闭合K2,若所盛溶液为滴有酚酞的NaCl溶液,则A电极附近可观察到的现象是
(3)如果要用电解的方法精炼粗铜,打开K1,闭合K2,电解液选用CuSO4溶液,则A电极的材料应换成是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电解的应用比较广泛,回答下列问题:
(1)由下列物质冶炼相应金属时采用电解法的是___________ (填字母,下同)。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是___________ 。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64 g,则转移电子数为2NA个
f.SO 的物质的量浓度不变(不考虑溶液体积变化)
的物质的量浓度不变(不考虑溶液体积变化)
(3)如图为电解精炼银的示意图,___________ (填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为___________ 。___________ (填化学式)溶液,阳极电极反应式为___________ ,电解过程中Li+向___________ (填“A”或“B”)电极迁移。___________ 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为___________ 。若改用AlCl3水溶液作电解液,则阴极产物为___________ 。
(1)由下列物质冶炼相应金属时采用电解法的是
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64 g,则转移电子数为2NA个
f.SO
 的物质的量浓度不变(不考虑溶液体积变化)
的物质的量浓度不变(不考虑溶液体积变化)(3)如图为电解精炼银的示意图,


您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铬是常见的过渡金属之一,研究铬的性质具有重要意义。回答下列问题:
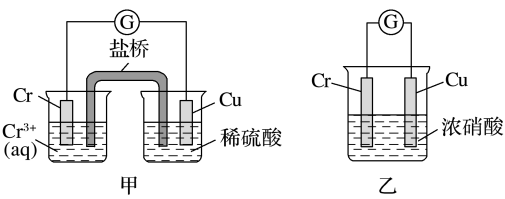
(1)在如图装置中,观察到装置甲中铜电极上产生大量的无色气体,而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由此可知,金属活动性Cr________ Cu(填“>”“<”或“=”);装置乙中正极的电极反应式为________ 。
(2)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法。将含Cr2O 的废水加入电解槽内,用石墨和铁做电极,在酸性环境中,加入适量的NaCl进行电解。
的废水加入电解槽内,用石墨和铁做电极,在酸性环境中,加入适量的NaCl进行电解。
①铁做________ 极(填“阳”或“阴”)。
②Cr2O 转化为Cr3+的离子方程式为
转化为Cr3+的离子方程式为________ 。
③阴极上Cr2O 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为______ ;若H+放电,则阴极区形成Fe(OH)3和Cr(OH)3沉淀,已知:常温下,Cr3+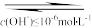 Cr(OH)3
Cr(OH)3 CrO
CrO ,则阴极区溶液pH的范围为
,则阴极区溶液pH的范围为________ 。

(1)在如图装置中,观察到装置甲中铜电极上产生大量的无色气体,而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由此可知,金属活动性Cr
(2)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法。将含Cr2O
 的废水加入电解槽内,用石墨和铁做电极,在酸性环境中,加入适量的NaCl进行电解。
的废水加入电解槽内,用石墨和铁做电极,在酸性环境中,加入适量的NaCl进行电解。①铁做
②Cr2O
 转化为Cr3+的离子方程式为
转化为Cr3+的离子方程式为③阴极上Cr2O
 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为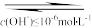 Cr(OH)3
Cr(OH)3 CrO
CrO ,则阴极区溶液pH的范围为
,则阴极区溶液pH的范围为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图是一个电化学过程的示意图。
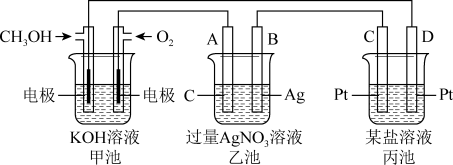
请回答下列问题:
(1)图中甲池是___________ (填“原电池”“电解池”或“电镀池”)。
(2)A(石墨)电极的名称是___________ (填“正极”“负极”“阴极”或“阳极”)。
(3)写出通入CH3OH的电极的电极反应式:___________ 。
(4)乙池中反应的化学方程式为___________ ,当乙池中B(Ag)极质量增加5.4 g,甲池中理论上消耗O2的体积为___________ L(标准状况下),此时丙池中某电极析出1.6 g某金属,则丙池中的某盐溶液可能是___________ 。
A.MgSO4溶液 B.CuSO4溶液 C.NaCl溶液 D.AgNO3溶液

请回答下列问题:
(1)图中甲池是
(2)A(石墨)电极的名称是
(3)写出通入CH3OH的电极的电极反应式:
(4)乙池中反应的化学方程式为
A.MgSO4溶液 B.CuSO4溶液 C.NaCl溶液 D.AgNO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)生活中常见的碱性锌锰电池,总反应方程式为Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH),负极反应为:_______ 。
(2)废旧的锌锰电池还含有锌和二氧化锰等物质,用稀硫酸将其溶解,转化为硫酸锌和硫酸锰,其反应的化学方程式为:Zn+MnO2+2H2SO4=ZnSO4+MnSO4+2H2O。再进行电解可以得到锌和二氧化锰。电解装置如下:
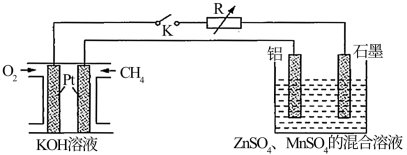
图中甲烷燃料电池负极的电极反应为_______ 。闭合开关K一段时间后,阳极附近溶液的pH_______ (填“增大”“不变”或“减小”),电解池中回收锌与MnO2的总反应离子方程式为_______ 。
(3)上述反应得到的二氧化锰可以用来制作新型的锰氢二次电池,原理示意图如图所示。
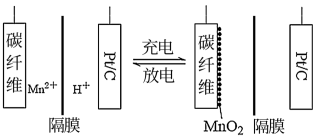
该电池以硫酸锰和硫酸的混合溶液为电解液,碳纤维和Pt/C分别作为电极材料,电池总反应式为:Mn2++2H2O MnO2+2H++H2↑。下列说法正确的是
MnO2+2H++H2↑。下列说法正确的是_______ 。
A.放电时,Pt/C电极为正极
B.放电时,电流由Pt/C电极流向碳纤维电极
C.充电时,阴极反应式为2H++2e-=H2↑
D.硫酸锰是丰富廉价工业盐,该电池成本低
(2)废旧的锌锰电池还含有锌和二氧化锰等物质,用稀硫酸将其溶解,转化为硫酸锌和硫酸锰,其反应的化学方程式为:Zn+MnO2+2H2SO4=ZnSO4+MnSO4+2H2O。再进行电解可以得到锌和二氧化锰。电解装置如下:

图中甲烷燃料电池负极的电极反应为
(3)上述反应得到的二氧化锰可以用来制作新型的锰氢二次电池,原理示意图如图所示。

该电池以硫酸锰和硫酸的混合溶液为电解液,碳纤维和Pt/C分别作为电极材料,电池总反应式为:Mn2++2H2O
 MnO2+2H++H2↑。下列说法正确的是
MnO2+2H++H2↑。下列说法正确的是A.放电时,Pt/C电极为正极
B.放电时,电流由Pt/C电极流向碳纤维电极
C.充电时,阴极反应式为2H++2e-=H2↑
D.硫酸锰是丰富廉价工业盐,该电池成本低
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某同学用如图所示装置探究在铝块表面生成氧化膜的实验, 为两种常见金属,它们的硫酸盐可溶于水。当
为两种常见金属,它们的硫酸盐可溶于水。当 闭合时,回答下列问题:
闭合时,回答下列问题:
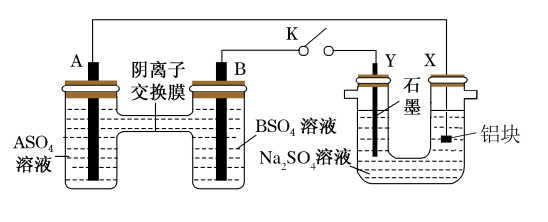
(1)①装置Ⅰ中A电极为_______ (填“正”或“负”)极,发生_______ (填“氧化”或“还原”)反应。
②在阴离子交换膜处_______ (填离子符号)从_______ (填“由右向左”或“由左向右”)移动。
(2)装置Ⅱ中, 电极上的电极反应式为
电极上的电极反应式为_______ 。
(3)当 三个电极的质量变化之比为
三个电极的质量变化之比为 时(忽略
时(忽略 电极上物质的溶解),金属
电极上物质的溶解),金属 的摩尔质量是
的摩尔质量是_______ ,金属B的元素符号是_______ 。
 为两种常见金属,它们的硫酸盐可溶于水。当
为两种常见金属,它们的硫酸盐可溶于水。当 闭合时,回答下列问题:
闭合时,回答下列问题:
(1)①装置Ⅰ中A电极为
②在阴离子交换膜处
(2)装置Ⅱ中,
 电极上的电极反应式为
电极上的电极反应式为(3)当
 三个电极的质量变化之比为
三个电极的质量变化之比为 时(忽略
时(忽略 电极上物质的溶解),金属
电极上物质的溶解),金属 的摩尔质量是
的摩尔质量是
您最近一年使用:0次




