下表中阿拉伯数字(1、2……)是元素周期表中行或列的序号。请参照元素A~I在周期表中的位置,回答下列问题。
(1)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M。写出Z与Y反应的化学方程式:_______ 。
(2)I元素在周期表中的位置是第_______ 周期、第_______ 族。
(3)实验室中采用下图所示装置模拟工业上同时制取元素A和I的单质的过程。
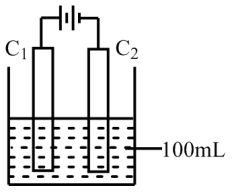
①写出电极C1上发生反应的电极反应式_______ 。
②当电极上产生112 mL(标准状况)元素I的单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=_______ 。(Kw=1.0×10-14)
纵行 横行 | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I |
(1)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1∶1和1∶2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素以原子个数之比为1∶1和1∶2形成两种离子化合物Z和M。写出Z与Y反应的化学方程式:
(2)I元素在周期表中的位置是第
(3)实验室中采用下图所示装置模拟工业上同时制取元素A和I的单质的过程。

①写出电极C1上发生反应的电极反应式
②当电极上产生112 mL(标准状况)元素I的单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=
更新时间:2023-01-14 08:59:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】随着信息技术的发展,小型化、便携式、工作寿命长的锂离子电池受到人们的青睐。某全固态薄膜锂离子电池截面结构如图1所示,集流体起导电作用;放电时电极B上发生反应的方程式为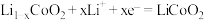 。
。

(1)放电时,电极A为_______ (填“正极”或“负极”),发生的电极反应式为_______ 。
(2)充电时,电极B上发生的电极反应式为_______ 。
(3)放电过程中,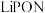 薄膜电解质中
薄膜电解质中 的物质的量会
的物质的量会_______ (填“增大”“减小”或“不变”)。
(4)若用该锂离子电池电解硫酸钠溶液制备氢气、氧气、硫酸和氢氧化钠溶液,电解装置如图2。

①离子交换膜2可选用_______ (填“阴离子交换膜”“阳离子交换膜”或“质子交换膜”)。
②D接口应与_______ (填“电极A”或“电极B)连接。
③该电解反应的化学方程式为_______ 。
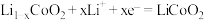 。
。
(1)放电时,电极A为
(2)充电时,电极B上发生的电极反应式为
(3)放电过程中,
 薄膜电解质中
薄膜电解质中 的物质的量会
的物质的量会(4)若用该锂离子电池电解硫酸钠溶液制备氢气、氧气、硫酸和氢氧化钠溶液,电解装置如图2。

①离子交换膜2可选用
②D接口应与
③该电解反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_________________ 。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是______________________ 。
“滤液”中的溶质主要是__________________ 。
(3)KIO3也可采用“电解法”制备,装置如图所示。

①写出电解时阴极的电极反应式________________________________ 。
②电解过程中通过阳离子交换膜的离子主要为_______________ 。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有___________________________________________ (写出一点)。
(1)KIO3的化学名称是
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是
“滤液”中的溶质主要是
(3)KIO3也可采用“电解法”制备,装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③与“电解法”相比,“KClO3氧化法”的主要不足之处有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)二氧化硫—空气质子交换膜燃料电池可以利用大气所含SO2快速启动,其装置示意图如图:

①质子的流动方向为_____ (“从A到B”或“从B到A”)。
②负极的电极反应式为_____ 。
(2)某工厂采用电解法处理含 的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,
的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水, 被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图:
被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图:

①写出电解时阴极的电极反应式________ 。
②写出 被还原为Cr3+的离子方程式
被还原为Cr3+的离子方程式______________ 。
(3)一氧化碳无色无味有毒,世界各国每年均有不少人因一氧化碳中毒而失去生命。一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。工作时,电极a作_____ 极,其电极电极反应式为_____________ ;


①质子的流动方向为
②负极的电极反应式为
(2)某工厂采用电解法处理含
 的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,
的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水, 被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图:
被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图:
①写出电解时阴极的电极反应式
②写出
 被还原为Cr3+的离子方程式
被还原为Cr3+的离子方程式(3)一氧化碳无色无味有毒,世界各国每年均有不少人因一氧化碳中毒而失去生命。一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。工作时,电极a作

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)如图所示,某同学设计了一个燃料电池探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。(甲醚
为阳离子交换膜。(甲醚 )
)
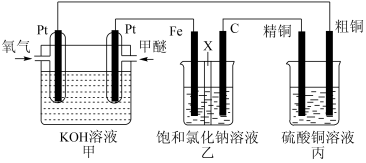
①写出甲装置中通入甲醚一极的电极反应式:___________ 。
②写出乙装置中的总反应的化学方程式:___________ 。
③电解一段时间后,丙装置中精铜质量增加9.6g,则消耗甲醚(标准状况下)体积为___________ mL。
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。(提示:放电顺序SO >OH-)
>OH-)

①图中b极要连接电源的___________ (填“正”或“负”)极。
②SO 放电的电极反应式为
放电的电极反应式为___________ 。
(1)如图所示,某同学设计了一个燃料电池探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
 为阳离子交换膜。(甲醚
为阳离子交换膜。(甲醚 )
)
①写出甲装置中通入甲醚一极的电极反应式:
②写出乙装置中的总反应的化学方程式:
③电解一段时间后,丙装置中精铜质量增加9.6g,则消耗甲醚(标准状况下)体积为
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。(提示:放电顺序SO
 >OH-)
>OH-)
①图中b极要连接电源的
②SO
 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)如图是自来水表的常见安装方式,发生腐蚀过程中,电流从___ (填“接头流向水表”或“水表流向接头”)。

(2)某二次电池放电的电池反应为2Fe+O2+2H2O=2Fe(OH)2。反应结束时,电池的负极的质量___ (“减小”“不变”或“增加”),该电池的正极反应式为___ 。
(3)有如图装置:
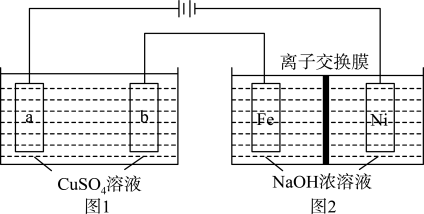
①图1中,用惰性电极电解过程中的实验数据如图,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中图1装置中产生气体的总体积(标准状况)。电解过程中转移n(e-)=0.4mol,b电极的实验现象为___ ;Q点时,a电极收集到的气体体积为___ 。

②图2中,装置通电后,溶液仍然保持澄清,铁电极附近呈紫红色(已知FeO42-在水溶液中呈紫红色),Fe电极上发生的电极反应式为___ 。
(1)如图是自来水表的常见安装方式,发生腐蚀过程中,电流从

(2)某二次电池放电的电池反应为2Fe+O2+2H2O=2Fe(OH)2。反应结束时,电池的负极的质量
(3)有如图装置:

①图1中,用惰性电极电解过程中的实验数据如图,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中图1装置中产生气体的总体积(标准状况)。电解过程中转移n(e-)=0.4mol,b电极的实验现象为

②图2中,装置通电后,溶液仍然保持澄清,铁电极附近呈紫红色(已知FeO42-在水溶液中呈紫红色),Fe电极上发生的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知图中甲池中A、B均为石墨电极,乙池中C为锌电极,D为铜电极,回答下列问题。

(1)乙池中电解质溶液为200mLCuSO4溶液,乙池为___________ (填“原电池”“电解池”),乙池中发生的化学方程式为___________ ;若把D电极换成银电极,则乙池中的反应速率会___________ 。
(2)甲池为100mLAgNO3溶液与100mLCuCl2溶液混合后的溶液,理论上两极所得气体的体积随时间变化的关系如图所示(气体体积已换算成标准状况下的体积,溶液混合过程中,体积细微变化忽略不计):

①混合前原100mLCuCl2溶液的物质的量浓度为___________ mol/L。
②t2时,甲池中所得溶液的pH=___________ ;此时乙池D增重的质量为___________ 。
③t2~t3时间段,I代表的气体为___________ 。
(3)以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,写出该电池正极电极反应式:___________ ,已知该电池的能量转换效率为86.4%,1mol甲烷燃烧释放的热量为890.3kJ,则该电池的比能量为___________ kW·h·kg-1[结果保留1位小数,比能量= ,1kW·h=3.6×106J]。
,1kW·h=3.6×106J]。

(1)乙池中电解质溶液为200mLCuSO4溶液,乙池为
(2)甲池为100mLAgNO3溶液与100mLCuCl2溶液混合后的溶液,理论上两极所得气体的体积随时间变化的关系如图所示(气体体积已换算成标准状况下的体积,溶液混合过程中,体积细微变化忽略不计):

①混合前原100mLCuCl2溶液的物质的量浓度为
②t2时,甲池中所得溶液的pH=
③t2~t3时间段,I代表的气体为
(3)以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,写出该电池正极电极反应式:
 ,1kW·h=3.6×106J]。
,1kW·h=3.6×106J]。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知A、B两种元素,A的原子序数为x,A和B所在周期的元素种类数目分别为m和n。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为___________ ,当B在A的下一周期时,B的原子序数为___________ ;
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________ ;当B在A的下一周期时,B的原子序数为___________ 。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素。
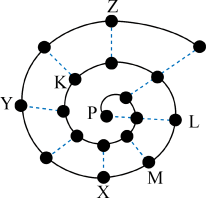
(1)X元素符号为__________________ 。
(2)M与Z两种元素形成的化合物含有的化学键为________________ 。
(3)下列说法正确的是__________________ 。
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键

(1)X元素符号为
(2)M与Z两种元素形成的化合物含有的化学键为
(3)下列说法正确的是
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】填写下列空白:
(1)已知某原子的核内有77个质子,质量数为191,则其核内的中子数为_________ 。
(2)周期表中位于第8纵行的铁元素属于第________ 族。
(3)周期表中最活泼的非金属元素位于第_____________ 纵行。
(4)所含元素为18种的周期是第____________ 周期。
(5)4g D2和20g 18O的单质化合时最多能生成_______ g D2O,这些D2O分子中含___ mol中子。
(6)氯元素在自然界中有质量数为35和37的两种核素,氯元素的相对原子质量为35.5,则两核素在自然界中的含量之比约为______________ 。
(1)已知某原子的核内有77个质子,质量数为191,则其核内的中子数为
(2)周期表中位于第8纵行的铁元素属于第
(3)周期表中最活泼的非金属元素位于第
(4)所含元素为18种的周期是第
(5)4g D2和20g 18O的单质化合时最多能生成
(6)氯元素在自然界中有质量数为35和37的两种核素,氯元素的相对原子质量为35.5,则两核素在自然界中的含量之比约为
您最近一年使用:0次



