铵明矾[NH4Al(SO4)2·12H2O]是分析化学常用基准试剂,其制备过程如图。
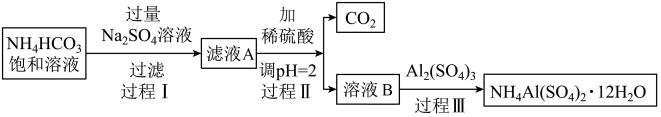
已知:过程Ⅰ的反应原理为:2NH4HCO3+Na2SO4=2NaHCO3↓+(NH4)2SO4
(1)写出过程Ⅱ中,往滤液A中加入稀H2SO4产生CO2的离子方程式_____ 。
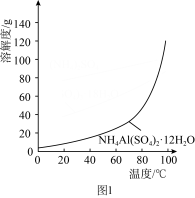
(2)过程Ⅲ中,往滤液B中,加入适量蒸馏水,加热并不断搅拌,加入适量Al2(SO4)3,_____ 、_____ 、过滤、洗涤、晾干,得到铵明矾(填具体的实验操作步骤,铵明矾的溶解度曲线如图1所示)。
(3)向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化关系如图2所示。
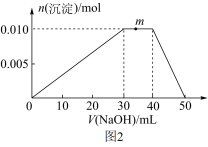
①写出m点反应的离子方程式_____ 。
②若在NH4Al(SO4)2溶液中改加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_____ mol。

已知:过程Ⅰ的反应原理为:2NH4HCO3+Na2SO4=2NaHCO3↓+(NH4)2SO4
(1)写出过程Ⅱ中,往滤液A中加入稀H2SO4产生CO2的离子方程式
(2)过程Ⅲ中,往滤液B中,加入适量蒸馏水,加热并不断搅拌,加入适量Al2(SO4)3,

(3)向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化关系如图2所示。

①写出m点反应的离子方程式
②若在NH4Al(SO4)2溶液中改加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
更新时间:2023-01-15 15:01:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】由氯元素形成的多种含氧酸盐应用于杀菌、消毒和化工领域。实验室利用下图装置(部分装置省略)制备 和NaClO并探究其氧化还原性质,回答下列问题;
和NaClO并探究其氧化还原性质,回答下列问题;
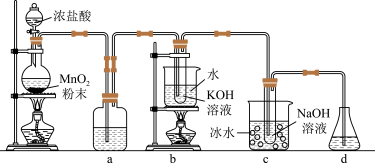
(1)盛装浓盐酸的仪器名称_______ ,圆底烧瓶中发生反应的离子方程式为_______ ,a中的试剂为_______ ,其作用是_______ 。
(2)b中采用的加热方式是_______ ,b中反应的化学方程式是_______ ,c中冰水的作用是_______ 。
(3)已知 在冷水中溶解度较小,且其溶解度随温度升高而增大,反应结束后,取出b中试管,经蒸发浓缩、
在冷水中溶解度较小,且其溶解度随温度升高而增大,反应结束后,取出b中试管,经蒸发浓缩、_______ 、过滤、_______ 、干燥,得到 晶体。
晶体。
(4)废水脱氮工艺中有一种方法是在废水中加入过量NaClO使 中的氮元素完全转化为无毒的
中的氮元素完全转化为无毒的 ,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:
,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:_______ 。
 和NaClO并探究其氧化还原性质,回答下列问题;
和NaClO并探究其氧化还原性质,回答下列问题;
(1)盛装浓盐酸的仪器名称
(2)b中采用的加热方式是
(3)已知
 在冷水中溶解度较小,且其溶解度随温度升高而增大,反应结束后,取出b中试管,经蒸发浓缩、
在冷水中溶解度较小,且其溶解度随温度升高而增大,反应结束后,取出b中试管,经蒸发浓缩、 晶体。
晶体。(4)废水脱氮工艺中有一种方法是在废水中加入过量NaClO使
 中的氮元素完全转化为无毒的
中的氮元素完全转化为无毒的 ,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:
,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】氯气是重要的化工原料。如图是实验室制取纯净、干燥氯气的装置图。_____ ,①中反应的化学方程式是_____ 。
(2)③中盛放的试剂的作用是_____ 。
(3)⑤中反应的离子方程式是_____ 。
(4)“地康法”制取氯气总反应的化学方程式为4HCl+O2=2H2O+2Cl2,其反应原理如下所示:
反应Ⅱ:……
①反应Ⅰ的离子方程式为_____ 。
②反应Ⅱ的化学方程式为_____ 。
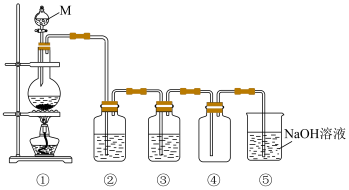
(2)③中盛放的试剂的作用是
(3)⑤中反应的离子方程式是
(4)“地康法”制取氯气总反应的化学方程式为4HCl+O2=2H2O+2Cl2,其反应原理如下所示:
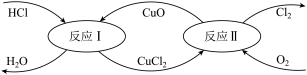
反应Ⅱ:……
①反应Ⅰ的离子方程式为
②反应Ⅱ的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】S和Te属于同主族元素,碲(Te)广泛应用于冶金、航空航天、电子等领域。从精炼钢的阳极泥(主要成分为Cu2Te,还含有金、铂等)中回收碲的工艺流程如下:
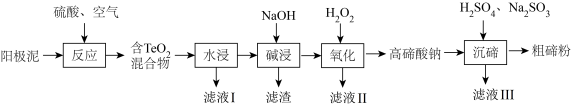
已知:TeO2具有强还原性,且TeO2、Cu2TeO4均难溶于水;高碲酸钠的化学式为Na2TeO4。
回答下列问题:
(1)Cu2Te中Te的化合价为_______ 。
(2)S和Te属于同主族元素,则稳定性:H2S_______ (填“>”或“<”)H2Te,试解释其原因:_______ 。
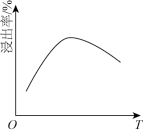
(3)“滤液I”的主要成分是_______ (写化学式);“滤液I”中溶质的浸出率与温度的关系如图所示,解释溶质的浸出率随温度变化的可能原因:_______ 。
(4)“碱浸”时发生反应的离子方程式为_______ 。
(5)粗碲粉中碲的质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为_______ ;若硫酸亚铁铵溶液使用之前部分被氧化,则测定结果_______ (填“偏高”或“偏低”)。

已知:TeO2具有强还原性,且TeO2、Cu2TeO4均难溶于水;高碲酸钠的化学式为Na2TeO4。
回答下列问题:
(1)Cu2Te中Te的化合价为
(2)S和Te属于同主族元素,则稳定性:H2S
(3)“滤液I”的主要成分是

(4)“碱浸”时发生反应的离子方程式为
(5)粗碲粉中碲的质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】无水AlCl3常用于有机合成的催化剂。现以铝酸钙(主要成分为CaO·Al2O3,含少量SiO2等杂质)和稀盐酸为原料制备无水氯化铝的方案如下:
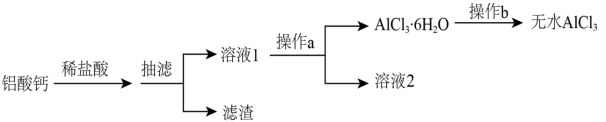
已知:AlCl3易升华,沸点181℃,SOCl2熔点﹣105℃、沸点76℃,遇水剧烈水解生成两种酸性气体。相关物质的溶解度数据如表:
按要求回答下列问题
(1)步骤①中稀盐酸应适当过量的原因是______________ 。
(2)操作a是_______________ 。
(3)操作b是_______________ 。
(4)某兴趣小组设计如图装置获取无水AlCl3。锥形瓶中得到的物质X的化学式为_________ 。碱石灰的作用是防止外界水蒸气进入和____________ 。
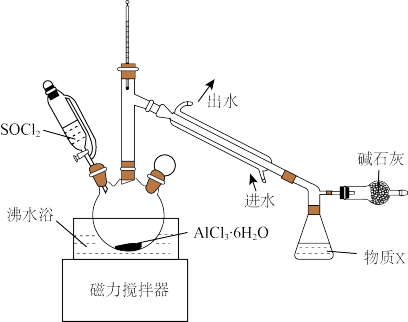
(5)写出一个化合反应(用化学方程式或离子方程式表示)________ 。要求同时满足:①其中一种反应物是AlCl3;②反应原理与“HCl+NH3=NH4Cl”相同。

已知:AlCl3易升华,沸点181℃,SOCl2熔点﹣105℃、沸点76℃,遇水剧烈水解生成两种酸性气体。相关物质的溶解度数据如表:
| 物质 | 0℃ | 80℃ |
| AlCl3 | 31.03g | 33.23g |
| CaCl2 | 37.3g | 59.5g |
(1)步骤①中稀盐酸应适当过量的原因是
(2)操作a是
(3)操作b是
(4)某兴趣小组设计如图装置获取无水AlCl3。锥形瓶中得到的物质X的化学式为

(5)写出一个化合反应(用化学方程式或离子方程式表示)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列物质(均为中学化学常见物质)转化关系如图所示,已知D为红棕色粉末(反应条件及部分反应物、产物未全部标出)。
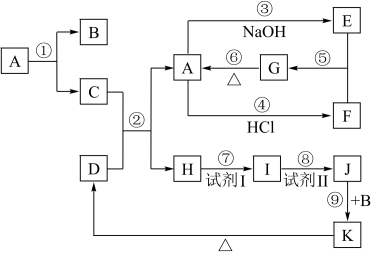
根据图示转化关系填写下列空白:
(1)写出下列物质的化学式:
A:__________ ;B:___________ ;E:_______ ;K:_______ ;
(2)C与D的混合物通常叫作________________ (填名称)。
(3)写出下列化学反应方程式(注明反应条件,若是离子反应的写离子方程式):
①______________________________ ;
②______________________________ ;
⑤______________________________ 。

根据图示转化关系填写下列空白:
(1)写出下列物质的化学式:
A:
(2)C与D的混合物通常叫作
(3)写出下列化学反应方程式(注明反应条件,若是离子反应的写离子方程式):
①
②
⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有一 无色溶液,除了水电离产生的离子外,可能还含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH 、K+、CO
、K+、CO 、SO
、SO 等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示:
等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示:
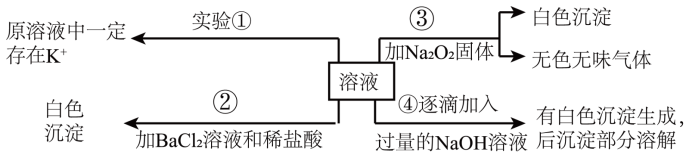
请你根据上述实验推断:
(1)实验①的名称是___________ 。
(2)原溶液中除了水电离产生的离子外一定存在的阴离子有___________ ,一定不存在的阳离子有Fe3+、Cu2+、___________ 。
(3)实验②中发生反应的离子方程式为___________ 。
(4)实验③中产生无色无味气体所发生反应的化学方程式为___________ 。
(5)写出实验④中剩余沉淀的化学式:___________ 。
(6)写出实验④中,沉淀溶解过程中所发生反应的离子方程式:___________ 。
 、K+、CO
、K+、CO 、SO
、SO 等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示:
等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示:
请你根据上述实验推断:
(1)实验①的名称是
(2)原溶液中除了水电离产生的离子外一定存在的阴离子有
(3)实验②中发生反应的离子方程式为
(4)实验③中产生无色无味气体所发生反应的化学方程式为
(5)写出实验④中剩余沉淀的化学式:
(6)写出实验④中,沉淀溶解过程中所发生反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】向20 mL某浓度的AlCl3溶液中滴加2 mol·L-1的NaOH溶液时,得到Al(OH)3沉淀的质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
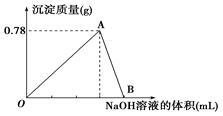
(1)图中A点表示的物质是_________ ,AlCl3溶液的浓度为___________ 。
(2)O点到B点反应的总离子方程式可表示为_______________ 。
(3)向图中B点溶液中滴加10ml 1 mol·L-1的HCl溶液,可观察到的现象是:________________________
发生的反应是__________________________
(4)若向20 mL该AlCl3溶液中加入一定体积的2 mol·L-1的NaOH溶液,生成0.39g沉淀,问加入NaOH溶液体积为_____________ 。

(1)图中A点表示的物质是
(2)O点到B点反应的总离子方程式可表示为
(3)向图中B点溶液中滴加10ml 1 mol·L-1的HCl溶液,可观察到的现象是:
发生的反应是
(4)若向20 mL该AlCl3溶液中加入一定体积的2 mol·L-1的NaOH溶液,生成0.39g沉淀,问加入NaOH溶液体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图是元素周期表的一部分,回答下列问题:

(1)元素④⑦⑧形成的简单离子,其离子半径由小到大的顺序为___________ (用离子符号表示)。
(2)推测⑤不可能具有的性质是___________(填字母)。
(3)用电子式表示①与③形成18e-化合物的电子式___________ 。
(4)由②、⑨组成的化合物分子中,②、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,写出该反应的化学方程式:___________ 。
(5)在含有①、⑥、⑦简单阳离子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:

①沉淀减少时发生的离子方程式:___________ 。
②a点的数值为:___________ mL。

(1)元素④⑦⑧形成的简单离子,其离子半径由小到大的顺序为
(2)推测⑤不可能具有的性质是___________(填字母)。
A.最高正化合价为 |
B.气态氢化物稳定性比 弱 弱 |
| C.最高价氧化物对应水化物的酸性比硝酸强 |
| D.单质在常温下可与氢气化合 |
(4)由②、⑨组成的化合物分子中,②、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,写出该反应的化学方程式:
(5)在含有①、⑥、⑦简单阳离子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:

①沉淀减少时发生的离子方程式:
②a点的数值为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】硼及其化合物在工业生产中应用广泛。用硼镁矿(主要成分Mg2B2O5.H2O)采用碳铵法生产硼酸主要流程如下:


(1)硼镁矿焙烧时需要粉碎,其目的是____________
(2)硼酸溶解度如下所示,从NH4H2BO3溶液获得硼酸晶体蒸发浓缩、冷去结晶、过滤、洗涤、干燥获得硼酸晶体。洗涤过程中需要用_______ (填“冷水”或“热水”),你的理由是____________ 。
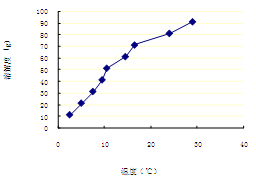
(3)测得硼酸晶体纯度的实验方法是,取0.5000g样品与锥形瓶中,加甘油和刚冷却的废水,微热使样品溶解,迅速冷却至室温,加酚酞指示剂,用NaOH标准溶液滴定至15.80ml时,溶液恰好显粉红色且半分钟不褪色。
已知:每1.00mlNaOH滴定液相当于30.92mg的H3BO3
①迅速冷却锥形瓶中溶液的方法是____________
②滴定实验中加入甘油的目的____________
③测该样品中H3BO3的质量分数为;__________


(1)硼镁矿焙烧时需要粉碎,其目的是
(2)硼酸溶解度如下所示,从NH4H2BO3溶液获得硼酸晶体蒸发浓缩、冷去结晶、过滤、洗涤、干燥获得硼酸晶体。洗涤过程中需要用

(3)测得硼酸晶体纯度的实验方法是,取0.5000g样品与锥形瓶中,加甘油和刚冷却的废水,微热使样品溶解,迅速冷却至室温,加酚酞指示剂,用NaOH标准溶液滴定至15.80ml时,溶液恰好显粉红色且半分钟不褪色。
已知:每1.00mlNaOH滴定液相当于30.92mg的H3BO3
①迅速冷却锥形瓶中溶液的方法是
②滴定实验中加入甘油的目的
③测该样品中H3BO3的质量分数为;
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】纯碱是重要化工产品,侯氏制碱法是由我国著名化学家侯德榜所创立,打破了欧美对制碱业的垄断。其简化工艺流程如下图:
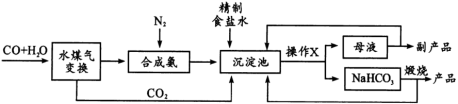
回答下列问题:
(1)高温下“水煤气变换”可制取合成氨的原料气体___________ (填化学式);沉淀池中反应的化学方程式为___________ ,该反应是否符合复分解反应发生的条件?___________ (填“是”或“否”)
(2)流程中的操作 为
为___________ ;“副产品”为___________ (填化学式)。
(3)流程中可循环利用的物质有___________ 。
(4)产品中可能混有杂质 ,设计实验检验
,设计实验检验___________ 。

回答下列问题:
(1)高温下“水煤气变换”可制取合成氨的原料气体
(2)流程中的操作
 为
为(3)流程中可循环利用的物质有
(4)产品中可能混有杂质
 ,设计实验检验
,设计实验检验
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸钾( ,
, g/mol)是一种高效多功能的绿色消毒剂,在新冠疫情期间大显身手。
g/mol)是一种高效多功能的绿色消毒剂,在新冠疫情期间大显身手。
【查阅资料】 为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生
为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生 。
。
I.湿法制备 (夹持装置略)
(夹持装置略)_______ mL浓溶液,量取所用量筒的规格是_______ (填“10mL”“25mL”或“50mL”)。若所配制的稀溶液浓度偏大,则可能的原因是_______ (填字母)。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓溶液时,仰视液面
C.未经冷却,立即转移至容量瓶定容 D.定容时,仰视液面
(2)A中发生反应的化学方程式是_______ 。
(3)下列试剂中,装置B的X溶液可以选用的是_______(填字母)。
(4)C中得到紫色固体和溶液,生成 的化学方程式是
的化学方程式是_______ 。
II.干法制备高铁酸钾分两步进行
(5)第一步反应为: ,该反应氧化剂和还原剂的物质的量之比为
,该反应氧化剂和还原剂的物质的量之比为_______ ;
第二步反应为:
(6)实验室用100mL 2.00
 溶液发生上述反应,产品经干燥后得到纯品35.0g,则
溶液发生上述反应,产品经干燥后得到纯品35.0g,则 的产率为
的产率为_______ (保留一位小数)。
 ,
, g/mol)是一种高效多功能的绿色消毒剂,在新冠疫情期间大显身手。
g/mol)是一种高效多功能的绿色消毒剂,在新冠疫情期间大显身手。【查阅资料】
 为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生
为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生 。
。I.湿法制备
 (夹持装置略)
(夹持装置略)
A.配制前,容量瓶中有少量蒸馏水 B.量取浓溶液时,仰视液面
C.未经冷却,立即转移至容量瓶定容 D.定容时,仰视液面
(2)A中发生反应的化学方程式是
(3)下列试剂中,装置B的X溶液可以选用的是_______(填字母)。
| A.饱和食盐水 | B.浓盐酸 | C.氢氧化钠溶液 | D.饱和 溶液 溶液 |
 的化学方程式是
的化学方程式是II.干法制备高铁酸钾分两步进行
(5)第一步反应为:
 ,该反应氧化剂和还原剂的物质的量之比为
,该反应氧化剂和还原剂的物质的量之比为第二步反应为:

(6)实验室用100mL 2.00

 溶液发生上述反应,产品经干燥后得到纯品35.0g,则
溶液发生上述反应,产品经干燥后得到纯品35.0g,则 的产率为
的产率为
您最近一年使用:0次



