已知几种化学键的键能和热化学方程式如下:
N2H4(g)+2Cl2(g)=N2(g)+4HCl(g) ΔH,下列推断正确的是
化学键 | H—N | N—N | Cl—Cl | N≡N | H—Cl |
| 键能(kJ∙mol-1) | 391 | 193 | 243 | 946 | 432 |
| A.H(g)+Cl(g)=HCl(g) ΔH= +432 kJ ·mol-1 |
| B.断裂 lmolH-Cl键吸收能量比断裂 1mol N≡N键多 514kJ |
| C.上述反应中,ΔH=-431 kJ·mol-1 |
| D.上述反应中,断裂极性键和非极性键,只形成极性键 |
更新时间:2023-01-24 14:59:46
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】25℃和101KPa下,H2(g)+Cl2(g)=2HCl(g)的能量变化如图所示,下列说法正确的是


| A.1molH2(g)比1molCl2(g)的能量高 |
| B.1molH2(g)和1molCl2(g)的总能量比2molHCl(g)的总能量高 |
| C.1个HCl(g)分子中的化学键断裂时需要吸收431kJ能量 |
| D.2HCl(g)=H2(g)+Cl2(g)的反应热△H=-183kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】中科院设计了一种利用 捕获气相
捕获气相 后,直接在纳米金催化剂表面加氢合成甲酸的反应,其过程如图所示。下列说法正确的是
后,直接在纳米金催化剂表面加氢合成甲酸的反应,其过程如图所示。下列说法正确的是

 捕获气相
捕获气相 后,直接在纳米金催化剂表面加氢合成甲酸的反应,其过程如图所示。下列说法正确的是
后,直接在纳米金催化剂表面加氢合成甲酸的反应,其过程如图所示。下列说法正确的是
A.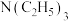 为非极性分子 为非极性分子 |
B. 被纳米金吸附后生成 被纳米金吸附后生成 放热 放热 |
C.纳米金催化剂能降低上述转化的 |
D. 转化为 转化为 中碳的杂化轨道类型发生了变化 中碳的杂化轨道类型发生了变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知一定条件下断裂或生成某些化学键的能量关系如下表:
对于反应:H2(g)+ Cl2 (g) =2HCl (g) ,下列说法错误的是
| 断裂或生成的化学键 | 能量数据 |
| 断裂1mol H2分子中的化学键 | 吸收能量436kJ |
| 断裂1mol Cl2分子中的化学键 | 吸收能量243kJ |
| 形成1mol HCl分子中的化学键 | 释放能量431kJ |
| A.该反应的反应热 △H < 0 |
| B.形成1mol HCl化学键时放热431 kJ |
| C.氯化氢分子中的化学键比氯气分子中的化学键更稳定 |
| D.相同条件下,氢气分子具有的总能量高于氯化氢分子具有的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】标准状态下,下列物质的相对能量如下表,下列说法不正确的是
| 气态物质 | H2 | O2 | H | O | HO | H2O | H2O2 |
| 能量(kJ/mol) | 0 | 0 | 218 | 249 | 39 | -242 | -136 |
| A.H2的键能为436kJ/mol |
| B.H2O2(g)=2HO(g) △H=-214kJ/mol |
| C.O2的键能大于H2O2中氧氧单键的键能的两倍 |
| D.2H2O2(g)=2H2O(g)+O2(g) △H=-212kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:
且硅晶体中每个硅原子和其他4个硅原子形成4个共价键。工业上所用的高纯硅可通过下列反应制取: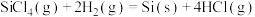 ,则该反应的反应热为
,则该反应的反应热为
| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
键能/kJ·mol | 360 | 436 | 431 | 176 |
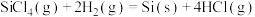 ,则该反应的反应热为
,则该反应的反应热为A.-116 kJ·mol | B.116 kJ·mol | C.-236 kJ·mol | D.236 kJ·mol |
您最近一年使用:0次
【推荐3】恒温恒容密闭容器中,一定条件发生下列反应,有关说法不正确的是
| A.反应2H2S(g)+SO2(g)=3S(s)+2H2O(1)能自发进行,说明该反应的△H<0 |
| B.反应2HS(g)+3O2(g)=2SO2(g)+2H2O(g)的△H<0,说明反应物的键能总和小于生成物的键能总和 |
| C.反应CaCO3(s)=CaO(s)+CO2(g)达平衡后,向该容器中充入少量CO2,反应再次达平衡时,c(CO2)增大 |
D.反应2SO3(g) 2SO2(g)+O2(g)达平衡后,向该容器中加入正催化剂,活化分子百分数增大,反应速率加快 2SO2(g)+O2(g)达平衡后,向该容器中加入正催化剂,活化分子百分数增大,反应速率加快 |
您最近一年使用:0次



