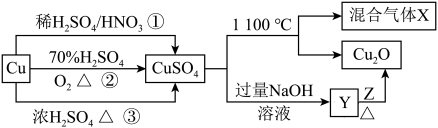
将质量为mg的Fe单质均分成两份,①第一份加入100mL稀硝酸,产生的NO标准状况下为2.688L,②另一份加入足量等浓度稀硝酸,产生标准状况下3.36LNO,下列说法正确的是
| A.m=8.4g |
| B.实验①中反应后铁有剩余 |
| C.所用硝酸的物质的量浓度为4.8mol/L |
| D.实验②发生反应后溶液中Fe2+与Fe3+物质的量之比为2:3 |
更新时间:2023-01-19 17:50:38
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】将10.7gMg、Al和Fe组成的合金溶于足量的氢氧化钠溶液中,产生标准状况下3.36L气体。另取等质量的合金溶于过量盐酸中,生成标准状况下7.84L气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀物质的量为
| A.0.1mol | B.0.2mol | C.0.25mol | D.0.3mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】为了探究FeSO4和Cu(NO3)2的混合物中各组分的含量,现设计如下流程.下列叙述中错误的是


| A.V=2240 | B.n=0.02 |
| C.原混合物中FeSO4的质量分数约为89% | D.m=0.6 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】24mL浓度为0.05mol/L的Na2SO3溶液,恰好与20mL浓度为0.02mol/L的 K2Cr2O7溶液完全反应,则元素Cr在还原产物中的化合价是( )
| A.+6 | B.+3 | C.+2 | D.0 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,22.4L庚烷中非极性键数目为6 |
B.铜电解精炼时,当阳极质量减少64g时,电路中转移电子数为2 |
C.将氯气通入 溶液中,当有 溶液中,当有 个 个 被氧化时,消耗标准状况下氯气33.6L 被氧化时,消耗标准状况下氯气33.6L |
D.0.1mol 和 和 的混合物中阴离子数目为0.1 的混合物中阴离子数目为0.1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列由相关实验现象所推断出的结论中,正确的是
| A.Cl2通入品红溶液,品红溶液褪色,说明Cl2有漂白性 |
| B.向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解,说明部分Na2SO3被氧化 |
| C.Fe与稀HNO3溶液、稀H2SO4溶液反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.向溶液中加NaOH溶液后加热,产生使湿润的蓝色石蕊试纸变红的气体,说明原溶液中含有NH4+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列离子方程式正确的是( )
A.等物质的量浓度的FeBr2和CuCl2混合溶液用惰性电极电解最初发生:Cu2+ + 2Br- Cu +Br2 Cu +Br2 |
B.Na2S溶液水解:S2— + 2H2O H2S+2OH- H2S+2OH- |
| C.Fe(NO3)3的酸性溶液中通入足量硫化氢:2Fe3++H2S=2Fe2++S↓+2H+ |
| D.H218O中投入Na2O2:2H218O+2Na2O2=4Na++4OH-+18O2↑ |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】如图表示铁与不同浓度硝酸反应时,各种还原产物的相对含量与硝酸溶液浓度的关系,从图中信息可推出下列说法不正确的是
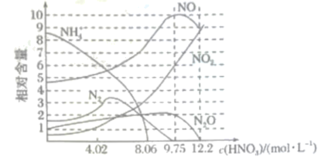

| A.硝酸与铁反应的还原产物不是单一的 |
| B.当用少量铁粉与足量的9.75mol•L-1HNO3溶液反应得到标准状况下气体2.24L,则参加反应的硝酸的物质的量为0.1mol |
| C.硝酸的浓度越大,其还原产物中高价态的N元素成分越多 |
| D.当硝酸浓度为12.2mol•L-1时,主还原产物是NO和NO2,且二者物质的量之比为1:1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】向稀硝酸中加入5.6g铁粉,铁粉完全溶解,生成 、
、 和NO气体,溶液质量增加3.2g (不考虑水的蒸发),所得溶液中
和NO气体,溶液质量增加3.2g (不考虑水的蒸发),所得溶液中 和
和 物质的量之比为( )
物质的量之比为( )
 、
、 和NO气体,溶液质量增加3.2g (不考虑水的蒸发),所得溶液中
和NO气体,溶液质量增加3.2g (不考虑水的蒸发),所得溶液中 和
和 物质的量之比为( )
物质的量之比为( )| A.4:1 | B.2:3 | C.1:1 | D.3:2 |
您最近一年使用:0次