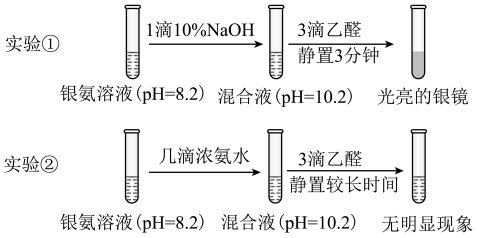
某实验小组设计如下实验探究 的制备,下列有关分析不合理的是
的制备,下列有关分析不合理的是
 的制备,下列有关分析不合理的是
的制备,下列有关分析不合理的是| 实验 | 操作 | 现象 |
| Ⅰ | 将一块 晶体浸入 晶体浸入 蒸馏水中 蒸馏水中 | 一分钟后,晶块表面仍为浅绿色,溶液呈更浅的绿色。 |
| Ⅱ | 将另一块 晶体浸入 晶体浸入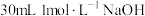 溶液中 溶液中 | 一分钟后,晶块表面变白;捞出晶块露置空气中,表面逐渐变为红褐色。 |
| Ⅲ | 将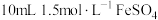 溶液与 溶液与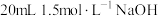 溶液混合 溶液混合 | 立即出现大量灰绿色浑浊,一分钟后,液面附近出现红褐色浑浊。 |
A.实验Ⅰ起对照作用,排除 晶体自身在水中的颜色变化 晶体自身在水中的颜色变化 |
B.实验Ⅱ晶块表面长时间保持白色,与 难溶、未分散于水有关 难溶、未分散于水有关 |
C.捞出晶块后发生了反应: |
| D.实验Ⅲ溶液中氧气含量明显多于实验Ⅱ中 |
2023·福建·一模 查看更多[2]
更新时间:2023-02-01 17:50:27
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列叙述中,错误的是
| A.离子键只存在于离子化合物中,不存在于共价化合物中 |
| B.含有共价键的化合物为共价化合物 |
| C.硫单质与金属铁反应生成硫化亚铁(FeS),体现了硫单质的氧化性 |
| D.FeCl2既有氧化性,又有还原性,不能通过铁和氯气反应制得FeCl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某溶液中含如下离子组中的几种K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-,某同学欲探究该溶液的组成进行了如下实验:
Ⅰ.用铂丝醮取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,此时溶液颜色加深,但无沉淀生成
Ⅲ.取Ⅱ反应后溶液分别置于两支试管中,第一支试管中加入BaCl2溶液有白色沉淀生成,再滴加KSCN溶液,上层清液变红,第二支试管加入CCl4,充分振荡静置后溶液分层,下层为无色。
下列说法正确的是( )
Ⅰ.用铂丝醮取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,此时溶液颜色加深,但无沉淀生成
Ⅲ.取Ⅱ反应后溶液分别置于两支试管中,第一支试管中加入BaCl2溶液有白色沉淀生成,再滴加KSCN溶液,上层清液变红,第二支试管加入CCl4,充分振荡静置后溶液分层,下层为无色。
下列说法正确的是( )
| A.原溶液中肯定不含Fe2+、NO3-、SiO32-、I- |
| B.原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- |
| C.步骤Ⅱ中无色气体是NO气体,无CO2气体产生 |
| D.为确定是否含有Cl-可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列化学用语对现象变化的解释不准确的是
A.“NO2球”浸泡在热水中,颜色加深: △H<0 △H<0 |
| B.用石墨电极电解CuSO4溶液,阴极附近溶液蓝色变浅:Cu2++2e-=Cu |
C.向FeSO4溶液中加入Br2水,溶液变为黄色: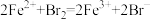 |
D.向Mg(OH)2悬浊液中滴加FeCl3溶液出现红褐色沉淀:3Mg(OH)2(s)+2Fe3+ 2Fe (OH)3(s)+3Mg2+ 2Fe (OH)3(s)+3Mg2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验现象和结论都正确且有因果关系的是
| 选项 | 操作 | 实验现象 | 结论 |
| A | 向NaHCO3溶液中滴加Na[Al(OH)4]溶液 | 有白色沉淀和气体产生 |  与 与 发生了相互促进的水解反应 发生了相互促进的水解反应 |
| B | 向某氯化亚铁溶液中加入Na2O2粉末 | 出现红褐色沉淀 | 说明原氯化亚铁已氧化变质 |
| C | 向无水乙醇中加入浓硫酸,加热至170℃,产生的气体通入酸性KMnO4溶液 | 溶液的紫色逐渐褪去 | 乙醇发生了消去反应 |
| D | 将充有NO2的密闭烧瓶放入热水中 | 烧瓶内气体颜色变深 | NO2生成N2O4的反应中,△H<0 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某废催化剂含58.2% SiO2、21.0% ZnO、4.50% ZnS和12.8% CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。设计实验流程如图:
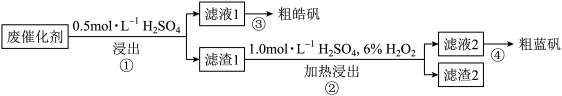
下列说法正确的是

下列说法正确的是
| A.某同学在实验完成之后,得到1.50 g CuSO4∙5H2O,则铜的回收率为30% |
| B.检验滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水 |
| C.步骤②操作中,应先加6% H2O2,再在加热搅拌下缓慢加入1.0 mol∙L−1 H2SO4 |
| D.步骤①④都需要用到蒸发皿、酒精灯、漏斗、烧杯等玻璃仪器 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】以锌焙砂(主要成分为 ,含少量
,含少量 、
、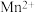 等离子)为原料制备
等离子)为原料制备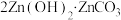 的工艺流程如下:
的工艺流程如下:
 ,含少量
,含少量 、
、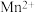 等离子)为原料制备
等离子)为原料制备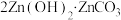 的工艺流程如下:
的工艺流程如下: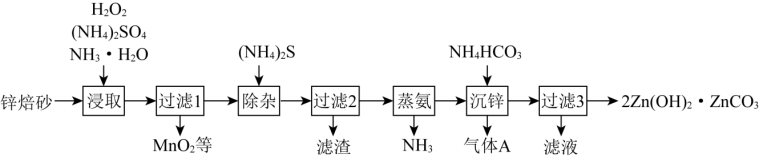
| A.“浸取”过程为加快反应速率应适当加热,但温度不宜过高 |
B.“除杂”步骤也可选择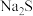 或 或 为沉淀剂,沉淀杂质离子 为沉淀剂,沉淀杂质离子 |
C.“沉锌”过程发生反应后释放的气体A为 |
D.“过滤3”所得滤液可循环使用,其主要成分的化学式是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某实验小组研究FeCl3溶液与Na2SO3溶液之间的反应,进行如下实验探究:
查阅资料:
| 编号 | 实验试剂及用量 | 开始混合时现象 | 30min时 | 3天后 |
| I | 取1.0mol/LFeCl3溶液2mL滴加1.0mol/LNa2SO3溶液2滴 | 溶液立即变为红色 | 红色明显变浅 | 溶液呈黄绿色 | |
| Ⅱ | 取1.0mol/LNa2SO3溶液2mL滴加1.0mol/LFeCl3溶液2滴 | 溶液立即变为红色,比I中略浅 | 与开始混合时一致 | 溶液呈黄绿色 |

| A.配制 FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度是为了抑制Fe3+的水解 |
| B.上述实验在开始混合时观察到的现象不涉及氧化还原反应,实验Ⅱ中红色比I中略浅的原因可能是Fe3+起始浓度小 |
| C.1~30min立即变红,随后变浅,证明生成红色配合物速率较快,红色配合物生成橙色配合物速率较慢 |
| D.取黄绿色溶液先滴加HCl溶液,再滴加BaCl2溶液,出现白色沉淀,可证明FeCl3溶液与Na2SO3溶液发生了氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是( )
| A.将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色 |
| B.将一小块钠放入盛有水的烧杯中钠在水面上游动,同时看到烧杯内的溶液变为红色 |
C.如图,一段时间后给烧杯内的溶液中加入黄色的K3[Fe(CN)6]溶液,可看到Fe电极附近有蓝色沉淀生成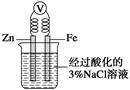 |
| D.向盛有少量Mg(OH)2沉淀悬浊液的试管中滴加氯化铵溶液,可看到沉淀溶解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验装置能达到相应实验目的的是
| 选项 | A | B | C | D |
| 实验装置 | 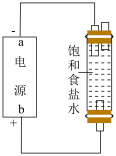 | 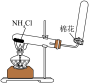 | 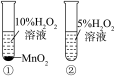 | 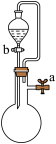 |
| 实验目的 | 电解制备家用消毒液(惰性电极) | 制备并收集氨气 | 验证MnO2是H2O2分解的催化剂 | 关闭a、打开b,可检查装置的气密性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 复合材料去除污染水体的
复合材料去除污染水体的 的反应过程(Ni不参与反应)如图所示:
的反应过程(Ni不参与反应)如图所示: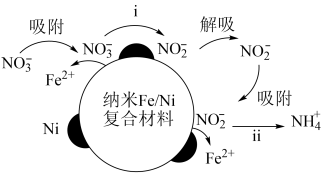
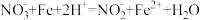

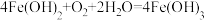

 Ag++2NH3
Ag++2NH3