有关电化学示意图如图。回答下列问题:

图1
(1)图1是工业上用电解法在强碱性条件下除去废水中的 的装置,发生的反应有
的装置,发生的反应有
ⅰ.
ⅱ.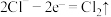
ⅲ.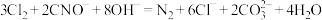
①石墨电极上发生_______ (填“氧化”或“还原”)反应;阴极反应式为_______ 。
②电解过程中有关微粒的定向移动的说法错误的是_______ (填字母)。
A.电子由电极b经导线流向铁电极
B.电流由铁电极经溶液流向石墨电极
C.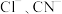 移向石墨电极
移向石墨电极
D. 移向铁电极
移向铁电极
③为了使电解池连续工作,需要不断补充_______ 。
(2)图2是一种高性能的碱性硼化钒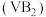 一空气电池,该电池工作时发生的离子反应
一空气电池,该电池工作时发生的离子反应 。
。
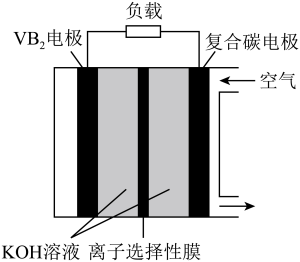
图2
① 电极为
电极为_______ 极(填“正”或“负”),电池工作时正极反应式为_______ 。
②若离子选择性膜只允许 通过,电池工作过程中,忽略溶液的体积变化,则正极室的碱性
通过,电池工作过程中,忽略溶液的体积变化,则正极室的碱性_______ (填“变大”、“变小”或“不变”)。
③放电过程中,消耗36.5 g硼化钒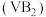 ,电路中转移
,电路中转移_______ mol电子。

图1
(1)图1是工业上用电解法在强碱性条件下除去废水中的
 的装置,发生的反应有
的装置,发生的反应有ⅰ.

ⅱ.
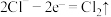
ⅲ.
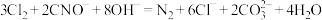
①石墨电极上发生
②电解过程中有关微粒的定向移动的说法错误的是
A.电子由电极b经导线流向铁电极
B.电流由铁电极经溶液流向石墨电极
C.
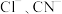 移向石墨电极
移向石墨电极D.
 移向铁电极
移向铁电极③为了使电解池连续工作,需要不断补充
(2)图2是一种高性能的碱性硼化钒
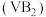 一空气电池,该电池工作时发生的离子反应
一空气电池,该电池工作时发生的离子反应 。
。
图2
①
 电极为
电极为②若离子选择性膜只允许
 通过,电池工作过程中,忽略溶液的体积变化,则正极室的碱性
通过,电池工作过程中,忽略溶液的体积变化,则正极室的碱性③放电过程中,消耗36.5 g硼化钒
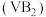 ,电路中转移
,电路中转移
更新时间:2023-02-03 17:23:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示,若电解5min时铜电极质量增加2.16g,B池的两极都有气体产生。试回答:

(1)电源电极X名称为_________ (填“正极”或“负极”)
(2)烧杯中溶液的 pH变化:(填“增大”、“减小”或“不变”)B池________________ ,C池________________ 。
(3)写出A池中所发生的电解反应方程式:_________________

(1)电源电极X名称为
(2)烧杯中溶液的 pH变化:(填“增大”、“减小”或“不变”)B池
(3)写出A池中所发生的电解反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学原理在工农业生产中有重要应用。已知N2H4是一种重要的清洁高能燃料,根据如图所示装置回答下列问题(C1~C6均为石墨电极,假设各装置在工作过程中溶液体积不变):

(1)甲装置C2电极为___________ 极(填“正”“负”“阳”或“阴”),C1电极上的电极反应式为___________ 。
(2)乙装置___________ (填“是”或“不是”)电镀池,若乙装置中溶液体积为400 mL,开始时溶液pH为6,当电极上通过0.04 mol电子时,溶液pH约为___________ 。
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱及氢气,膜X为___________ 交换膜(填“阳离子”“阴离子”或“质子”),当电极上通过0.04 mol电子时,中间硫酸钠废水的质量改变___________ g(假定水分子不能通过膜X和膜Y)。
(4)电解一段时间后,丁装置的电解质溶液中能观察到的现象是___________ ,丁装置中电解反应的总化学方程式为___________ 。

(1)甲装置C2电极为
(2)乙装置
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱及氢气,膜X为
(4)电解一段时间后,丁装置的电解质溶液中能观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天。如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导正极生成的O2-离子(O2+4e-=2O2-)。
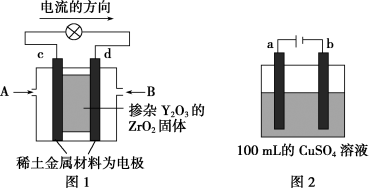
(1)c电极为___________ 极,d电极上的电极反应式为___________
(2)如图2所示为用惰性电极电解100mLCuSO4溶液,a电极上的电极反应式为___________ ;电解一段时间后,a电极产生气体,b电极不产生气体,则溶液的pH___________ (填“减小”或“增大”),要使电解质溶液恢复到电解前的状态,可加入___________ (填序号)
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
(3)在工业上,利用该电池电解NaOH溶液生产Na2FeO4,装置如图。
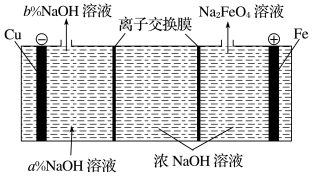
①阳极的电极反应式为___________ 。
②阴极产生的气体为___________ 。
③右侧的离子交换膜为___________ (填“阴”或“阳”)离子交换膜,阴极区a%___________ b%(填“>”“=”或“<”)。

(1)c电极为
(2)如图2所示为用惰性电极电解100mLCuSO4溶液,a电极上的电极反应式为
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
(3)在工业上,利用该电池电解NaOH溶液生产Na2FeO4,装置如图。

①阳极的电极反应式为
②阴极产生的气体为
③右侧的离子交换膜为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图是利用氯碱工业的原理图。回答下列问题:
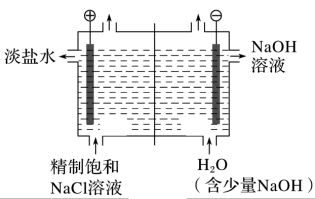
(1)请写出氯碱工业的电极反应方程式:__ ,__ 。(注明电极)
(2)图中的离子交换膜是__ (填“阳离子”或“阴离子”)交换膜,采用该离子交换膜的作用有__ (写出一点)。
(3)请写出检验左室气体产物的方法__ 。
(4)请写出NaOH在工业上的一种用途__ 。

(1)请写出氯碱工业的电极反应方程式:
(2)图中的离子交换膜是
(3)请写出检验左室气体产物的方法
(4)请写出NaOH在工业上的一种用途
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色的气体,易溶于水.
Ⅰ.ClO2可由KClO3在H2SO4存在的条件下与Na2SO3反应制得,其离子反应可表示为 (未配平).则该反应的氧化产物与还原产物的物质的量之比是
(未配平).则该反应的氧化产物与还原产物的物质的量之比是________ .
Ⅱ.实验室也可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:

(1)电解时的反应方程式为NH4Cl+2HCl 3H2↑+NCl3,写出电解时阳极电极反应
3H2↑+NCl3,写出电解时阳极电极反应________ .
(2)除去ClO2中的NH2可选用的试剂是________ (填序号).
A.饱和食盐水
B.碱石灰
C.浓硫酸
D.水
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液作指示剂,用cmol·L-1硫代硫酸钠标准溶液滴定( ),共用去VmL硫代硫酸钠溶液.
),共用去VmL硫代硫酸钠溶液.

①装置中玻璃液封管的作用除使锥形瓶内外压强相等外还能________
②请写出上述ClO2气体与碘化钾溶液反应的离子方程式:________
③判断此滴定实验达到滴定终点的方法是________ .
④因下列滴定操作不当,导致测定结果偏低的是________ .
A.用于量取待测液的滴定管用蒸馏水洗涤后,未用待测液润洗
B.滴定前,在用蒸馏水洗涤滴定管后,未用标准液润洗
C.滴定前,滴定管尖端有气泡,滴定后气泡消失
D.滴定前,没有用待测液润洗锥形瓶
E.读取标准液的刻度时,滴定前平视,滴定后俯视
Ⅰ.ClO2可由KClO3在H2SO4存在的条件下与Na2SO3反应制得,其离子反应可表示为
 (未配平).则该反应的氧化产物与还原产物的物质的量之比是
(未配平).则该反应的氧化产物与还原产物的物质的量之比是Ⅱ.实验室也可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:

(1)电解时的反应方程式为NH4Cl+2HCl
 3H2↑+NCl3,写出电解时阳极电极反应
3H2↑+NCl3,写出电解时阳极电极反应(2)除去ClO2中的NH2可选用的试剂是
A.饱和食盐水
B.碱石灰
C.浓硫酸
D.水
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液作指示剂,用cmol·L-1硫代硫酸钠标准溶液滴定(
 ),共用去VmL硫代硫酸钠溶液.
),共用去VmL硫代硫酸钠溶液.
①装置中玻璃液封管的作用除使锥形瓶内外压强相等外还能
②请写出上述ClO2气体与碘化钾溶液反应的离子方程式:
③判断此滴定实验达到滴定终点的方法是
④因下列滴定操作不当,导致测定结果偏低的是
A.用于量取待测液的滴定管用蒸馏水洗涤后,未用待测液润洗
B.滴定前,在用蒸馏水洗涤滴定管后,未用标准液润洗
C.滴定前,滴定管尖端有气泡,滴定后气泡消失
D.滴定前,没有用待测液润洗锥形瓶
E.读取标准液的刻度时,滴定前平视,滴定后俯视
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】短程硝化-厌氧氨氧化工艺的目的是将氨氮(NH )废水中的氮元素转变为N2脱除,其机理如下:
)废水中的氮元素转变为N2脱除,其机理如下:

资料:氧气浓度过高时,NO 会被氧化成NO
会被氧化成NO 。
。
(1)该工艺中NH 是被
是被___________ (填“氧化”或“还原”)的微粒。
(2)参与Ⅰ中反应的n(NH ):n(O2)=
):n(O2)=___________
(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被抑制,II中反应无法发生;还有可能是___________ 。

(4)经上述工艺处理后,排出的水中含有一定量的NO ,可以通过改进工艺提高氮的脱除率。
,可以通过改进工艺提高氮的脱除率。
①加入还原铁粉能有效除去NO 。该过程涉及的三个反应(a、b和c)如下:
。该过程涉及的三个反应(a、b和c)如下:

在整个反应过程中几乎监测不到NH 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:___________ 。
②采用微生物电解工艺也可有效除去NO ,其原理如图所示。A是电源
,其原理如图所示。A是电源___________ 极。结合电极反应式解释该工艺能提高氮的脱除率的原因:___________

 )废水中的氮元素转变为N2脱除,其机理如下:
)废水中的氮元素转变为N2脱除,其机理如下:
资料:氧气浓度过高时,NO
 会被氧化成NO
会被氧化成NO 。
。(1)该工艺中NH
 是被
是被(2)参与Ⅰ中反应的n(NH
 ):n(O2)=
):n(O2)=(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被抑制,II中反应无法发生;还有可能是

(4)经上述工艺处理后,排出的水中含有一定量的NO
 ,可以通过改进工艺提高氮的脱除率。
,可以通过改进工艺提高氮的脱除率。①加入还原铁粉能有效除去NO
 。该过程涉及的三个反应(a、b和c)如下:
。该过程涉及的三个反应(a、b和c)如下:
在整个反应过程中几乎监测不到NH
 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:②采用微生物电解工艺也可有效除去NO
 ,其原理如图所示。A是电源
,其原理如图所示。A是电源
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
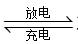
【推荐1】(1)高铁酸钾 不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为
不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为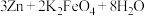
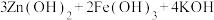 ,如图是高铁电池的模拟实验装置:
,如图是高铁电池的模拟实验装置:

①该电池盐桥中盛有饱和 溶液,此盐桥中氯离子向
溶液,此盐桥中氯离子向______ (填“左”或“右”)移动。
②该电池放电时正极的电极反应式为______ ;充电时每转移0.3mol电子,有______ mol 生成,正极附近溶液的碱性
生成,正极附近溶液的碱性______ (填“增强”,“不变”或“减弱”)。
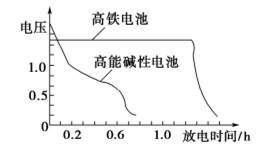
③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_________________ 。
(2)“ ”电池可将
”电池可将 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“ ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为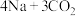

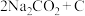 。放电时该电池“吸入”
。放电时该电池“吸入” ,其工作原理如图所示:
,其工作原理如图所示:
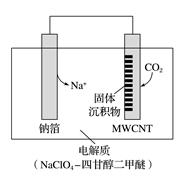
①充电时,正极的电极反应式为________________________________ 。
②放电时,若生成的 和
和 全部沉积在电极表面,当转移0.2mol
全部沉积在电极表面,当转移0.2mol 时,两极的质量差为
时,两极的质量差为______ 。
 不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为
不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为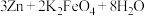

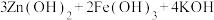 ,如图是高铁电池的模拟实验装置:
,如图是高铁电池的模拟实验装置:
①该电池盐桥中盛有饱和
 溶液,此盐桥中氯离子向
溶液,此盐桥中氯离子向②该电池放电时正极的电极反应式为
 生成,正极附近溶液的碱性
生成,正极附近溶液的碱性
③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
(2)“
 ”电池可将
”电池可将 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“ ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为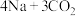

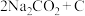 。放电时该电池“吸入”
。放电时该电池“吸入” ,其工作原理如图所示:
,其工作原理如图所示:
①充电时,正极的电极反应式为
②放电时,若生成的
 和
和 全部沉积在电极表面,当转移0.2mol
全部沉积在电极表面,当转移0.2mol 时,两极的质量差为
时,两极的质量差为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据原电池原理可以设计原电池,实现多种用途

(1) 可以用如图所示装置吸收SO2并制取硫酸,写出通入SO2和O2的电极的电极反应式及反应的总方程式。
负极________________________________
正极________________________________
总反应_________________________________________ 。
(2) 如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。

试回答下列问题:
①图中通过负载的电子流动方向________ (填“向左”或“向右”)。
②写出氢氧燃料电池工作时电极反应方程式。
正极:_________________________ ,负极:____________________________ ,
③若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,
正极反应式为__________________________________________________ ;
负极反应式为__________________________________________________ 。

(1) 可以用如图所示装置吸收SO2并制取硫酸,写出通入SO2和O2的电极的电极反应式及反应的总方程式。
负极
正极
总反应
(2) 如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。

试回答下列问题:
①图中通过负载的电子流动方向
②写出氢氧燃料电池工作时电极反应方程式。
正极:
③若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,
正极反应式为
负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氨和铵盐用途广泛。
(1)工业合成氨的反应是 N2+3H2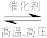 2NH3 。
2NH3 。
① 一定温度下,在某500mL的密闭容器中充入3mol H2 和 1 mol N2,3min后反应达平衡,H2的物质的量为0.75mol,求
a. H2的转化率,___________
b.平衡时NH3的体积分数___________ 。(写出计算过程)
② 对上述反应,下列说法不正确的是___________
A.正反应方向和逆反应方向均能进行的化学反应统称为可逆反应
B.当可逆反应的正反应速率和逆反应速率相等时,该反应达到化学平衡状态
C.化学反应的限度决定了反应物在该条件下的最大转化率
D.改变可逆反应的反应条件可以在一定程度上改变其化学平衡状态
(2)已知日常所用的干电池中,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作为电解质,电极反应可简化为2NH + 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
+ 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是___________ ,负极是___________ 。当生成25.5克NH3时,转移___________ mol电子。
(1)工业合成氨的反应是 N2+3H2
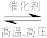 2NH3 。
2NH3 。① 一定温度下,在某500mL的密闭容器中充入3mol H2 和 1 mol N2,3min后反应达平衡,H2的物质的量为0.75mol,求
a. H2的转化率,
b.平衡时NH3的体积分数
② 对上述反应,下列说法不正确的是
A.正反应方向和逆反应方向均能进行的化学反应统称为可逆反应
B.当可逆反应的正反应速率和逆反应速率相等时,该反应达到化学平衡状态
C.化学反应的限度决定了反应物在该条件下的最大转化率
D.改变可逆反应的反应条件可以在一定程度上改变其化学平衡状态
(2)已知日常所用的干电池中,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作为电解质,电极反应可简化为2NH
 + 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
+ 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
您最近一年使用:0次



