下图为元素周期表的一部分,请参照① ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
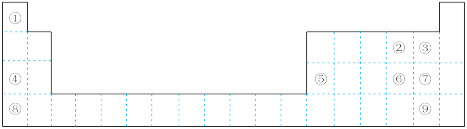
(1)最高价氧化物对应水化物碱性最强的是_______ (填化学式),氢化物热稳定性最强的是_______ (填电子式)。
(2)②③④的原子半径从大到小的顺序是_______ (填元素符号)。④⑤⑧的阳离子中氧化性最强的是_______ (填离子符号)。
(3)元素⑥的非金属性比⑦_______ (填“强”或“弱”),请从原子结构的角度解释:_______ 。
(4)现在含有元素硒( )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为_______ ,则下列叙述中正确的是_______ 。
A.原子序数为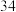
B.气态氢化物的稳定性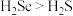
C. 不能与氢氧化钠反应
不能与氢氧化钠反应
D. 既有氧化性又有还原性
既有氧化性又有还原性
(5)①和④可形成 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为_______ ,其与水反应放出气体的化学方程式为_______ 。
 ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
(1)最高价氧化物对应水化物碱性最强的是
(2)②③④的原子半径从大到小的顺序是
(3)元素⑥的非金属性比⑦
(4)现在含有元素硒(
 )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为A.原子序数为
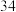
B.气态氢化物的稳定性
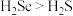
C.
 不能与氢氧化钠反应
不能与氢氧化钠反应D.
 既有氧化性又有还原性
既有氧化性又有还原性(5)①和④可形成
 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为
更新时间:2023-02-05 10:09:46
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】在化学学习过程中,我们常用化学用语表示物质的组成、结构和变化。为了简便起见,我们用电子式表示物质的形成过程。
问题:为什么可用电子式表示物质的形成过程___ ?
问题:为什么可用电子式表示物质的形成过程
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】写出下列原子的电子式:
(1)O_____ ;
(2)Al_____ ;
(3)Si_____ ;
(4)Cl_____ 。
(1)O
(2)Al
(3)Si
(4)Cl
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】如表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
(1)金属性最强的元素是_______ ;
(2)F的原子结构示意图是________ ;
(3)地壳中含量最多的元素是_______ ;
(4)Ne原子的最外层电子数是_______ ;
(5)N与O原子半径较大的是_______ ;
(6)H2S与HCl热稳定性较弱的是______ ;
(7)Na2O与MgO难与水反应的是______ ;
(8)Mg(OH)2与Al(OH)3能与强碱反应的是______ ;
(9)用于制造光导纤维的物质是______ (填“Si”或“SiO2”);
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为____ ,HClO不稳定,易分解生成HCl和O2,写出其在光照条件下分解的化学方程式:____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | N | O | F | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)金属性最强的元素是
(2)F的原子结构示意图是
(3)地壳中含量最多的元素是
(4)Ne原子的最外层电子数是
(5)N与O原子半径较大的是
(6)H2S与HCl热稳定性较弱的是
(7)Na2O与MgO难与水反应的是
(8)Mg(OH)2与Al(OH)3能与强碱反应的是
(9)用于制造光导纤维的物质是
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某元素R有4个电子层,最外层上有5个电子,指出:
(1)R在第____________ 周期,第____________ ,元素符号____________ 。
(2)R的最高正价____________ ,负价_____________ ,最高价氧化物化学式____________ ,对应水化物化学式____________ ,氢化物化学式____________ 。
(1)R在第
(2)R的最高正价
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,表中字母分别代表一种元素。回答下列问题。
(1)表中所标元素,最活泼的金属元素形成简单离子符号为____ ;最不活泼的元素的原子结构示意图为 _____ ;其中一种元素的气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐,该盐是_______ 。
(2)写出两种满足下列条件的物质______ (写化学式)。
①由c、x、e组成的;②含有共价键的离子化合物。
(3)g、x、y的气态氢化物,最稳定的是______ (填化学式)。
(4)表中元素的最高价氧化物的水化物中:酸性最强的是______ (填化学式,下同);碱性最强的是_______ ,这两种物质反应的离子方程式为_________ 。
(5)推测元素的非金属性:a______ g(填“>”或“<”)。利用图装置设计实验,证明推测结论。

①仪器A的名称为___________ ,干燥管D的作用是______________ 。
②填空。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | b | c | d | ||||
| 3 | e | f | g | x | y | z |
(2)写出两种满足下列条件的物质
①由c、x、e组成的;②含有共价键的离子化合物。
(3)g、x、y的气态氢化物,最稳定的是
(4)表中元素的最高价氧化物的水化物中:酸性最强的是
(5)推测元素的非金属性:a

①仪器A的名称为
②填空。
| 装置内试剂 | C中发生反应的化学方程式 | ||
| A | B | C | |
| 稀硫酸 | 碳酸钠 | ||
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室加热液体时常加入沸石,其主要成分为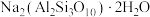 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:
(1)元素Si在周期表中的位置是_______ 。
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式);Na与同周期非金属性最强的元素形成的化合物可做调味品,用电子式表示该化合物的形成过程_______ 。
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是_______ (填化学式)。
(4)Na所在周期的主族元素中,简单离子半径最小的是_______ (填离子符号)
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
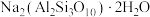 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:(1)元素Si在周期表中的位置是
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是
(4)Na所在周期的主族元素中,简单离子半径最小的是
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)鉴于 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的_______ 族。
(2)甲元素 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是_______ (填元素名称),写出可以验证该结论的一个化学方程式:_______ 。
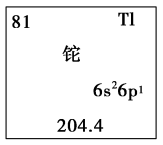
(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。
(1)鉴于
 的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的(2)甲元素
 层上7个电子,甲元素与硫元素相比,非金属性较强的是
层上7个电子,甲元素与硫元素相比,非金属性较强的是(3)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如图所示。下列叙述不正确的是_______(填字母)。

| A.铊元素在元素周期表中的位置是第六周期第ⅡA族 |
B.铊原子的中子数为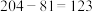 |
| C.铊原子有6个电子层,最外电子层上有3个电子 |
| D.铊元素的金属性比铝元素的强 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白:
(1)这11种元素中化学性质最不活泼的是_______ ,金属性最强的是_______ 。(写元素符号)
(2)第三周期元素中,单质氧化性最强的元素是_______ 。(写元素符号)
(3)J的简单离子的结构示意图_______ ,D和G所形成的化合物,阴、阳离子个数比为_______ 。
(4)比较G、H两元素的最高价氧化物对应水化物的酸性_______ >_______ 。比较C、G两元素的气态氢化物稳定性_______ >_______ 。(写化学式)
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
一 | A | |||||||
二 | B | C | ||||||
三 | D | E | F | G | H | I | ||
四 | K | J | ||||||
(2)第三周期元素中,单质氧化性最强的元素是
(3)J的简单离子的结构示意图
(4)比较G、H两元素的最高价氧化物对应水化物的酸性
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
(1)④、⑤、⑥的原子半径由大到小的顺序是_____ 。(用元素符号表示)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是____ 。
(3)③、④、⑥元素可形成含10个电子的微粒,其中A和B为分子,C和E为阳离子,D为阴离子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。用电子式表示下列4种微粒:A_____ 、B____ 、C_____ 、D____ 。并写出A、B、E三种微粒反应的离子方程式________ 。
(4)由④⑤⑧三种元素组成的某种盐是家用消毒液的主要成分,将该盐溶液滴入KI淀粉溶液中溶液变为蓝色,则反应的离子方程式为__________ 。

(1)④、⑤、⑥的原子半径由大到小的顺序是
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)③、④、⑥元素可形成含10个电子的微粒,其中A和B为分子,C和E为阳离子,D为阴离子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。用电子式表示下列4种微粒:A
(4)由④⑤⑧三种元素组成的某种盐是家用消毒液的主要成分,将该盐溶液滴入KI淀粉溶液中溶液变为蓝色,则反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】元素周期表的一部分,按要求完成各小题。
(1)金属性最强的单质与水反应的离子方程式为____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是____ 。
(3)①③⑤三种元素的原子半径由大到小的顺序为____ 。
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是____ 。向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH至过量,现象为____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是
(3)①③⑤三种元素的原子半径由大到小的顺序为
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是
您最近一年使用:0次



