某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成再加入过量的稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是_______ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有_______ ,写出生成该白色沉淀的离子方程式为_______ 。
(4)原溶液可能大量共存的阴离子是_______(填字母)。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成再加入过量的稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是_______(填字母)。
| A.OH— | B. | C. | D.Cl— |
21-22高一上·天津·期中 查看更多[11]
天津市五校联考2021-2022学年高一上学期期中考试化学试题福建省连城县第一中学2021-2022学年高一上学期第二次月考化学试题(已下线)1.2.3 离子方程式正误判断与离子共存-2022-2023学年高一化学上学期课后培优分级练 (人教版2019必修第一册)福建省莆田锦江中学2022-2023学年高三上学期第一次月考化学试题河北省石家庄市第十五中学2022-2023学年高一上学期十月月考化学试题山东省莒南第一中学2022-2023学年高一上学期期中考试化学试题天津市八校联考2022-2023学年高一上学期期中考试化学试题湖南省怀化市中方县第一中学2022-2023学年高一上学期9月份月考化学试题四川省天府新区太平中学2022-2023学年高一上学期期中考试化学试题四川省广元中学2022-2023学年高一上学期第一次段考化学试题湖北省襄阳市第一中学2023-2024学年高一上学期9月月考化学试题
更新时间:2023/02/07 13:15:03
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D为四种可溶性的盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO3-、SO42-、Cl-、CO32-中的一种。(离子在物质中不能重复出现)
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断它们的化学式为:
(1)A________ ,C________ ,D____________ 。
(2)写出盐酸与D反应的离子方程式:___________________________ 。
(3)写出C与Ba(OH)2溶液反应的离子方程式:_______________________ 。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断它们的化学式为:
(1)A
(2)写出盐酸与D反应的离子方程式:
(3)写出C与Ba(OH)2溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某无色透明溶液中可能存在大量Ag+、Mg2+、Fe3+、Cu2+中的一种或几种,请填写下列空白。
(1)不用做任何实验就可以肯定溶液中不存在的离子是________________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是________ ,有关反应的离子方程式为________________ 。
(3)取(2)的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有________ ,有关反应的离子方程式为________________ 。
(4)原溶液中可能大量存在的阴离子是________ (填序号)。
A.Cl- B. C.
C. D.OH-
D.OH-
(1)不用做任何实验就可以肯定溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
(3)取(2)的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液中可能大量存在的阴离子是
A.Cl- B.
 C.
C. D.OH-
D.OH-
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】在Na+浓度为0.5 mol·L-1的某澄清溶液中,还可能含有下表中的若干种离子。(已知H2SiO3为不溶于水的胶状沉淀,加热时易分解为固体SiO2和H2O)
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
请回答下列问题。
(1)实验Ⅰ能确定一定不存在的离子是___________ ;
(2)实验Ⅰ中生成气体的离子方程式为____________________________________ ;
(3)通过实验Ⅰ、Ⅱ、Ⅲ,写出SiO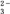 物质的量浓度的计算过程
物质的量浓度的计算过程_______ 。
(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由_______ 。
| 阳离子 | K+ | Ag+ | Ca2+ | Ba2+ |
| 阴离子 | NO | CO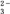 | SiO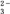 | SO |
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色胶状沉淀并放出标准状况下0.56 L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4 g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
(1)实验Ⅰ能确定一定不存在的离子是
(2)实验Ⅰ中生成气体的离子方程式为
(3)通过实验Ⅰ、Ⅱ、Ⅲ,写出SiO
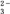 物质的量浓度的计算过程
物质的量浓度的计算过程(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】MnO2是实验室常用试剂,可用于制备多种气体。
Ⅰ.利用MnO2制备氯气。实验室制取纯净、干燥的氯气的装置如图。
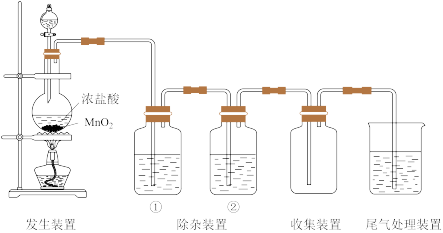
(1)实验室制取Cl2的化学方程式是_______ 。
(2)除杂装置②中的试剂是_______ 。
(3)检验尾气处理装置中含有的Cl-的方法是:取少量烧杯中溶液,_______ 。
(4)氯气溶于水形成氯水,氯水通常保存在棕色瓶中,因为光照条件下容易变质。用传感器分析氯水在光照过程中微粒成分的变化,得到以下图像,其中不合理 的是_______。
Ⅱ.利用制备氧气
(5)实验室加热MnO2和KClO3的固体混合物制取O2,同时生成KCl,反应中MnO2是催化剂,化学方程式是_______ 。
(6)用该方法中得到的O2有刺激性气味,推测反应生成了Cl2,反应的化学方程式:2KClO3+2MnO2=K2Mn2O8+Cl2↑+O2↑。该反应每转移1mol电子,生成标准状况下O2的体积为_______ L。
Ⅰ.利用MnO2制备氯气。实验室制取纯净、干燥的氯气的装置如图。

(1)实验室制取Cl2的化学方程式是
(2)除杂装置②中的试剂是
(3)检验尾气处理装置中含有的Cl-的方法是:取少量烧杯中溶液,
(4)氯气溶于水形成氯水,氯水通常保存在棕色瓶中,因为光照条件下容易变质。用传感器分析氯水在光照过程中微粒成分的变化,得到以下图像,其中
A.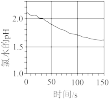 | B.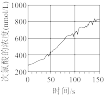 | C.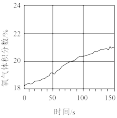 | D.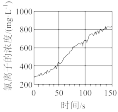 |
Ⅱ.利用制备氧气
(5)实验室加热MnO2和KClO3的固体混合物制取O2,同时生成KCl,反应中MnO2是催化剂,化学方程式是
(6)用该方法中得到的O2有刺激性气味,推测反应生成了Cl2,反应的化学方程式:2KClO3+2MnO2=K2Mn2O8+Cl2↑+O2↑。该反应每转移1mol电子,生成标准状况下O2的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】随着新能源汽车销量逐年攀升,动力电池的制备和回收利用技术至关重要。利用含 的锂电池废料回收制备
的锂电池废料回收制备 的流程图如下:
的流程图如下:
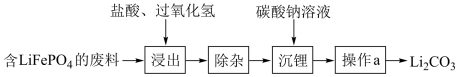
(1)含 的废料在浸出操作之前要进行粉碎,其作用是
的废料在浸出操作之前要进行粉碎,其作用是_______ 。
(2)浸出过程中温度不宜高于40℃,原因是_______ 。
(3)操作a的名称为_______ 。
(4)欲证明 产品中是否含LiCl,简述实验方法(包括步骤、试剂、现象和结论等)
产品中是否含LiCl,简述实验方法(包括步骤、试剂、现象和结论等)_______ °
(5)工业通过处理含 的废旧电池正极材料可以回收Li,Li可用于空气中
的废旧电池正极材料可以回收Li,Li可用于空气中 的固定,其工作原理为:
的固定,其工作原理为: 。该电池的正极反应式为
。该电池的正极反应式为_______ 。反应中当有3 mol氧化剂被还原,通过交换膜的 的物质的量为
的物质的量为_______ mol。
 的锂电池废料回收制备
的锂电池废料回收制备 的流程图如下:
的流程图如下:
(1)含
 的废料在浸出操作之前要进行粉碎,其作用是
的废料在浸出操作之前要进行粉碎,其作用是(2)浸出过程中温度不宜高于40℃,原因是
(3)操作a的名称为
(4)欲证明
 产品中是否含LiCl,简述实验方法(包括步骤、试剂、现象和结论等)
产品中是否含LiCl,简述实验方法(包括步骤、试剂、现象和结论等)(5)工业通过处理含
 的废旧电池正极材料可以回收Li,Li可用于空气中
的废旧电池正极材料可以回收Li,Li可用于空气中 的固定,其工作原理为:
的固定,其工作原理为: 。该电池的正极反应式为
。该电池的正极反应式为 的物质的量为
的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。

资料:沉淀池中的反应为NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(1)操作1的名称为___________ ;煅烧炉中反应的化学方程式为___________ 。
(2)物质X可循环利用,其化学式为___________ 。
(3)某同学提出制得的纯碱中可能含有氯化钠,请设计实验鉴别:___________ (写出步骤、现象和结论)。

资料:沉淀池中的反应为NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(1)操作1的名称为
(2)物质X可循环利用,其化学式为
(3)某同学提出制得的纯碱中可能含有氯化钠,请设计实验鉴别:
您最近一年使用:0次
【推荐1】某同学设计了如图所示的实验装置探究将SO2、Cl2同时通入水中发生的反应。

(1)H装置中主要发生的离子方程式为__ ,I仪器的作用是__ 。
(2)若H中Cl2和SO2恰好完全反应,为了检验溶液中的阴离子,补充完整实验操作,并写出结论:取少量H中溶液于洁净的试管中,__ 。

(1)H装置中主要发生的离子方程式为
(2)若H中Cl2和SO2恰好完全反应,为了检验溶液中的阴离子,补充完整实验操作,并写出结论:取少量H中溶液于洁净的试管中,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】草酸亚铁晶体(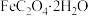 )可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:
)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:

(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是_______ 。
(2)“转化”在下图所示的装置中进行。导管A的作用是_______ 。
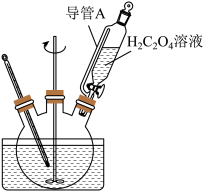
(3)检验“洗涤”完全的实验操作是_______ 。
(4)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓 、磷酸,用
、磷酸,用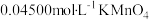 标准溶液滴定至终点(草酸亚铁转化为
标准溶液滴定至终点(草酸亚铁转化为 和CO2),消耗
和CO2),消耗 标准溶液
标准溶液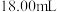 。(
。(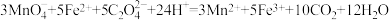 )计算样品中
)计算样品中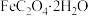 的纯度
的纯度_______ (写出计算过程)。
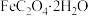 )可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:
)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如图:
(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是
(2)“转化”在下图所示的装置中进行。导管A的作用是

(3)检验“洗涤”完全的实验操作是
(4)测定草酸亚铁样品纯度的方法如下:准确称取0.2500g样品,加入适量水、浓
 、磷酸,用
、磷酸,用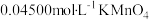 标准溶液滴定至终点(草酸亚铁转化为
标准溶液滴定至终点(草酸亚铁转化为 和CO2),消耗
和CO2),消耗 标准溶液
标准溶液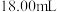 。(
。(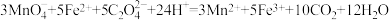 )计算样品中
)计算样品中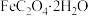 的纯度
的纯度
您最近一年使用:0次
【推荐3】草木灰中富含钾盐,主要成分是碳酸钾,还含有少量氯化钾和硫酸钾。现从草木灰中提取钾盐,并用实验检验其中的CO 、SO
、SO 和Cl-,从草木灰中提取钾盐的实验操作顺序如下:①称量样品,②溶解沉降,③过滤,④蒸发,⑤冷却结晶。
和Cl-,从草木灰中提取钾盐的实验操作顺序如下:①称量样品,②溶解沉降,③过滤,④蒸发,⑤冷却结晶。
(1)在进行②③④操作时,都要用到玻璃棒,其作用分别是:②__________ ;③__________ ;④_________ 。
(2)将制得的少量晶体放入试管,加蒸馏水溶解并把溶液分成三份,分装在3支试管里。
①在第一支试管里加入稀盐酸,可观察有____________ 生成,证明溶液中有___________ 离子。
②在第二支试管里加入足量稀盐酸后,再加入BaCl2溶液,可观察到有______ 生成,证明溶液中有____ 离子。
③在第三支试管里加入足量Ba(NO3)2溶液,过滤后,再向滤液中加入足量稀硝酸后,再加入AgNO3溶液,可观察到有沉淀生成,证明溶液中有________ 离子。
 、SO
、SO 和Cl-,从草木灰中提取钾盐的实验操作顺序如下:①称量样品,②溶解沉降,③过滤,④蒸发,⑤冷却结晶。
和Cl-,从草木灰中提取钾盐的实验操作顺序如下:①称量样品,②溶解沉降,③过滤,④蒸发,⑤冷却结晶。(1)在进行②③④操作时,都要用到玻璃棒,其作用分别是:②
(2)将制得的少量晶体放入试管,加蒸馏水溶解并把溶液分成三份,分装在3支试管里。
①在第一支试管里加入稀盐酸,可观察有
②在第二支试管里加入足量稀盐酸后,再加入BaCl2溶液,可观察到有
③在第三支试管里加入足量Ba(NO3)2溶液,过滤后,再向滤液中加入足量稀硝酸后,再加入AgNO3溶液,可观察到有沉淀生成,证明溶液中有
您最近一年使用:0次



