某无色透明溶液中可能存在大量Ag+、Mg2+、Fe3+、Cu2+中的一种或几种,请填写下列空白。
(1)不用做任何实验就可以肯定溶液中不存在的离子是________________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是________ ,有关反应的离子方程式为________________ 。
(3)取(2)的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有________ ,有关反应的离子方程式为________________ 。
(4)原溶液中可能大量存在的阴离子是________ (填序号)。
A.Cl- B. C.
C. D.OH-
D.OH-
(1)不用做任何实验就可以肯定溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
(3)取(2)的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液中可能大量存在的阴离子是
A.Cl- B.
 C.
C. D.OH-
D.OH-
16-17高一下·新疆·开学考试 查看更多[19]
江西省吉安市遂川中学2021-2022学年高一上学期第一次月考化学(B卷)试题黑龙江省绥化市望奎县第一中学2021-2022学年高一上学期第一次月考化学试题山西省大同市平城中学校2021-2022学年高一上学期10月月考化学试题湖北省麻城市实验高级中学2021-2022学年高一上学期9月月考化学试题湖南省长沙市浏阳市第三中学2019-2020学年高一上学期12月月考化学试题江苏省南京市外国语学校2020-2021学年高一上学期化学10月月考化学试卷湖南省娄底市春元中学2020-2021学年高一上学期第一次月考化学试题河北省石家庄外国语学校2020-2021学年高一上学期第二阶段考试化学试卷湖南省娄底市第一中学2020-2021学年高一上学期期中考试化学试题湖南常德市桃花源风景名胜区第一中学2020-2021学年高一上学期期中考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2020-2021学年高一(德强班)10月月考化学试题高一必修第一册(苏教2019版)专题3 第二单元 金属钠及钠的化合物 课时3 离子反应鲁科版(2019)高一必修第一册第二章第2节 电解质的电离 离子反应 课时2 离子反应人教版(2019)高一必修第一册第一章 物质及其变化 第二节 离子反应 课时2 离子反应及其发生的条件2019-2020学年高一上学期期末复习《新题速递·化学》12月(考点12-15)云南省曲靖市会泽县茚旺高级中学2019-2020学年高一上学期期中考试化学试题辽宁省大连海湾高级中学2019-2020学年高一上学期第一次质量检测化学试题天津市静海区瀛海学校等四校2019-2020学年高一11月联考化学试题2016-2017学年新疆兵团农二师华山中学高一下学期学前考试化学试卷
更新时间:2021-01-13 10:57:49
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有五瓶损坏标签的试剂,分别盛有硫酸溶液、氢氧化钾溶液、硝酸钡溶液、碳酸氢钠溶液、氯化铜溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E。观察发现,C试剂颜色为蓝色,其余为无色;几种试剂用小试管各取少量,两两相互滴加,反应现象为:A与其余三种混合无明显现象,B与D出现白色沉淀,B与E无明显现象,D与E混合有气泡产生,A与C混合有蓝色沉淀。
(1)下列试剂瓶中所盛试剂为(用溶质的化学式表示):A____ ,B____ ,E____ 。
(2)写出D与E反应的化学反应方程式:___ 。
(1)下列试剂瓶中所盛试剂为(用溶质的化学式表示):A
(2)写出D与E反应的化学反应方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某溶液的溶质只可能由下列离子中的几种组成:Cl—、CO 、SO
、SO 、H+、Ba2+、Na+,某同学进行了如下实验:
、H+、Ba2+、Na+,某同学进行了如下实验:
①向溶液中加入过量的BaCl2溶液,有白色沉淀生成,过滤;
②向①中滤液加入AgNO3溶液,有白色沉淀产生;
③将①的沉淀加入稀盐酸中,沉淀部分消失,有气体生成。
依据以上实验可以推断:(填化学式)
(1)原溶液中一定含有___________ ;一定没有___________ ;可能含有___________ 。
(2)②中生成的沉淀是___________ ;③中反应的离子方程式是___________ 。
 、SO
、SO 、H+、Ba2+、Na+,某同学进行了如下实验:
、H+、Ba2+、Na+,某同学进行了如下实验:①向溶液中加入过量的BaCl2溶液,有白色沉淀生成,过滤;
②向①中滤液加入AgNO3溶液,有白色沉淀产生;
③将①的沉淀加入稀盐酸中,沉淀部分消失,有气体生成。
依据以上实验可以推断:(填化学式)
(1)原溶液中一定含有
(2)②中生成的沉淀是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】为探究某固体化合物X(仅含三种元素)的组成和性质,设计并完成如图实验,请回答:
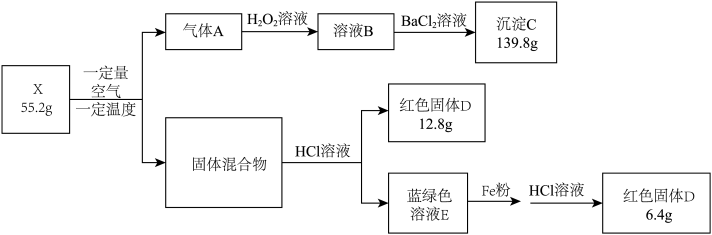
已知:a.X与一定量空气恰好完全反应
b.固体混合物由一种单质和一种磁性物质组成
c.实验过程中的使用的溶液和Fe粉均过量
(1)蓝绿色溶液中含有的金属阳离子是_______ 。
(2)固体混合物与 溶液反应的离子方程式是
溶液反应的离子方程式是_______ 。(只能用一条离子方程式表示)
(3)X的化学式是_______ 。
(4)设计实验,检验上述磁性物质中所含的阳离子:_______ 。

已知:a.X与一定量空气恰好完全反应
b.固体混合物由一种单质和一种磁性物质组成
c.实验过程中的使用的溶液和Fe粉均过量
(1)蓝绿色溶液中含有的金属阳离子是
(2)固体混合物与
 溶液反应的离子方程式是
溶液反应的离子方程式是(3)X的化学式是
(4)设计实验,检验上述磁性物质中所含的阳离子:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的方法为:_______________ (注明试剂、现象)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为__________ (填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边___________________ (填操作名称)、过滤、洗涤。
④高铁酸钠(Na2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与漂白液(主要成分NaClO)在强碱性条件下反应可制取Na 2FeO4,反应的离子方程式为___________________________ 。
(2) ①SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______________ (填代号)。
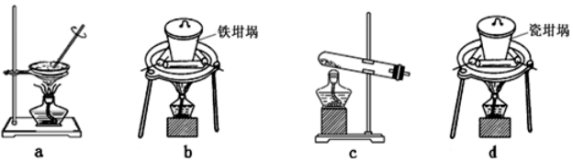
②过量CO2通入到硅酸钠的溶液中,然后加热蒸干,再高温灼烧,最后所得固体成分___________ 。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的方法为:
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边
④高铁酸钠(Na2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与漂白液(主要成分NaClO)在强碱性条件下反应可制取Na 2FeO4,反应的离子方程式为
(2) ①SiO2和NaOH焙烧制备硅酸钠,可采用的装置为

②过量CO2通入到硅酸钠的溶液中,然后加热蒸干,再高温灼烧,最后所得固体成分
您最近半年使用:0次
【推荐2】实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料α-Fe2O3。其主要实验流程如图。

(1)酸浸。用一定浓度的H2SO4溶液浸取铁泥中的铁元素。若其他条件不变,实验中提高铁元素浸出率的措施有___ (写2条)。
(2)还原。向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为Fe2+。“还原”过程中除生成Fe3+外,还会生成___ (填化学式);检验Fe3+是否还原完全的实验操作是___ 。
(3)除杂。向“还原”后的滤液中加入NH4F溶液,使Ca2+转化为CaF2沉淀除去。若溶液的pH偏低、将会导致CaF2沉淀不完全,其原因是___ [Ksp(CaF2)=5.3×10-9,Ka(HF)=6.3×10-4]。
(4)沉铁。将提纯后的FeSO4溶液与氨水-NH4HCO3混合溶液反应,生成FeCO3沉淀。设计以FeSO4溶液、氨水-NH4HCO3混合溶液为原料,制备FeCO3的实验方案:___ 。[FeCO3沉淀需“洗涤完全”,Fe(OH)2开始沉淀的pH=6.5]。

(1)酸浸。用一定浓度的H2SO4溶液浸取铁泥中的铁元素。若其他条件不变,实验中提高铁元素浸出率的措施有
(2)还原。向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为Fe2+。“还原”过程中除生成Fe3+外,还会生成
(3)除杂。向“还原”后的滤液中加入NH4F溶液,使Ca2+转化为CaF2沉淀除去。若溶液的pH偏低、将会导致CaF2沉淀不完全,其原因是
(4)沉铁。将提纯后的FeSO4溶液与氨水-NH4HCO3混合溶液反应,生成FeCO3沉淀。设计以FeSO4溶液、氨水-NH4HCO3混合溶液为原料,制备FeCO3的实验方案:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】探究0.5mol/LFeCl3溶液(pH=1)与不同金属反应时的多样性的原因。
(各组实验中:所用FeCl3溶液体积相同;金属过量;静置、不振荡)
(1)根据实验Ⅰ中的现象,推测红褐色液体为胶体,并用光束照射该液体,在与光束垂直的方向观察到_______ 得以证实。
(2)已知:Fe和Fe3O4均能被磁铁吸引。
①为了确定黑色固体的成分是否含有Fe与Fe3O4,重复实验Ⅰ,及时取少量镁条表面生成的黑色粉末,洗净后进行实验如下:
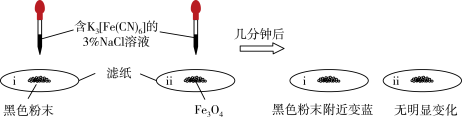
该实验说明黑色固体中一定含有_______ ,结合现象写出判断的理由:_______ 。
②除上述结论外,分析实验Ⅰ的现象,可知被还原得到的产物一定还有_______ 。
(3)实验Ⅰ、Ⅱ中现象的差异,与Fe3+、Mg2+、Fe2+、H+、Cu2+的氧化性强弱有关,其顺序是Mg2+<Fe2+<_______ 。
(各组实验中:所用FeCl3溶液体积相同;金属过量;静置、不振荡)
| 编号 | 金属 | 现象及产物检验 |
| Ⅰ | 镁条 | 立即产生大量气体,金属表面变黑,该黑色固体能被磁铁吸引,液体颜色由棕黄色逐渐变为红褐色; 片刻后气泡减少,金属表面覆盖有红褐色沉淀,此时取反应后的液体,滴加K3[Fe(CN)6]溶液,生成蓝色沉淀。 |
| Ⅱ | 铜粉 | 无气体产生,溶液逐渐变为蓝绿色; 取反应后的溶液,滴加K3[Fe(CN)6]溶液,生成蓝色沉淀。 |
(2)已知:Fe和Fe3O4均能被磁铁吸引。
①为了确定黑色固体的成分是否含有Fe与Fe3O4,重复实验Ⅰ,及时取少量镁条表面生成的黑色粉末,洗净后进行实验如下:

该实验说明黑色固体中一定含有
②除上述结论外,分析实验Ⅰ的现象,可知被还原得到的产物一定还有
(3)实验Ⅰ、Ⅱ中现象的差异,与Fe3+、Mg2+、Fe2+、H+、Cu2+的氧化性强弱有关,其顺序是Mg2+<Fe2+<
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某溶液X中含有H+、Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的几种(除此以外,无其他大量存在的离子),针对该溶液进行实验,内容如下:
①用洁净的玻璃棒蘸取少量X溶液,点在pH试纸上,试纸显红色;
②取适量X溶液,加入过量的Ba(NO3)2溶液,得澄清透明的溶液A,并放出一种无色无味的气体B;
③向溶液A中加入过量的NaOH溶液,微热,放出一种有刺激性气味的气体C,同时生成红褐色沉淀D,过滤得到溶液F;
④向F溶液中通入过量的CO2,有白色沉淀生成。
请回答:
(1)C、D的化学式分别为:C 、D 。
(2)步骤②中反应的离子方程式为: ;
步骤④中反应的离子方程式为: 。
(3)X溶液中一定含有的离子是: ,不能确定是否含有的离子是 ,若要确定该离子(若不止一种,可任选一种)是否存在,可靠的化学方法是 。
①用洁净的玻璃棒蘸取少量X溶液,点在pH试纸上,试纸显红色;
②取适量X溶液,加入过量的Ba(NO3)2溶液,得澄清透明的溶液A,并放出一种无色无味的气体B;
③向溶液A中加入过量的NaOH溶液,微热,放出一种有刺激性气味的气体C,同时生成红褐色沉淀D,过滤得到溶液F;
④向F溶液中通入过量的CO2,有白色沉淀生成。
请回答:
(1)C、D的化学式分别为:C 、D 。
(2)步骤②中反应的离子方程式为: ;
步骤④中反应的离子方程式为: 。
(3)X溶液中一定含有的离子是: ,不能确定是否含有的离子是 ,若要确定该离子(若不止一种,可任选一种)是否存在,可靠的化学方法是 。
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某无色透明溶液中只可能大量存在NH4+、Na+、Ag+、Ba2+、MnO4-、Fe3+、CO32-、SO42-、NO3-中的几种离子。从其中取两份各100mL,进行如下实验:
(1)不做任何实验就可以肯定原溶液中不存在的两种离子是__________ 、_______ 。
(2)取其中的一份进行实验,加入过量氢氧化钠溶液并加热,生成气体0.06mol。另取其中的一份加入过量Ba(NO3)2溶液,生成白色沉淀4.30 g,过滤,向沉淀中再加入过量稀盐酸,沉淀部分消失,余下沉淀2.33 g。综上所述说明原溶液中肯定存在的各离子浓度分别是(下面填写要求:例如c(Na+)=0.1 mol/L)________ 、_________ 、_________ 、_________ (此空可以不填完)。
(3)题干中的MnO4-是化学中的典型强氧化剂,另外生活中常用到的草酸(H2C2O4)是二元弱酸且具有还原性,二者在酸性条件下反应,其中MnO4-被还原成Mn2+,H2C2O4被氧化成CO2,请写出该反应的离子方程式__________ 。
(1)不做任何实验就可以肯定原溶液中不存在的两种离子是
(2)取其中的一份进行实验,加入过量氢氧化钠溶液并加热,生成气体0.06mol。另取其中的一份加入过量Ba(NO3)2溶液,生成白色沉淀4.30 g,过滤,向沉淀中再加入过量稀盐酸,沉淀部分消失,余下沉淀2.33 g。综上所述说明原溶液中肯定存在的各离子浓度分别是(下面填写要求:例如c(Na+)=0.1 mol/L)
(3)题干中的MnO4-是化学中的典型强氧化剂,另外生活中常用到的草酸(H2C2O4)是二元弱酸且具有还原性,二者在酸性条件下反应,其中MnO4-被还原成Mn2+,H2C2O4被氧化成CO2,请写出该反应的离子方程式
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】电解法促进橄榄石(主要成分是Mg2SiO4)固定CO2的部分工艺流程如下:
已知:Mg2SiO4(s) +4HCl(aq) 2MgCl2(aq) +SiO2 (s) + 2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq) +SiO2 (s) + 2H2O(l) △H =-49.04 kJ·mol-1
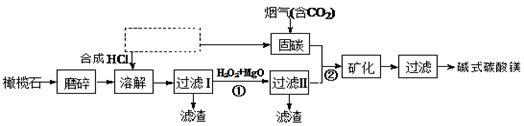
(1)橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为______________ 。
(2)上图虚框内需要补充一步工业生产的名称为________________ 。
(3)下列物质中也可用作“固碳”的是____________ 。(填字母)
a.CaCl2 b.H2NCH2COONa c.(NH4)2CO3
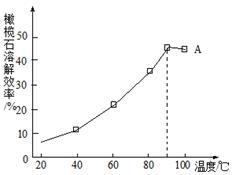
(4)由下图可知,90℃后曲线A溶解效率下降,分析其原因_______________ 。
(5)过滤Ⅰ所得滤液中含有Fe2+,检验该离子方法为________________ 。
(6)过程①为除去滤液中的杂质,写出该除杂过程所涉及反应的离子方程式
______________________ 、______________________ 。
已知:Mg2SiO4(s) +4HCl(aq)
 2MgCl2(aq) +SiO2 (s) + 2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq) +SiO2 (s) + 2H2O(l) △H =-49.04 kJ·mol-1
(1)橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为
(2)上图虚框内需要补充一步工业生产的名称为
(3)下列物质中也可用作“固碳”的是
a.CaCl2 b.H2NCH2COONa c.(NH4)2CO3
(4)由下图可知,90℃后曲线A溶解效率下降,分析其原因

(5)过滤Ⅰ所得滤液中含有Fe2+,检验该离子方法为
(6)过程①为除去滤液中的杂质,写出该除杂过程所涉及反应的离子方程式
您最近半年使用:0次



