A~R 9种元素在元素周期表中的位置如图。
回答下列问题:
(1)E的原子结构示意图为_______ 。
(2)常温下, 的状态为
的状态为_______ (填“液”、“固”或“气”)态。
(3)写出单质A与 在加热条件下发生反应的化学方程式:
在加热条件下发生反应的化学方程式:_______ 。
(4)化合物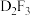 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为_______ 。
(5)H元素形成的单质的用途有_______ (填一种即可)。
(6)最高价氧化物对应水化物的碱性:C_______ (填“>”、“<”或“=”)A,判断的理由为_______ 。
(7)化合物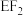 所含分子中的电子总数为
所含分子中的电子总数为_______ ,与其具有相同电子数的化合物分子为_______ (填标号)。
a. b.
b. c.
c. d.
d.
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | A | E | F | |||||
| 3 | C | D | G | H | ||||
| 4 | B | R | ||||||
(1)E的原子结构示意图为
(2)常温下,
 的状态为
的状态为(3)写出单质A与
 在加热条件下发生反应的化学方程式:
在加热条件下发生反应的化学方程式:(4)化合物
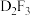 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为(5)H元素形成的单质的用途有
(6)最高价氧化物对应水化物的碱性:C
(7)化合物
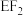 所含分子中的电子总数为
所含分子中的电子总数为a.
 b.
b. c.
c. d.
d.
更新时间:2023-02-08 18:02:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩种元素,
按要求填写下列空白:
(1)在这些元素中,化学性质最不活泼的元素是:_______ (填元素符号),其原子结构示意图为_______________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是______ ,碱性最强的化合物的电子式是________________ 。
(3)最高价氧化物属两性氧化物的元素是______ (填元素符号);写出它的最高价氧化物与氢氧化钠溶液反应的化学方程式:__________________________ 。
(4)用电子式表示元素④与⑦形成的化合物的形成过程:_______________ 。
该化合物属于_________ (填 “共价”或“离子”)化合物。
(5)比较:氢化物稳定性②_____ ③,最高价氧化物对应水化物的酸性②____ ⑥
(填“>”、“<”或“=”)。
(6)⑥的最高价氧化物与烧碱溶液反应的离子方程式为__________________ ;
(7)工业上制取元素⑥的单质的化学方程式为_______________________ 。
按要求填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(1)在这些元素中,化学性质最不活泼的元素是:
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)最高价氧化物属两性氧化物的元素是
(4)用电子式表示元素④与⑦形成的化合物的形成过程:
该化合物属于
(5)比较:氢化物稳定性②
(填“>”、“<”或“=”)。
(6)⑥的最高价氧化物与烧碱溶液反应的离子方程式为
(7)工业上制取元素⑥的单质的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是周期表中的一部分,根据①—⑧在周期表中的位置,用元素符号或化学式回答问题
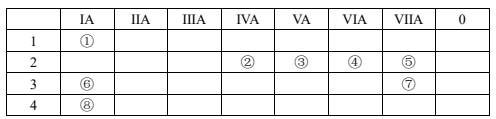
(1)画出表中元素中,非金属性最强的元素的离子结构示意图_______ ;
(2)这些元素的最高价氧化物对应水化物中酸性最强的是______ ,碱性最强的是______ ;
(3)用电子式表示表中④和⑥两元素以1:2微粒个数比形成化合物的过程_______ ;
(4)表中⑤⑦两种元素氢化物的稳定性更强的是_______ ;
(5)⑥和⑧两种元素形成的氯化物的熔点较高的是_______ ,简述判断理由_______ ;
(6)用一个化学方程式证明②③两种元素非金属性的强弱_______ 。

(1)画出表中元素中,非金属性最强的元素的离子结构示意图
(2)这些元素的最高价氧化物对应水化物中酸性最强的是
(3)用电子式表示表中④和⑥两元素以1:2微粒个数比形成化合物的过程
(4)表中⑤⑦两种元素氢化物的稳定性更强的是
(5)⑥和⑧两种元素形成的氯化物的熔点较高的是
(6)用一个化学方程式证明②③两种元素非金属性的强弱
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期律的重要性。如表列出了元期表中短周期的一部分,a~i代表9种短周期元素。
已知c与氢元素能组成生活中最常见的化合物X。回答下列问题:
(1)元素h在周期表中位于第_______ 族,g的原子结构示意图为_______ 。
(2)由元素d与e组成的化合物的电子式为_______ 。
(3)a~i中,非金属性最强的是_______ (填元素符号);f、g、h、i四种元素的最高价氧化物对应的水化物中,酸性最强的化合物的化学式为_______ 。
(4)因在元素a的电池材料领域做出了杰出贡献,97岁的古迪纳夫荣获2019年诺贝尔化学奖,a的单质与氧气共热时的化学方程式为_______ 。
(5)一定条件下,铁能与气态X发生反应,该反应的化学方程式为_______ 。
(6)设计实验比较元素i的单质和I2的氧化性,操作与现象是:取2mLKI溶液于试管中,_______ 。
| a | b | c | d | |||
| e | f | g | h | i |
(1)元素h在周期表中位于第
(2)由元素d与e组成的化合物的电子式为
(3)a~i中,非金属性最强的是
(4)因在元素a的电池材料领域做出了杰出贡献,97岁的古迪纳夫荣获2019年诺贝尔化学奖,a的单质与氧气共热时的化学方程式为
(5)一定条件下,铁能与气态X发生反应,该反应的化学方程式为
(6)设计实验比较元素i的单质和I2的氧化性,操作与现象是:取2mLKI溶液于试管中,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表前20号元素的有关信息:
已知:Li的半径为0.152nm,Be的半径为0.111nm。回答下列问题:
(1)元素c在周期表中的位置为________ ,用电子式表示a2e的形成过程:________ 。
(2)f、h、b简单离子半径由大到小的顺序为________ (用离子符号表示)。
(3)BaCl2溶液中先通入eb2,再加入h的单质,可观察到的现象是________ ,发生反应的离子方程式为________ 。
(4)化合物A、B均由a、b、e、f四种元素组成,则A和B相互反应的离子方程式:________ 。
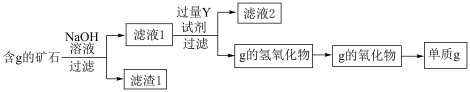
(5)工业上用含g元素的矿石(主要成分为g的氧化物,还含有杂质FeO、Fe2O3)提纯g的氧化物并冶炼单质g,流程如下,滤渣1的成分为:________ (填写化学式),滤液1中通入过量Y试剂反应的离子方程式为:________ 。
| 元素 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.030 | 0.066 | 0.117 | 0.232 | 0.106 | 0.186 | 0.143 | 0.099 |
| 最高正化合价 | +1 | +4 | +1 | +6 | +1 | +3 | +7 | |
| 最低负化合价 | -2 | -4 | -2 | -1 |
(1)元素c在周期表中的位置为
(2)f、h、b简单离子半径由大到小的顺序为
(3)BaCl2溶液中先通入eb2,再加入h的单质,可观察到的现象是
(4)化合物A、B均由a、b、e、f四种元素组成,则A和B相互反应的离子方程式:
(5)工业上用含g元素的矿石(主要成分为g的氧化物,还含有杂质FeO、Fe2O3)提纯g的氧化物并冶炼单质g,流程如下,滤渣1的成分为:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,元素①-⑦是短周期的主族元素,请参照元素①-⑥在表中的位置,回答下列问题:
(1)写出⑥在元素周期表中的位置_____ 。
(2)②的气态氢化物的沸点____ ⑥的气态氢化物的沸点。(填大于、小于或等于)
(3)④的最高价氧化物与③的最高价氧化物对应的水化物的水溶液反应的离子方程式为
_____ 。
(4)①和⑤形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是_____ , 与该化合物晶体类型相同的是______ (请用相应的编号填写)。
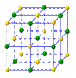
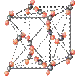

A B C
(5)由①和③形成的化合物甲和乙,甲受到撞击会分解生成一种固体单质和一种气体单质,此反应中反应物、固体单质和气体单质的物质的量之比是2:2:3;乙中加入过量的盐酸后生成两种盐,在其中一种盐中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体。则化合物甲的化学式为_____ ,化合物乙与过量盐酸反应的化学方程式为_____ 。
| ① | ② | |||||
| ③ | ④ | ⑤ | ⑥ | ⑦ |
(1)写出⑥在元素周期表中的位置
(2)②的气态氢化物的沸点
(3)④的最高价氧化物与③的最高价氧化物对应的水化物的水溶液反应的离子方程式为
(4)①和⑤形成的化合物是化工行业已合成的一种硬度很大、熔点很高的晶体,若已知在此化合物中各元素均处于其最高或最低价态,据此推断:该化合物的化学式可能是



A B C
(5)由①和③形成的化合物甲和乙,甲受到撞击会分解生成一种固体单质和一种气体单质,此反应中反应物、固体单质和气体单质的物质的量之比是2:2:3;乙中加入过量的盐酸后生成两种盐,在其中一种盐中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体。则化合物甲的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分。表中所列字母分别代表一种元素。
回答下列问题:
(1)j在元素周期表中的位置是______ 。
(2)e、h、m形成的简单离子其半径由大到小的顺序为________ 。(填写离子符号)
(3)n与g形成的化合物为______ (填写化学式,下同),将该化合物进行焰色反应,火焰呈______ 色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为______ 。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____ Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释______ 。
| a | b | |||||||
| c | d | e | f | |||||
| g | h | i | j | k | l | m | ||
| n |
(1)j在元素周期表中的位置是
(2)e、h、m形成的简单离子其半径由大到小的顺序为
(3)n与g形成的化合物为
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次



