下表是元素周期表的一部分。表中所列字母分别代表一种元素。
回答下列问题:
(1)j在元素周期表中的位置是______ 。
(2)e、h、m形成的简单离子其半径由大到小的顺序为________ 。(填写离子符号)
(3)n与g形成的化合物为______ (填写化学式,下同),将该化合物进行焰色反应,火焰呈______ 色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为______ 。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____ Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释______ 。
| a | b | |||||||
| c | d | e | f | |||||
| g | h | i | j | k | l | m | ||
| n |
(1)j在元素周期表中的位置是
(2)e、h、m形成的简单离子其半径由大到小的顺序为
(3)n与g形成的化合物为
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释
21-22高一上·湖南怀化·期末 查看更多[4]
湖南省怀化市2021-2022学年高一上学期期末考试化学试题(已下线)第四章 物质结构 元素周期律(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题(已下线)【2023】【高一下】【其他】【杭高卷四-期中复习卷】【高中化学】【刘尼尼收集】
更新时间:2022-01-14 09:52:12
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.生活中化学无处不在,家庭厨卫用品中有许多中学化学常见的物质。下表为部分厨卫用品名称及其主要成分表。回答下列问题:
(1)若不慎将食盐洒在天然气灶的火焰上,观察到的现象是_______ 。
(2)除去碳酸钠固体中含有少量碳酸氢钠的方法是_______ ,发生反应的化学方程式为_______ 。
(3)碳酸氢钠可以作为治疗胃酸(主要成分为盐酸)过多的药物的主要成分,其反应原理的离子方程式为_______ 。
(4)“84”消毒液不能与洁厕灵混合使用,否则可能会产生有毒气体单质,该气体单质是_______ (填名称)。
Ⅱ.亚硝酸钠( )是肉制品生产中最常使用的一种食品添加剂。
)是肉制品生产中最常使用的一种食品添加剂。
(5)某兴趣小组研究亚硝酸钠时,查阅资料得到以下信息:
ⅰ.亚硝酸钠的水溶液呈碱性;
ⅱ.亚硝酸钠是一种强氧化剂,进入血液后与血红蛋白结合,导致组织缺氧,使人体出现青紫并中毒;
ⅱ.亚硝酸钠的外观与食盐极为相似,容易被误用而引起中毒。
回答下列问题:
①已知 能与HI发生如下化学反应:
能与HI发生如下化学反应: ,该反应的还原剂是
,该反应的还原剂是_______ (填化学式),请用双线桥表示该反应电子转移的方向和数目_______ 。
②下列方法中可用来区分 和
和 的是
的是_______ (填标号)。
A.观察外形
B.在酸性条件下加入淀粉碘化钾溶液观察溶液变化
C.向两物质的水溶液中滴加酚酞溶液观察溶液颜色变化
| 名称 | 食盐 | 碱面 | 发酵粉 | 洁厕灵 | “84”消毒液 |
| 主要成分 |  |  |  |  |  |
(2)除去碳酸钠固体中含有少量碳酸氢钠的方法是
(3)碳酸氢钠可以作为治疗胃酸(主要成分为盐酸)过多的药物的主要成分,其反应原理的离子方程式为
(4)“84”消毒液不能与洁厕灵混合使用,否则可能会产生有毒气体单质,该气体单质是
Ⅱ.亚硝酸钠(
 )是肉制品生产中最常使用的一种食品添加剂。
)是肉制品生产中最常使用的一种食品添加剂。(5)某兴趣小组研究亚硝酸钠时,查阅资料得到以下信息:
ⅰ.亚硝酸钠的水溶液呈碱性;
ⅱ.亚硝酸钠是一种强氧化剂,进入血液后与血红蛋白结合,导致组织缺氧,使人体出现青紫并中毒;
ⅱ.亚硝酸钠的外观与食盐极为相似,容易被误用而引起中毒。
回答下列问题:
①已知
 能与HI发生如下化学反应:
能与HI发生如下化学反应: ,该反应的还原剂是
,该反应的还原剂是②下列方法中可用来区分
 和
和 的是
的是A.观察外形
B.在酸性条件下加入淀粉碘化钾溶液观察溶液变化
C.向两物质的水溶液中滴加酚酞溶液观察溶液颜色变化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组在课外活动中,对某溶液进行了多次检验,其中三次检验结果如下表所示,请回答下列问题。
(1)三次检验结果中第___________ 次检验结果不正确。
(2)检验时,为了确定溶液中是否存在 、
、 、
、 进行下列实验:
进行下列实验:
第一,向溶液中滴加___________ (填化学式)溶液,其目的是___________ ;
第二,继续加入过量的___________ (填化学式)溶液,其目的是___________ ;
第三:向溶液中滴加___________ (填化学式)溶液,其目的是___________ ;
第四:过滤,再向滤液中加入___________ (填化学式)溶液,其目的是___________ 。
(3)为了确定 的存在,写出
的存在,写出 鉴定的实验方法和现象:
鉴定的实验方法和现象:___________ 。
| 检验次数 | 溶液中检验出的物质 |
| 第一次 |  、 、 、 、 、 、 |
| 第二次 |  、 、 、 、 、 、 |
| 第三次 |  、 、 、 、 、 、 |
(2)检验时,为了确定溶液中是否存在
 、
、 、
、 进行下列实验:
进行下列实验:第一,向溶液中滴加
第二,继续加入过量的
第三:向溶液中滴加
第四:过滤,再向滤液中加入
(3)为了确定
 的存在,写出
的存在,写出 鉴定的实验方法和现象:
鉴定的实验方法和现象:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出C、D、的化学式:C_______ ,D______ 。
(2)将含1 mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,请写出A与E反应的离子方程式:_______________ 。
(3)在A溶液中加入少量澄清石灰水,其离子方程式为_____________________ 。
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理______________________ 。
(5)若向含溶质0.5 mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为__________ g。
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 |    OH- OH- |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出C、D、的化学式:C
(2)将含1 mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,请写出A与E反应的离子方程式:
(3)在A溶液中加入少量澄清石灰水,其离子方程式为
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理
(5)若向含溶质0.5 mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分。
(1)表中元素_______ 的非金属性最强;元素_______ 的金属性最强; (写元素符号)。
(2)表中半径最大的元素是_______ ;(写元素符号)
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是_______ ;(写化学式,下同)
(4)表中元素⑥、⑦氢化物的稳定性顺序为_______ ;
(5)表中元素最高价氧化物对应水化物酸性最强的酸是_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ⑤ | |||||
| 三 | ③ | ⑥ | |||||
| 四 | ④ | ⑦ | |||||
(1)表中元素
(2)表中半径最大的元素是
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是
(4)表中元素⑥、⑦氢化物的稳定性顺序为
(5)表中元素最高价氧化物对应水化物酸性最强的酸是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】六种短周期元素a、b、c、d、e、f其原子序数与其最高正价或最低负价的关系如下图所示。

(1)上述六种元素,其中属于金属元素的有________ 种。
(2)元素f在周期表中的位置是____________ 。
(3)由a、b、c三种元素组成既含离子键又含共价键的化合物,该化合物的化学式为________ ,该化合物的水溶液显_________ 性,该化合物在水中的电离方程式为____________ 。
(4)b元素的气态氢化物与f元素的气态氢化物熔沸点高低顺序为_________ (用氢化物的化学式表示)。
(5)a与b、c两元素分别可形成18电子的分子M和N,其中M的电子式为_______ 。化合物M是一种环保的液体燃料,常温下8g液态M与足量的液态N反应可放出204.5kJ的热量,则该反应的热化学反应方程式为___________________________ 。

(1)上述六种元素,其中属于金属元素的有
(2)元素f在周期表中的位置是
(3)由a、b、c三种元素组成既含离子键又含共价键的化合物,该化合物的化学式为
(4)b元素的气态氢化物与f元素的气态氢化物熔沸点高低顺序为
(5)a与b、c两元素分别可形成18电子的分子M和N,其中M的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮可以形成多种离子,如N3-、NH2-、N3-、NH4+、N2H5+等。已知N2H5+离子的形成过程类似NH4+的形成过程,N2H5+在碱性溶液中生成电中性的分子和水,试填写下列空白。
(1)该电中性分子的化学式为________________________ 。
(2)N2H5+离子的电子式为______________________ 。
(3)写出两种由多原子组成的含有与N3-电子数相同的分子的化学式_______ 、________ 。
(1)该电中性分子的化学式为
(2)N2H5+离子的电子式为
(3)写出两种由多原子组成的含有与N3-电子数相同的分子的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如图是元素周期表的一部分,其中每个数字序号代表一种 短周期元素。根据表中所列①~⑩元素,请按要求回答下列问题:

(1)元素⑤形成的氧化物的电子式为_______ ;①、⑦两种元素的最高价氧化物的熔点较高的是________ (填化学式)。
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是_______ (填化学式)。
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有______ 。
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为_________ 。
(5)下列事实能说明③非金属性比⑧强的有___________ (填字母)。
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高

(1)元素⑤形成的氧化物的电子式为
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为
(5)下列事实能说明③非金属性比⑧强的有
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如表列出了①~⑦七种元素在周期表中的位置:
请按要求回答下列问题:
(1)元素③的原子结构示意图是___________ ,以上元素的最高价氧化物形成的水化物酸性最强的是___________ (填分子式)。
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序排列为___________ (用离子符号表示);②、③两种元素的最高价氧化物对应的水化物碱性由弱到强的顺序是___________ (用化学式表示)。
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为___________ 。
(4)②和⑦按原子个数比1∶1形成离子化合物的电子式___________ 。
(5)设计一个实验比较②与③的金属性强弱___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 二 | ① | ⑦ | ||||||
| 三 | ② | ③ | ④ | ⑤ | ⑥ |
请按要求回答下列问题:
(1)元素③的原子结构示意图是
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序排列为
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为
(4)②和⑦按原子个数比1∶1形成离子化合物的电子式
(5)设计一个实验比较②与③的金属性强弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。

(1)元素Ga在元素周期表中的位置为:___ (写明周期和族)。
(2)Sn的最高正价为______ ,Cl的最高价氧化物对应水化物的化学式为______ ,As的气态氢化物为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______ (填化学式)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4______ H2SeO4(填“>”、“<”或“=”)。
③氢化物的还原性:H2O__ H2S(填“>”、“<”或“=”)。
(4)可在图中分界线(虚线部分)附近寻找________ (填序号)。
A. 优良的催化剂 B. 半导体材料 C. 合金材料 D. 农药
(5)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
(4)可在图中分界线(虚线部分)附近寻找
A. 优良的催化剂 B. 半导体材料 C. 合金材料 D. 农药
(5)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
| 实验步骤 | 实验现象与结论 |
| 在试管中加入 | 现象: |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有表格中短周期元素的数据(已知Be的原子半径为0.089nm):
(1)⑧号元素在元素周期表中的位置是。_______ 。
(2)①④⑦元素的简单气态氢化物中,热稳性定由高到低排序_______ (写化学式)。
(3)结合原子结构解释③⑥元素的最高价氧化物对应的水化物的碱性强弱_______ 。
(4)含锂材料在社会中应用广泛,如各种储氢材料Li2NH等)、便携式电源材料(LiCoO2等),根据下列要求回答问题:
①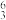 Li和
Li和 Li可作核反应堆最佳热载体,
Li可作核反应堆最佳热载体, LiH和
LiH和 LiD用作高温堆减速剂。下列说法正确的是
LiD用作高温堆减速剂。下列说法正确的是_______ (填字母,下同)。
A.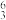 Li和
Li和 Li互为同位素 B.
Li互为同位素 B.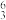 Li和
Li和 Li属于同种核素
Li属于同种核素
C. LiH和
LiH和 LiD中质子总数相同 D.
LiD中质子总数相同 D. LiH和
LiH和 LiD中电子总数相同
LiD中电子总数相同
②实验室中钠为避免接触空气保存在_______ 中;锂电池使用时需要注意防水,其原因用离子反应方程式表示为_______ 。
③下列说法不正确的是_______ 。
A.碱性:Be(OH)2<LiOH<NaOH<KOH
B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+
D.金属性:Cs>Rb>K>Na>Li>Be
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
| 最高正价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低负价 | -2 | -3 | -1 | -3 |
(2)①④⑦元素的简单气态氢化物中,热稳性定由高到低排序
(3)结合原子结构解释③⑥元素的最高价氧化物对应的水化物的碱性强弱
(4)含锂材料在社会中应用广泛,如各种储氢材料Li2NH等)、便携式电源材料(LiCoO2等),根据下列要求回答问题:
①
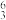 Li和
Li和 Li可作核反应堆最佳热载体,
Li可作核反应堆最佳热载体, LiH和
LiH和 LiD用作高温堆减速剂。下列说法正确的是
LiD用作高温堆减速剂。下列说法正确的是A.
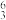 Li和
Li和 Li互为同位素 B.
Li互为同位素 B.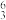 Li和
Li和 Li属于同种核素
Li属于同种核素C.
 LiH和
LiH和 LiD中质子总数相同 D.
LiD中质子总数相同 D. LiH和
LiH和 LiD中电子总数相同
LiD中电子总数相同②实验室中钠为避免接触空气保存在
③下列说法不正确的是
A.碱性:Be(OH)2<LiOH<NaOH<KOH
B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+
D.金属性:Cs>Rb>K>Na>Li>Be
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。
Ⅰ.如图是元素周期表的一部分,回答下列问题:
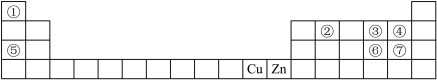
(1)①~⑦号元素中原子半径最大的是___________ (填元素符号),其最高价氧化物对应的水化物中含有的化学键是___________ 。该元素的单质与氧气在加热条件下反应生成R,用电子式表示R的形成过程___________ 。
(2)①~⑦号元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同),碱性最强的是___________ 。
(3)将锌片、铜片用导线连接后浸入⑥的最高价氧化物对应水化物的稀溶液中,构成了原电池,则负极的电极反应式是___________ 。一段时间后,若锌片的质量减少了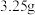 ,则导线中通过电子
,则导线中通过电子___________  。
。
Ⅱ.某小组为探究 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
(4)实验①可得出氧化性强弱:___________ 。
(5)实验②观察到的现象是___________ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,他补做了实验③。
,他补做了实验③。
补做实验③的目的是___________ 。
Ⅰ.如图是元素周期表的一部分,回答下列问题:

(1)①~⑦号元素中原子半径最大的是
(2)①~⑦号元素的最高价氧化物对应的水化物中,酸性最强的是
(3)将锌片、铜片用导线连接后浸入⑥的最高价氧化物对应水化物的稀溶液中,构成了原电池,则负极的电极反应式是
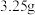 ,则导线中通过电子
,则导线中通过电子 。
。Ⅱ.某小组为探究
 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 | 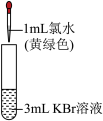 | 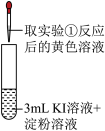 |
| 现象 | 溶液变为黄色 |
(5)实验②观察到的现象是
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,他补做了实验③。
,他补做了实验③。| 实验③ | 另取实验①反应后的黄色溶液少许,先加入足量的 固体,充分振荡,然后加入 固体,充分振荡,然后加入 溶液和淀粉溶液。 溶液和淀粉溶液。 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期律反映了元素性质的周期性变化规律。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是_______ (填化学式)。
(2)在元素周期表中, ,
, 具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:
具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:_______ 。
(3)氮氧化铝(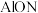 )是一种高硬度,耐高温的防弹材料,
)是一种高硬度,耐高温的防弹材料, 、O、N三种元素的简单离子半径由大到小的排列顺序是
、O、N三种元素的简单离子半径由大到小的排列顺序是_______ 。
(4)锡为主族元素,其原子结构示意图: 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是_______ , 能与
能与 溶液反应生成钠盐,写出发生反应的化学方程式:
溶液反应生成钠盐,写出发生反应的化学方程式:_______ 。
(5)硒 是与人类的健康密切相关的一种元素,工业上用浓
是与人类的健康密切相关的一种元素,工业上用浓 ,焙烧
,焙烧 的方法提取硒(其中
的方法提取硒(其中 转化为
转化为 ),且有
),且有 和
和 (固体)生成,写出发生反应的化学方程式:
(固体)生成,写出发生反应的化学方程式:_______ 。理论上该反应每转移 电子,可得到的
电子,可得到的 的质量为
的质量为_______ g。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是
(2)在元素周期表中,
 ,
, 具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:
具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:(3)氮氧化铝(
 )是一种高硬度,耐高温的防弹材料,
)是一种高硬度,耐高温的防弹材料, 、O、N三种元素的简单离子半径由大到小的排列顺序是
、O、N三种元素的简单离子半径由大到小的排列顺序是(4)锡为主族元素,其原子结构示意图:
 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是 能与
能与 溶液反应生成钠盐,写出发生反应的化学方程式:
溶液反应生成钠盐,写出发生反应的化学方程式:(5)硒
 是与人类的健康密切相关的一种元素,工业上用浓
是与人类的健康密切相关的一种元素,工业上用浓 ,焙烧
,焙烧 的方法提取硒(其中
的方法提取硒(其中 转化为
转化为 ),且有
),且有 和
和 (固体)生成,写出发生反应的化学方程式:
(固体)生成,写出发生反应的化学方程式: 电子,可得到的
电子,可得到的 的质量为
的质量为
您最近一年使用:0次



