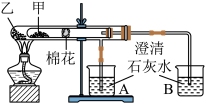
为探究铁片与浓硝酸的反应原理,某同学设计如下4组实验,所有实验过程中均有红棕色气体产生,且③产生的红棕色气体明显比②多,④不考虑空气对反应的影响。
下列说法正确的是
 | 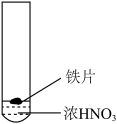 |  |  |
| ① | ② | ③ | ④ |
| A.①中产生的气体一定是混合物 |
| B.②和③中发生的反应完全相同 |
C.③能说明铁片与浓硝酸发生反应生成 |
D.由④可说明浓硝酸具有挥发性,且 为还原产物 为还原产物 |
更新时间:2023-02-10 09:12:23
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
 |  |  |
| ① | ② | ③ |
| A.由①中的红棕色气体,推断产生的气体一定是混合气体 |
| B.由②中的红棕色气体不能表明木炭与浓硝酸发生了反应 |
| C.由③说明浓硝酸具有挥发性,生成的红棕色气体为氧化产物 |
D.③的气体产物中检测出 ,由此说明木炭一定与浓硝酸发生了反应 ,由此说明木炭一定与浓硝酸发生了反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】下列方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 探究NO2能否支持燃烧 | 取少量浓硝酸加热分解,将产物先通入浓硫酸,后用集气瓶收集气体 | 将带火星的木条放置瓶内,木条复燃,说明NO2支持燃烧 |
| B | 探究乙醇与浓硫酸反应是否生成了乙烯 | 将乙醇与浓硫酸混合加热,产生的气体通入酸性KMnO4溶液,观察颜色变化 | 溶液紫红色褪去,说明产生的气体中一定含有乙烯 |
| C | 苯和液溴反应是否生成了HBr | 将少量铁粉、5mL苯和1mL液溴混合,产生的气体通入AgNO3溶液中 | 混合时液体剧烈沸腾,AgNO3溶液中产生淡黄色沉淀,苯和液溴发生反应生了HBr |
| D | 探究维生素C的还原性 | 向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 | 黄色溶液变为浅绿色,说明生素C具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】某学习小组为研究铜与浓、稀HNO3反应的差异,设计了如图所示的实验装置。

下列说法不正确的是

下列说法不正确的是
| A.反应开始前通入过量的CO2气体,目的是排除装置内的空气 |
B.A中的离子方程式为Cu+2NO +4H+=Cu2++2NO2↑+2H2O +4H+=Cu2++2NO2↑+2H2O |
| C.当B中0.03 mol铜粉被氧化时,B中产生的NO气体小于0.02 mol |
| D.C装置中装入一定量的水进行尾气处理 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】下列由相关实验现象所推出的结论错误的是
| A.NH4Cl和NH4HCO3受热都能分解,说明可以用加热NH4Cl或NH4HCO3固体的方法制氨气 |
B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,不能说明该溶液一定有 |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别将充满HCl、NH3的烧瓶倒置于水中,液面均迅速上升,说明二者均易溶于水 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】Cl2O 是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会发生燃烧并爆炸。一种制取Cl2O 的装置如图所示。
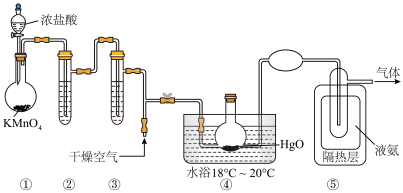
已知:Cl2O 的熔点为-116℃,沸点为 3.8℃;Cl2的沸点为-34.6℃;氨气的沸点:-33℃;HgO+2Cl2===HgCl2+Cl2O。
下列说法中不正确的是

已知:Cl2O 的熔点为-116℃,沸点为 3.8℃;Cl2的沸点为-34.6℃;氨气的沸点:-33℃;HgO+2Cl2===HgCl2+Cl2O。
下列说法中不正确的是
| A.Cl2O 与水的反应为氧化还原反应 |
| B.通入干燥空气的目的是将生成的Cl2O 稀释,减小爆炸危险 |
| C.从装置⑤中逸出气体的主要成分是 Cl2O |
| D.装置④与⑤之间不用橡胶管连接,是为了防止橡胶管燃烧和爆炸 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】铬与氮能形成多种化合物,其中氮化铬( )是一种良好的耐磨材料。实验室可用无水氯化铬(
)是一种良好的耐磨材料。实验室可用无水氯化铬( )与氨气在高温下反应制备,反应原理为:
)与氨气在高温下反应制备,反应原理为: 。
。
下列说法正确的是
 )是一种良好的耐磨材料。实验室可用无水氯化铬(
)是一种良好的耐磨材料。实验室可用无水氯化铬( )与氨气在高温下反应制备,反应原理为:
)与氨气在高温下反应制备,反应原理为: 。
。
下列说法正确的是
A.无水氯化铬可以通过直接加热氯化铬晶体( )脱水得到 )脱水得到 |
| B.反应开始时应先将硬质玻璃管预热,再打开分液漏斗活塞 |
| C.硬质玻璃管右端的导气管过细,易产生堵塞 |
D.将12.8g产品在空气中充分加热,得15.2g固体残渣( ),产品中可能含有 ),产品中可能含有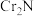 |
您最近一年使用:0次

 =2Br-+2H++SO
=2Br-+2H++SO