请列举铁与硝酸反应的各种情况,写出相关的离子方程式_______ 。
更新时间:2023/03/07 22:01:21
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)把下列式子改成氧化物形式
①正长石(KAlSi3O8)__________________ ;
②蛇纹石(H4Mg3Si2O9)___________________ ;
(2)写出下列物质间的关系:红磷与白磷_________________ ;
35Cl和37Cl____________________ ;
(3)写出除去括号中杂质的方法:
碳酸钠固体(碳酸氢钠晶体)__________________ ;
SiO2固体(CaO)___________________ ;
CO2(SO2)_________________________ ;
(4)写出稀硝酸与金属银在加热条件下反应的离子方程式:__________________ ;
将PbO2放入浓盐酸中会产生Cl2,此反应的化学方程式为:_________________ ;
(5)标准状况下,在三个容积相同的干燥的烧瓶中,甲瓶装入干燥纯净的NH3,乙瓶装入含四分之一体积空气的HCl,丙瓶装入NO2和O2(体积比为4:1),以水为溶剂作喷泉实验。实验结束后三个烧瓶中溶液的物质的量浓度之比为______________ ,丙瓶中发生反应的总化学方程式为______________________ 。
①正长石(KAlSi3O8)
②蛇纹石(H4Mg3Si2O9)
(2)写出下列物质间的关系:红磷与白磷
35Cl和37Cl
(3)写出除去括号中杂质的方法:
碳酸钠固体(碳酸氢钠晶体)
SiO2固体(CaO)
CO2(SO2)
(4)写出稀硝酸与金属银在加热条件下反应的离子方程式:
将PbO2放入浓盐酸中会产生Cl2,此反应的化学方程式为:
(5)标准状况下,在三个容积相同的干燥的烧瓶中,甲瓶装入干燥纯净的NH3,乙瓶装入含四分之一体积空气的HCl,丙瓶装入NO2和O2(体积比为4:1),以水为溶剂作喷泉实验。实验结束后三个烧瓶中溶液的物质的量浓度之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。请回答下列问题:
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有____________ 性。用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有______________ 性。
用玻璃棒蘸取浓硝酸滴在pH试纸上,试纸逐渐变白,这种漂白现象说明浓硝酸具有_______ 性。
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是__________ (填序号)。
①Cu + HNO3(浓)→ Cu(NO3)2
②Cu + HNO3(稀)→ Cu(NO3)2
③Cu CuO
CuO Cu(NO3)2
Cu(NO3)2
(3)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式_____________ 。
(4)若将12.8g铜跟一定质量的浓HNO3反应,铜消耗完时,共产生气体5.6L(标准状况) (不考虑N2O4),则所耗HNO3的物质的量____________ mol.
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为____________________________________________ 。
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有
用玻璃棒蘸取浓硝酸滴在pH试纸上,试纸逐渐变白,这种漂白现象说明浓硝酸具有
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是
①Cu + HNO3(浓)→ Cu(NO3)2
②Cu + HNO3(稀)→ Cu(NO3)2
③Cu
 CuO
CuO Cu(NO3)2
Cu(NO3)2(3)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(4)若将12.8g铜跟一定质量的浓HNO3反应,铜消耗完时,共产生气体5.6L(标准状况) (不考虑N2O4),则所耗HNO3的物质的量
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)配平下列化学方程式(将系数填在横线上),并写出还原剂。
___ NH3+___ O2= ___ N2+ ___ H2O,该反应中的还原剂是_______ 。
⑵铁和稀硝酸反应,若反应后铁无剩余,则生成的盐可能是__________ 或____________ 或_________ ;若反应后硝酸有剩余,则生成的盐是___________ ;该反应的化学方程式为:_______________ 。
⑵铁和稀硝酸反应,若反应后铁无剩余,则生成的盐可能是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,则该反应的离子方程式是______________ 。
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是______________ 。
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中①A元素在周期表中的位置是第______________ 周期______________ 族,气体Y的化学式是______________ 。
②含amolX的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X的物质的量为______________ mol。
(4)若A、B、X、Y均为化合物。A溶于水电离出的金属阳离子水解的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4恰好反应,所得溶液为无色时,该该反应的离子方程式是______________ 。
Ⅱ.用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
③H2O(g)=H2O(l)ΔH=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式______________ 。
(1)若Y是黄绿色气体,则该反应的离子方程式是
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中①A元素在周期表中的位置是第
②含amolX的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X的物质的量为
(4)若A、B、X、Y均为化合物。A溶于水电离出的金属阳离子水解的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4恰好反应,所得溶液为无色时,该该反应的离子方程式是
Ⅱ.用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
③H2O(g)=H2O(l)ΔH=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:_______________ 。
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3·xH2O),反应的化学方程式为_________________ 。
(3)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被完全除尽后,溶液中继续发生的化合反应的化学方程式为____________________________ 。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3·xH2O),反应的化学方程式为
(3)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被完全除尽后,溶液中继续发生的化合反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】金属腐蚀原理的应用
(1)将铝片浸入浓硫酸或浓硝酸时,铝片表面产生___________ ,从而阻止铝进一步被氧化。可以用___________ 运输冷的浓硝酸或浓硫酸。
(2)铁在___________ 的混合液中发蓝、发黑,使铁表面形成一层___________ ,可防止铁被腐蚀。
(3)生活中常用的“暖宝宝”是利用___________ 原理制造的。
(1)将铝片浸入浓硫酸或浓硝酸时,铝片表面产生
(2)铁在
(3)生活中常用的“暖宝宝”是利用
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】2021年是国际化学年十周年纪念,中国的宣传口号是“化学一我们的生活,我们的未来”。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
(2)工业上常用金属钠冶炼钛,是利用金属钠的强_______ 性。
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为_______ 。
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯_______ (填“I”或“II”)中澄清石灰水变浑浊。加热后试管中发生反应的化学方程式为_______ 。

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式_______ 。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
| A.晶体硅用于制作半导体材料 | B.硅在常温下化学性比较活泼 |
| C.玻璃属于硅酸盐材料 | D.玛瑙的主要成分是硅单质 |
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
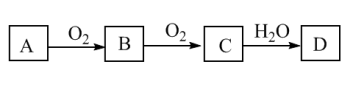
【推荐3】Ⅰ.图象具有直观、线索清晰、引导性强等特点,有利于提高统筹思维和概括能力。图是氮元素的化合价与部分常见含氮物质的关系。

请回答下列问题:
(1)丙的化学式为_______
(2)写出实验室制备甲的化学方程式:_______ ;收集甲物质的常用方法是_______
(3)若己物质的水溶液呈浅绿色,向该溶液中加入稀硫酸,溶液变黄色,同时生成丙,写出该过程中发生反应的离子方程式:_______
(4)丁是一种有颜色的气体,写出丁与水反应生成丙和戊的化学方程式,并用双线桥表示电子转移的情况:_______
(5)常温下,戊的浓溶液可以用干燥的铁罐车运输,原因是_______
Ⅱ.将等物质的量的 、
、 混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中
混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中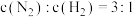 ;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
(6)原容器中 的物质的量是
的物质的量是_______
(7)5min后容器中 的物质的量浓度
的物质的量浓度_______
(8) 的转化率是
的转化率是_______

请回答下列问题:
(1)丙的化学式为
(2)写出实验室制备甲的化学方程式:
(3)若己物质的水溶液呈浅绿色,向该溶液中加入稀硫酸,溶液变黄色,同时生成丙,写出该过程中发生反应的离子方程式:
(4)丁是一种有颜色的气体,写出丁与水反应生成丙和戊的化学方程式,并用双线桥表示电子转移的情况:
(5)常温下,戊的浓溶液可以用干燥的铁罐车运输,原因是
Ⅱ.将等物质的量的
 、
、 混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中
混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中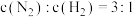 ;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;(6)原容器中
 的物质的量是
的物质的量是(7)5min后容器中
 的物质的量浓度
的物质的量浓度(8)
 的转化率是
的转化率是
您最近半年使用:0次