Ⅰ.图象具有直观、线索清晰、引导性强等特点,有利于提高统筹思维和概括能力。图是氮元素的化合价与部分常见含氮物质的关系。

请回答下列问题:
(1)丙的化学式为_______
(2)写出实验室制备甲的化学方程式:_______ ;收集甲物质的常用方法是_______
(3)若己物质的水溶液呈浅绿色,向该溶液中加入稀硫酸,溶液变黄色,同时生成丙,写出该过程中发生反应的离子方程式:_______
(4)丁是一种有颜色的气体,写出丁与水反应生成丙和戊的化学方程式,并用双线桥表示电子转移的情况:_______
(5)常温下,戊的浓溶液可以用干燥的铁罐车运输,原因是_______
Ⅱ.将等物质的量的 、
、 混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中
混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中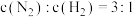 ;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
(6)原容器中 的物质的量是
的物质的量是_______
(7)5min后容器中 的物质的量浓度
的物质的量浓度_______
(8) 的转化率是
的转化率是_______

请回答下列问题:
(1)丙的化学式为
(2)写出实验室制备甲的化学方程式:
(3)若己物质的水溶液呈浅绿色,向该溶液中加入稀硫酸,溶液变黄色,同时生成丙,写出该过程中发生反应的离子方程式:
(4)丁是一种有颜色的气体,写出丁与水反应生成丙和戊的化学方程式,并用双线桥表示电子转移的情况:
(5)常温下,戊的浓溶液可以用干燥的铁罐车运输,原因是
Ⅱ.将等物质的量的
 、
、 混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中
混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中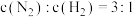 ;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;(6)原容器中
 的物质的量是
的物质的量是(7)5min后容器中
 的物质的量浓度
的物质的量浓度(8)
 的转化率是
的转化率是
更新时间:2022-04-23 11:02:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)实验室制取氯气反应的化学方程式为:_________ ;
①在该反应中,氧化剂与还原剂的物质的量之比是_________ ;
②若在反应中生成了标况下2.24L氯气,则电子转移的个数是________ NA。
(2)氯酸钾和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
①用双线桥表示上述反应中电子转移的方向和数目_________ ;
②浓盐酸在该反应中表现的性质是__________ (填序号) ;
;
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③该反应的还原产物是___________ (填化学式);
④上述反应产生0.1molCl2时,转移电子的物质的量为___________ 。
①在该反应中,氧化剂与还原剂的物质的量之比是
②若在反应中生成了标况下2.24L氯气,则电子转移的个数是
(2)氯酸钾和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
①用双线桥表示上述反应中电子转移的方向和数目
②浓盐酸在该反应中表现的性质是
 ;
;A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③该反应的还原产物是
④上述反应产生0.1molCl2时,转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】实验室中可以利用反应KClO3+6HCl═KCl+3Cl2↑+3H2O来制取氯气。
(1)用双线桥标出该反应中电子转移的方向和数目_____________________ KClO3+6HCl(浓)═KCl+3Cl2+3H2O
(2)该反应中还原剂是_____ ,还原产物是______ .
(3)若有1molHCl完全反应,则转移的电子得到物质的量是_______ mol
(1)用双线桥标出该反应中电子转移的方向和数目
(2)该反应中还原剂是
(3)若有1molHCl完全反应,则转移的电子得到物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】新型陶瓷材料氮化硅(Si3N4)可用于制作火箭发动机中燃料的喷嘴。氮化硅可由石英、焦炭在高温氮气流中制取。完成下列填空:______SiO2+______C+______N2 ______Si3N4+______CO。
______Si3N4+______CO。
(1)试配平该化学反应方程式,将系数填写在对应位置上。在方程式上标出电子转移的方向和数目。____________
(2)反应中______ 被还原,当氧化产物比还原产物多 1mol 时,反应中电子转移数为______ 。
(3)在该反应体系中:所涉及物质属于非极性分子的电子式为______ ;所涉及元素中原子半径最大的原子的最外层电子排布式为______ 。
(4)反应的主要产物氮化硅所属的晶体类型为______ ,证明氮化硅组成元素非金属性强弱:
(Ⅰ)写出一个化学事实______ ;
(Ⅱ)从原子结构上进行说明:______ 。
 ______Si3N4+______CO。
______Si3N4+______CO。(1)试配平该化学反应方程式,将系数填写在对应位置上。在方程式上标出电子转移的方向和数目。
(2)反应中
(3)在该反应体系中:所涉及物质属于非极性分子的电子式为
(4)反应的主要产物氮化硅所属的晶体类型为
(Ⅰ)写出一个化学事实
(Ⅱ)从原子结构上进行说明:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请根据要求书写出方程式。
(1)NO2与水形成酸雨的化学方程式为______________________________ 。
(2)1754年,Briestly用硵砂(主要成份NH4Cl)和熟石灰共热制得了氨,化学反应方程式为______________________________ 。
(3)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程_________________________________ 。
(4)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式_________________________________ 。
(1)NO2与水形成酸雨的化学方程式为
(2)1754年,Briestly用硵砂(主要成份NH4Cl)和熟石灰共热制得了氨,化学反应方程式为
(3)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
(4)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】用方程式回答下列问题。
(1)书写离子方程式。
①将 通入
通入 溶液中:
溶液中:_______ 。
②将 通入
通入 溶液中:
溶液中:_______ 。
③将炽热的炭放入浓 中:
中:_______ 。
(2)书写化学方程式。
①实验室用 和
和 制氨气:
制氨气:_______ 。
②将 通入灼热的
通入灼热的 中,固体由黑色变红色:
中,固体由黑色变红色:_______ 。
③用 可以检验
可以检验 管道是否漏气,若漏气则有白烟生成:
管道是否漏气,若漏气则有白烟生成:_______ 。
④制硝基苯:_______ 。
(1)书写离子方程式。
①将
 通入
通入 溶液中:
溶液中:②将
 通入
通入 溶液中:
溶液中:③将炽热的炭放入浓
 中:
中:(2)书写化学方程式。
①实验室用
 和
和 制氨气:
制氨气:②将
 通入灼热的
通入灼热的 中,固体由黑色变红色:
中,固体由黑色变红色:③用
 可以检验
可以检验 管道是否漏气,若漏气则有白烟生成:
管道是否漏气,若漏气则有白烟生成:④制硝基苯:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮及其化合物在生产生活中有着广泛的应用,但同时随意排放氮的化合物也会造成环境污染问题。
I.某研究性学习小组设计用如图所示实验装置(夹持仪器省略)制取干燥的氨气并验证 具有还原性,请回答下列问题:
具有还原性,请回答下列问题:
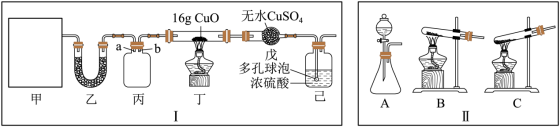
(1)实验室制备氨气有多种方法,现欲用 与熟石灰反应制取
与熟石灰反应制取 ,则甲中的气体发生装置为
,则甲中的气体发生装置为_______ (从Ⅱ中选用)。
(2)装置丙用于收集 ,应将导管
,应将导管_______ (填“a”或“b”)延长至集气瓶底部,装置乙中盛放的试剂为_______ 。
Ⅱ.氨是工业生产硝酸的重要原料,请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
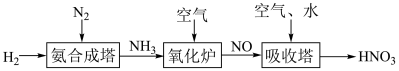
(3)氨气在“氧化炉”中所发生反应的化学方程式_______ 。
(4)“吸收塔”尾部会有含 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下三种方法处理:
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下三种方法处理:
①纯碱溶液吸收法。请用离子方程式表示纯碱吸收 的反应原理:
的反应原理:_______ 。
②氨转化法。已知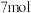 氨恰好能将含
氨恰好能将含 和
和 共
共 的混合气体完全转化为
的混合气体完全转化为 ,则混合气体中
,则混合气体中 和
和 的物质的量之比
的物质的量之比_______ 。
③臭氧脱硝法: 氧化
氧化 结合水洗,可产生
结合水洗,可产生 和氧气,该反应的化学方程式为
和氧气,该反应的化学方程式为_______ 。
Ⅲ.国家规定地下水中氨氧化物的排放标准不超过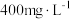 。氮氧化物可以用酸性硫酸亚铁溶液来吸收,反应原理为
。氮氧化物可以用酸性硫酸亚铁溶液来吸收,反应原理为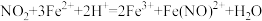 。现测定某地下水脱硝过程中氦氧化物的排放量:收集
。现测定某地下水脱硝过程中氦氧化物的排放量:收集 排放的气体,缓慢通过
排放的气体,缓慢通过 酸性
酸性 溶液(过量),充分反应,量取吸收气体的溶液置于锥形瓶中,用
溶液(过量),充分反应,量取吸收气体的溶液置于锥形瓶中,用 酸性溶液反应过量的
酸性溶液反应过量的 (还原产物为
(还原产物为 ),重复上述实验操作3次,平均消耗酸性溶液的体积为
),重复上述实验操作3次,平均消耗酸性溶液的体积为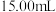 。
。
(5)试通过计算分析地下水脱硝过程中氮氧化物(以 进行计算)的排放是否符合国家标准
进行计算)的排放是否符合国家标准_______ 。(已知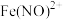 与酸性
与酸性 溶液不反应,写出计算过程)
溶液不反应,写出计算过程)
I.某研究性学习小组设计用如图所示实验装置(夹持仪器省略)制取干燥的氨气并验证
 具有还原性,请回答下列问题:
具有还原性,请回答下列问题:
(1)实验室制备氨气有多种方法,现欲用
 与熟石灰反应制取
与熟石灰反应制取 ,则甲中的气体发生装置为
,则甲中的气体发生装置为(2)装置丙用于收集
 ,应将导管
,应将导管Ⅱ.氨是工业生产硝酸的重要原料,请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:

(3)氨气在“氧化炉”中所发生反应的化学方程式
(4)“吸收塔”尾部会有含
 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下三种方法处理:
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下三种方法处理:①纯碱溶液吸收法。请用离子方程式表示纯碱吸收
 的反应原理:
的反应原理:②氨转化法。已知
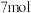 氨恰好能将含
氨恰好能将含 和
和 共
共 的混合气体完全转化为
的混合气体完全转化为 ,则混合气体中
,则混合气体中 和
和 的物质的量之比
的物质的量之比③臭氧脱硝法:
 氧化
氧化 结合水洗,可产生
结合水洗,可产生 和氧气,该反应的化学方程式为
和氧气,该反应的化学方程式为Ⅲ.国家规定地下水中氨氧化物的排放标准不超过
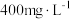 。氮氧化物可以用酸性硫酸亚铁溶液来吸收,反应原理为
。氮氧化物可以用酸性硫酸亚铁溶液来吸收,反应原理为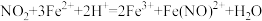 。现测定某地下水脱硝过程中氦氧化物的排放量:收集
。现测定某地下水脱硝过程中氦氧化物的排放量:收集 排放的气体,缓慢通过
排放的气体,缓慢通过 酸性
酸性 溶液(过量),充分反应,量取吸收气体的溶液置于锥形瓶中,用
溶液(过量),充分反应,量取吸收气体的溶液置于锥形瓶中,用 酸性溶液反应过量的
酸性溶液反应过量的 (还原产物为
(还原产物为 ),重复上述实验操作3次,平均消耗酸性溶液的体积为
),重复上述实验操作3次,平均消耗酸性溶液的体积为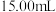 。
。(5)试通过计算分析地下水脱硝过程中氮氧化物(以
 进行计算)的排放是否符合国家标准
进行计算)的排放是否符合国家标准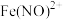 与酸性
与酸性 溶液不反应,写出计算过程)
溶液不反应,写出计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】二氧化碳催化加氢合成乙烯是综合利用 的热点研究领域。回答下列问题:
的热点研究领域。回答下列问题:
(1) 催化加氢生成乙烯和水的反应方程式是
催化加氢生成乙烯和水的反应方程式是_______ 。当反应达到平衡时,若增大压强,则
_______ (填“变大”“变小”或“不变")。
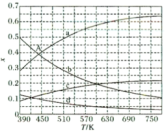
(2)理论计算表明,原料初始组成 ,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。图中,表示
,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。图中,表示 、
、 变化的曲线分别是
变化的曲线分别是_______ 、_______ 。 催化加氢合成
催化加氢合成 反应的
反应的
_______ 0(填“大于”或“小于”)。
(3)根据图中点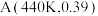 ,计算该温度时反应的平衡常数
,计算该温度时反应的平衡常数
_______  (列出计算式。以分压表示,分压=总压×物质的量分数)。
(列出计算式。以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成 、
、 、
、 等低碳经。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当
等低碳经。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当_______ 。
 的热点研究领域。回答下列问题:
的热点研究领域。回答下列问题:(1)
 催化加氢生成乙烯和水的反应方程式是
催化加氢生成乙烯和水的反应方程式是
(2)理论计算表明,原料初始组成
 ,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。图中,表示
,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。图中,表示 、
、 变化的曲线分别是
变化的曲线分别是 催化加氢合成
催化加氢合成 反应的
反应的

(3)根据图中点
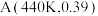 ,计算该温度时反应的平衡常数
,计算该温度时反应的平衡常数
 (列出计算式。以分压表示,分压=总压×物质的量分数)。
(列出计算式。以分压表示,分压=总压×物质的量分数)。(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成
 、
、 、
、 等低碳经。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当
等低碳经。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】碳及其化合物在化工生产中有着广泛的应用。
I.为解决大气中CO2的含量增大的问题,某科学家提出如下构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,在合成塔中经化学反应使废气中的CO2转变为燃料甲醇。部分技术流程如下:
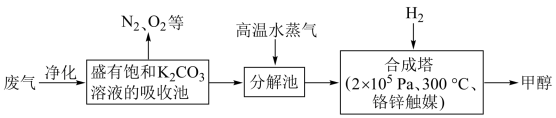
(1)吸收池中反应的化学方程式为K2CO3+CO2+H2O=2KHCO3,△H<0。该反应为可逆反应,从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,其原因是____________________ ,_________________________
(2)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=-890.3kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ/mol
如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。写出CO2(g)与H2(g)反应生CH4(g)与液态水的热化学方程式_____________ 。
II.某兴趣小组模拟工业合成甲醇的反应:CO(g)+2H2(g) CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:
CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:
(1)从反应开始到20min时,以CO表示反应速率为___________________
(2)下列描述能说明反应达到平衡 是
是_______
A.装置内CO和H2的浓度比值不再改变
B.容器内气体的平均摩尔质量保持不变
C.容器内气体的压强保持不变
D.容器内气体密度保持不变
(3)该温度下平衡常数K=_______ ,若达到平衡后加入少量CH3OH(g),此时平衡常数K值将_________ (填“增大”、“减小”或“不变”)
(4)该反应达到平衡后,再向容器中充入1mol CO和2mol H2,此时CO的转化率将_____ (填“增大”、“减小”或“不变”)
I.为解决大气中CO2的含量增大的问题,某科学家提出如下构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,在合成塔中经化学反应使废气中的CO2转变为燃料甲醇。部分技术流程如下:

(1)吸收池中反应的化学方程式为K2CO3+CO2+H2O=2KHCO3,△H<0。该反应为可逆反应,从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,其原因是
(2)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H1=-890.3kJ/mol
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ/mol
如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。写出CO2(g)与H2(g)反应生CH4(g)与液态水的热化学方程式
II.某兴趣小组模拟工业合成甲醇的反应:CO(g)+2H2(g)
 CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:
CH3OH(g),在容积固定为2L的密闭容器中充入1mol CO和2mol H2,加入合适的催化剂(催化剂体积忽略不计)后开始反应。测得容器内的压强随时间变化如下:| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/Mpa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(1)从反应开始到20min时,以CO表示反应速率为
(2)下列描述能说明反应达到平衡
 是
是A.装置内CO和H2的浓度比值不再改变
B.容器内气体的平均摩尔质量保持不变
C.容器内气体的压强保持不变
D.容器内气体密度保持不变
(3)该温度下平衡常数K=
(4)该反应达到平衡后,再向容器中充入1mol CO和2mol H2,此时CO的转化率将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在1L密闭容器中发生反应: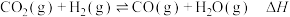 ,其化学平衡常数K与温度T的关系如下表:
,其化学平衡常数K与温度T的关系如下表:
回答下列问题:
(1)该反应的
___________ (填“>”或“<”)0。
(2)某温度时,测得平衡体系中各物质的物质的量浓度相等,则此时对应的温度为___________ ℃。保持温度和体积不变,充入一定量的 ,则平衡常数
,则平衡常数___________ (填“增大”“减小”或“不变”)。
(3)下列措施可以提高 的平衡转化率的是
的平衡转化率的是___________ (填字母)。
A.选择适当的催化剂 B.增大压强
C.及时分离出 D.升高温度
D.升高温度
(4)650℃时,将2 mol 和3 mol
和3 mol  投入上述容器中开始反应,达到平衡时
投入上述容器中开始反应,达到平衡时 的转化率为
的转化率为___________ 。
(5)800℃时,某时刻测得 、
、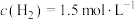 、
、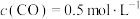 、
、 ,则此时反应是否达到平衡状态
,则此时反应是否达到平衡状态
____ (填“是”或“否”),此时,v(正)___________ (填“>”“<”或“=”)v(逆)。
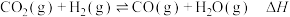 ,其化学平衡常数K与温度T的关系如下表:
,其化学平衡常数K与温度T的关系如下表:| T(℃) | 650 | 700 | 800 | 830 | 1000 |
| K | 0.5 | 0.6 | 0.9 | 1.0 | 1.7 |
(1)该反应的

(2)某温度时,测得平衡体系中各物质的物质的量浓度相等,则此时对应的温度为
 ,则平衡常数
,则平衡常数(3)下列措施可以提高
 的平衡转化率的是
的平衡转化率的是A.选择适当的催化剂 B.增大压强
C.及时分离出
 D.升高温度
D.升高温度(4)650℃时,将2 mol
 和3 mol
和3 mol  投入上述容器中开始反应,达到平衡时
投入上述容器中开始反应,达到平衡时 的转化率为
的转化率为(5)800℃时,某时刻测得
 、
、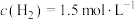 、
、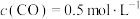 、
、 ,则此时反应是否达到平衡状态
,则此时反应是否达到平衡状态
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请列举铁与硝酸反应的各种情况,写出相关的离子方程式_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁及其化合物在工农业生产、环境保护等领域中有着重要的作用。
(1)酸性条件下,硫酸亚铁可将MnO2还原为MnSO4,该反应的离子方程式为:_____________ 。
(2)分析表明,铁在浓硫酸中发生钝化时,生成的氧化物中Fe、O两种元素的质量比为28∶11,则其化学式为______________ 。
(3)铁及其化合物可用于消除环境污染。常温下,硫酸亚铁能将SO2转化为 ,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为
,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为____________________ 。
常温下,用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2反应可生成0.5 mol N2,则y=____________ 。
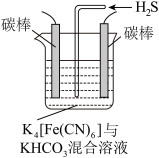
(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2 +H2S=2[Fe(CN)6]4-+2H
+H2S=2[Fe(CN)6]4-+2H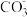 +S↓。电解时,阳极的电极反应式为
+S↓。电解时,阳极的电极反应式为___________ ;电解过程中阴极区溶液的pH______________ (填“变大”、“变小”或“不变”)。
(1)酸性条件下,硫酸亚铁可将MnO2还原为MnSO4,该反应的离子方程式为:
(2)分析表明,铁在浓硫酸中发生钝化时,生成的氧化物中Fe、O两种元素的质量比为28∶11,则其化学式为
(3)铁及其化合物可用于消除环境污染。常温下,硫酸亚铁能将SO2转化为
 ,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为
,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为常温下,用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2反应可生成0.5 mol N2,则y=

(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2
 +H2S=2[Fe(CN)6]4-+2H
+H2S=2[Fe(CN)6]4-+2H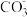 +S↓。电解时,阳极的电极反应式为
+S↓。电解时,阳极的电极反应式为
您最近一年使用:0次



