电冶金
利用电解熔融盐或氧化物的方法来冶炼活泼金属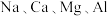 等.
等.
利用电解熔融盐或氧化物的方法来冶炼活泼金属
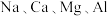 等.
等.| 总反应化学方程式 | 阳极、阴极反应式 | |
| 冶炼钠 | 阳极: 阴极: | |
| 冶炼镁 | 阳极: 阴极: | |
| 冶炼铝 | 阳极: 阴极: |
2023高三·全国·专题练习 查看更多[1]
(已下线)第六章 化学反应与能量 第37讲 电解池 金属的腐蚀与防护
更新时间:2023-02-11 20:06:49
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】海洋是一座巨大的宝藏,海水中蕴含80多种元素。氯碱工业和制备金属镁的原料都可来自于海水。
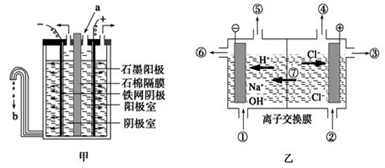
Ⅰ.在氯碱工业中,曾用石棉隔膜电解槽来电解食盐水(如图甲所示)。
(1)写出阳极的反应式____________________________________ 。
(2)图甲中流出的b是______________________ 溶液。
(3)石棉隔膜的作用是______________________________________________ 。
Ⅱ.随着科技的发展,电解工艺不断革新,电解效率和产品纯度得到提高。20世纪80年代起,隔膜法电解工艺逐渐被离子交换膜电解技术取代。
(1)离子交换膜电解槽(如图乙所示)中⑥、⑦分别是_______ 、______________ 。
(2)已知一个电子的电量是1.602×10-19C,用离子膜电解槽电解饱和食盐水,当电路中通过1.929×105 C的电量时,生成NaOH________ g。
Ⅲ.下图是工业上生产镁的流程。

(1)写出下列反应的化学方程式:
①沉淀池:_____________________ ; ②电解:______________________________ ;
(2)整个生产流程中循环使用的物质是______________ 。
(3)简述加热氯化镁的结晶水合物使之脱水转化为无水氯化镁的注意事项:__________________ 。

Ⅰ.在氯碱工业中,曾用石棉隔膜电解槽来电解食盐水(如图甲所示)。
(1)写出阳极的反应式
(2)图甲中流出的b是
(3)石棉隔膜的作用是
Ⅱ.随着科技的发展,电解工艺不断革新,电解效率和产品纯度得到提高。20世纪80年代起,隔膜法电解工艺逐渐被离子交换膜电解技术取代。
(1)离子交换膜电解槽(如图乙所示)中⑥、⑦分别是
(2)已知一个电子的电量是1.602×10-19C,用离子膜电解槽电解饱和食盐水,当电路中通过1.929×105 C的电量时,生成NaOH
Ⅲ.下图是工业上生产镁的流程。

(1)写出下列反应的化学方程式:
①沉淀池:
(2)整个生产流程中循环使用的物质是
(3)简述加热氯化镁的结晶水合物使之脱水转化为无水氯化镁的注意事项:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】C、N、O、Na、Mg、Al、S、Cl是常见的八种元素,根据元素及其化合物性质,回答下列问题:
(1)S在周期表中的位置为______ ;CO2的电子式是_______ 。
(2)比较O、Na元素常见离子的半径大小(用化学式表示,下同)____>____;__________ 比较S、Cl元素的最高价氧化物对应水化物的酸性强弱: ____>____ 。_______________
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是___________ ;制铝时,电解Al2O3而不电解AlCl3的原因是___________ 。
(4)碳与镁形成的1 mol化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃, 该烃分子中碳氢质量比为9:1,烃的结构简式为______ ;Q的化学式为_______ 。
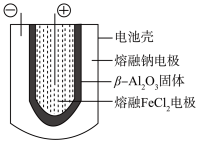
(5)熔融状态下,钠和FeCl2能组成可充电电池(装置示意图如下),反应原理为:2Na+ FeCl2 Fe + 2NaCl .放电时,电池的正极反应式为
Fe + 2NaCl .放电时,电池的正极反应式为___________ ;充电时,_______ (写物质名称)电极接电源的负极;该电池的电解质为_______ 。
(1)S在周期表中的位置为
(2)比较O、Na元素常见离子的半径大小(用化学式表示,下同)____>____;
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是
(4)碳与镁形成的1 mol化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃, 该烃分子中碳氢质量比为9:1,烃的结构简式为
(5)熔融状态下,钠和FeCl2能组成可充电电池(装置示意图如下),反应原理为:2Na+ FeCl2
 Fe + 2NaCl .放电时,电池的正极反应式为
Fe + 2NaCl .放电时,电池的正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】海水中富含镁,可经过加碱沉淀、过滤、酸溶、结晶及脱水等步骤得到无水氯化镁,最后电解得到金属镁。已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]= 1.0×10-38。 当溶液中离子浓度≤1.0×10-5 mol·L-1可视为沉淀完全。
(1)有浓度为1.8×10-3mol·L-1的MgCl2溶液,该溶液中含有少量Fe3+,当溶液中Fe3+沉淀完全时,Mg 2+ 是否开始沉淀__________ ,Mg(OH)2开始沉淀时溶液的pH为________ 。
(2)除去MgCl2酸性溶液中少量的FeCl3,可加入的试剂有____________ 。
a.MgO b.Mg(OH)2 c.NH3·H2O d.MgSO4
(3)若在空气中加热MgCl2·6H2O,可生成Mg(OH)Cl或MgO,写出生成Mg(OH)Cl或MgO相关的化 学方程式_________________________ 。
(4)MgCl2·6H2O在干燥的HCl气流中加热可得到无水氯化镁,其原因是______________ 。
(5)电解熔融的MgCl2,阳极的电极反应式为:_________________ 。
(1)有浓度为1.8×10-3mol·L-1的MgCl2溶液,该溶液中含有少量Fe3+,当溶液中Fe3+沉淀完全时,Mg 2+ 是否开始沉淀
(2)除去MgCl2酸性溶液中少量的FeCl3,可加入的试剂有
a.MgO b.Mg(OH)2 c.NH3·H2O d.MgSO4
(3)若在空气中加热MgCl2·6H2O,可生成Mg(OH)Cl或MgO,写出生成Mg(OH)Cl或MgO相关的化 学方程式
(4)MgCl2·6H2O在干燥的HCl气流中加热可得到无水氯化镁,其原因是
(5)电解熔融的MgCl2,阳极的电极反应式为:
您最近一年使用:0次



