利用如图所示的“价-类”二维图,可以从物质类别、化合价角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
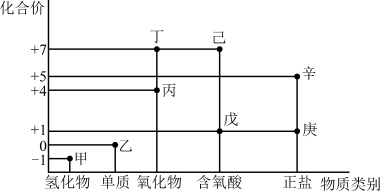
(1)将新制乙的水溶液滴加几滴到干燥的有色纸条上观察到的现象是_____ 。
(2)戊的结构式为______ ;甲、乙、丙、戊中,属于非电解质的是______ (填化学式)。
(3)丙是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂,丙在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是_____ (填字母序号)。
a.Fe2(SO4)3 b.HClO4 c.SO2 d.KMnO4
(4)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
①写出氯气和NaOH溶液生产此消毒液的离子方程式______ ;该“84消毒液”有效成分的物质的量浓度为_____ (结果保留1位小数)。
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18.0mol/L的浓硫酸配制90mL 0.90mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要量取上述浓硫酸的体积为_____ mL(结果保留1位小数).若所配制的稀硫酸浓度大于0.90mol/L,则可能的原因是_____ 。
A.配制前,容量瓶未干燥
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.浓硫酸溶解后未恢复到室温,立即转移至容量瓶定容
D.转移硫酸溶液至容量瓶时,有少量溶液溅出
E.定容时,仰视容量瓶刻度线进行定容

(1)将新制乙的水溶液滴加几滴到干燥的有色纸条上观察到的现象是
(2)戊的结构式为
(3)丙是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂,丙在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是a.Fe2(SO4)3 b.HClO4 c.SO2 d.KMnO4
(4)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
| 84消毒液 有效成分 NaClO 规格 500mL 质量分数 25% 密度 1.19g•cm-3 |
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18.0mol/L的浓硫酸配制90mL 0.90mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要量取上述浓硫酸的体积为
A.配制前,容量瓶未干燥
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.浓硫酸溶解后未恢复到室温,立即转移至容量瓶定容
D.转移硫酸溶液至容量瓶时,有少量溶液溅出
E.定容时,仰视容量瓶刻度线进行定容
更新时间:2023-02-17 13:45:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】2019年是“国际化学元素周期表年”。元素周期表中的成员数不断增加,ⅤA族元素是元素周期表中的重要组成元素。
(1)2016年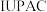 确认了四种新元素,其中之一为
确认了四种新元素,其中之一为 ,中文名为“镆”,位于第七周期ⅤA族,
,中文名为“镆”,位于第七周期ⅤA族,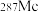 与
与 互为
互为______ 。
(2) 的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是:
的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是: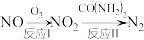
① 的电子式为
的电子式为______ ;反应Ⅰ为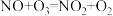 ,其中还原产物为
,其中还原产物为______ ;每消除 ,转移电子
,转移电子______  。
。
②反应Ⅱ中氧化产物与还原产物的质量比为______ 。
(3)①三碘化磷( )是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷(
)是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷( )与
)与 在
在 溶剂中反应制得。该反应的化学方程式为
溶剂中反应制得。该反应的化学方程式为______ 。制备时常在溶剂中加入 ,其作用是
,其作用是______ 。
②亚磷酸( )是一种中强酸,与足量的
)是一种中强酸,与足量的 溶液反应生成
溶液反应生成 和
和 。
。 属于
属于______ 元酸(填“一”“二”或“三”), 属于
属于______ (填“正盐”或“酸式盐”)。亚磷酸具有强还原性,能与 溶液反应置换出
溶液反应置换出 ,写出其离子反应方程式
,写出其离子反应方程式______ 。
(1)2016年
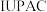 确认了四种新元素,其中之一为
确认了四种新元素,其中之一为 ,中文名为“镆”,位于第七周期ⅤA族,
,中文名为“镆”,位于第七周期ⅤA族,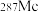 与
与 互为
互为(2)
 的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是:
的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是: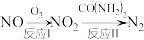
①
 的电子式为
的电子式为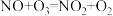 ,其中还原产物为
,其中还原产物为 ,转移电子
,转移电子 。
。②反应Ⅱ中氧化产物与还原产物的质量比为
(3)①三碘化磷(
 )是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷(
)是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷( )与
)与 在
在 溶剂中反应制得。该反应的化学方程式为
溶剂中反应制得。该反应的化学方程式为 ,其作用是
,其作用是②亚磷酸(
 )是一种中强酸,与足量的
)是一种中强酸,与足量的 溶液反应生成
溶液反应生成 和
和 。
。 属于
属于 属于
属于 溶液反应置换出
溶液反应置换出 ,写出其离子反应方程式
,写出其离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮是植物体内蛋白质、叶绿素的重要组成元素,氮肥能促进农作物的生长。氨是生产氮肥的原料。氮及其部分化合物的转化关系如图所示,回答下列问题:
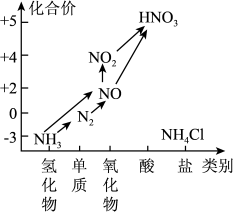
(1)下列反应中,不属于氮的固定的是_______
(2)氨的电子式是_______ 。
(3)在物质转化图中的各气体,可用排水法收集的气体是_______ (填化学式,下同),既可以用浓硫酸干燥,又可以用碱石灰干燥的是气体是_______ 。
(4)实验室常用NH4Cl与Ca(OH)2制取氨气,请写出该反应的化学方程式_______ 。而工业上则由氮气和氢气直接合成氨,该反应的化学方程式为_______ 。
(5)NO、CO都是汽车尾气的主要成分,直接排放会污染空气,人们研究出一种催化剂,可将两种气体通过,反应转化为无污染的空气成分,则反应的化学方程式是_______ 。
(6)氮的一种化合物肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,则断裂1molN-H所需的能量是_______ kJ。


(1)下列反应中,不属于氮的固定的是_______
| A.N2和H2在一定条件下合成NH3 |
| B.豆科植物把空气中的氮气转化为化合态的氮 |
| C.雷电时,空气中的N2与O2反应生成NO |
| D.由NH3制碳酸氢铵 |
(3)在物质转化图中的各气体,可用排水法收集的气体是
(4)实验室常用NH4Cl与Ca(OH)2制取氨气,请写出该反应的化学方程式
(5)NO、CO都是汽车尾气的主要成分,直接排放会污染空气,人们研究出一种催化剂,可将两种气体通过,反应转化为无污染的空气成分,则反应的化学方程式是
(6)氮的一种化合物肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,则断裂1molN-H所需的能量是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】自然界的矿物,岩石的成因和变化收到许多条件的影响。地壳内每增加1km,压强增大约25000-30000kPa。在地壳内SiO2和HF存在一下平衡:SiO2(s) +4HF(g)  SiF4(g)+ 2H2O(g) +148.9kJ。
SiF4(g)+ 2H2O(g) +148.9kJ。
(1)写出H2O的电子式:___________ ,SiF4的结构式:____________
(2)在地壳深处容易有___________ 气体逸出,在地壳浅处容易有___________ 沉积。该反应的平衡常数表达式为:K=_______________ 。如果上述反应的平衡常数K值变大,该反应_______ (选填编号)。
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,______ (选填编号)。
a.2v正(HF)=v逆(H2O) b.v正(H2O)=2v逆(SiF4)
c.SiO2的质量保持不变 d.反应物不再转化为生成物
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为______ 。
 SiF4(g)+ 2H2O(g) +148.9kJ。
SiF4(g)+ 2H2O(g) +148.9kJ。(1)写出H2O的电子式:
(2)在地壳深处容易有
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,
a.2v正(HF)=v逆(H2O) b.v正(H2O)=2v逆(SiF4)
c.SiO2的质量保持不变 d.反应物不再转化为生成物
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有下列物质:①酒精② 溶液③熔融
溶液③熔融 ④
④ ⑤稀硫酸⑥
⑤稀硫酸⑥ 溶液⑦铁⑧
溶液⑦铁⑧ 固体
固体
(1)上述物质中,可导电的是_______ (填序号,下同),属于非电解质的是_______ ,属于电解质但在该状态下不导电的是_______ ;
(2)写出②在水溶液中的电离方程式:_______ ;
(3)向⑧的水溶液中滴加少量②溶液,反应的离子方程式为:_______ 。
 溶液③熔融
溶液③熔融 ④
④ ⑤稀硫酸⑥
⑤稀硫酸⑥ 溶液⑦铁⑧
溶液⑦铁⑧ 固体
固体(1)上述物质中,可导电的是
(2)写出②在水溶液中的电离方程式:
(3)向⑧的水溶液中滴加少量②溶液,反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有下列物质:①Ba(OH)2固体;②熔融的KHSO4;③HNO3;④稀硫酸;⑤CO2;⑥铜;⑦氨水;⑧蔗糖晶体;⑨FeCl3固体;⑩CH3COOH。
(1)上述状态下的物质可导电的是_______ (填序号,下同)。
(2)属于非电解质的是_______ 。
(3)写出KHSO4在水溶液中的电离方程式:_______ 。
(4)写出用⑨制备Fe(OH)3胶体的化学方程式:_______ 。
(5)写出①的溶液与②的溶液恰好中和时的离子方程式:_______ 。
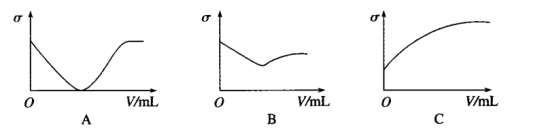
(6)在一定温度下,向不同电解质溶液中加入新物质时溶液电导率(σ)随新物质加入量(V)的变化曲线如图所示。分别与A、B、C曲线变化趋势一致的是_______ 、_______ 、_______ (填序号)。
①向NH3·H2O溶液中通入HCl气体直至过量
②向饱和石灰水中不断通入CO2
③向硝酸中逐滴加入等浓度的氢氧化钾溶液至过量
(1)上述状态下的物质可导电的是
(2)属于非电解质的是
(3)写出KHSO4在水溶液中的电离方程式:
(4)写出用⑨制备Fe(OH)3胶体的化学方程式:
(5)写出①的溶液与②的溶液恰好中和时的离子方程式:
(6)在一定温度下,向不同电解质溶液中加入新物质时溶液电导率(σ)随新物质加入量(V)的变化曲线如图所示。分别与A、B、C曲线变化趋势一致的是

①向NH3·H2O溶液中通入HCl气体直至过量
②向饱和石灰水中不断通入CO2
③向硝酸中逐滴加入等浓度的氢氧化钾溶液至过量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)有以下六种物质:
①乙醇;②Na2CO3溶液;③ 固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
上述状态下的物质中,能导电的有___________ (填序号,下同),属于电解质的有___________ 。
(2)已知H3PO2是一元弱酸,NaH2PO2属于___________ (填:酸式盐、正盐或者碱式盐)。写出H3PO2与足量NaOH溶液反应的离子方程式:___________
(3)某种飞船以联氨 和
和 为动力源,发生反应:
为动力源,发生反应: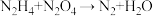 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。
①配平该方程式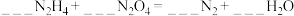 。
。___________
②该反应中,氧化产物与还原产物的质量之比为___________ 。
(4)补全并配平下列方程式
①_______ _______HCl=______KCl+______
_______HCl=______KCl+______ ______
______ ______
______
___________
②______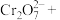 _______
_______ _______H+=______
_______H+=______ _______
_______ ________
________ ___________
(1)有以下六种物质:
①乙醇;②Na2CO3溶液;③
 固体;④液态氯化氢;⑤冰醋酸;⑥石墨。
固体;④液态氯化氢;⑤冰醋酸;⑥石墨。上述状态下的物质中,能导电的有
(2)已知H3PO2是一元弱酸,NaH2PO2属于
(3)某种飞船以联氨
 和
和 为动力源,发生反应:
为动力源,发生反应: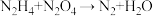 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。①配平该方程式
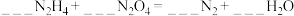 。
。②该反应中,氧化产物与还原产物的质量之比为
(4)补全并配平下列方程式
①_______
 _______HCl=______KCl+______
_______HCl=______KCl+______ ______
______ ______
______
②______
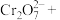 _______
_______ _______H+=______
_______H+=______ _______
_______ ________
________
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】实验室用高锰酸钾和浓盐酸反应制备氯气:2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
(1)用双线桥法标出上述反应方程式中电子转移的方向与数目___ 。
(2)上述反应中,氧化剂是___ (填化学式,下同),氧化产物___ ,浓盐酸体现了___ 性和____ 性,当有4mol水生成的时候,转移的电子有___ mol。
(3)实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是___ (填写化学式),请用化学方程式表示该反应的原理___ 。
(4)若在标准状况下,将一个充满HCl气体的集气瓶倒扣于盛水的水槽中,水充满整个集气瓶,(假设HCl全部留在集气瓶内),则该集气瓶内溶液中HCl的物质的量浓度为___ mol/L。(保留三位小数)
(1)用双线桥法标出上述反应方程式中电子转移的方向与数目
(2)上述反应中,氧化剂是
(3)实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是
(4)若在标准状况下,将一个充满HCl气体的集气瓶倒扣于盛水的水槽中,水充满整个集气瓶,(假设HCl全部留在集气瓶内),则该集气瓶内溶液中HCl的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】由氢气和氯气组成的混合气体,经光照充分反应后,通入100mL1molLNaOH溶液中,溶液中某种离子的物质的量(图甲)和溶液的导电性(图乙)随着反应后的混合气体通入体积的变化而变化。
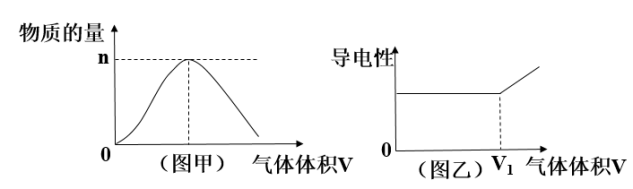
(1)图甲曲线表示溶液中___________ 离子的变化。
(2)对溶液进行导电性实验时,发现当通入的光照反应后的混合气体体积大于V1时,随着混合气体的通入,溶液导电性明显增强,引起导电性增强的主要正、负离子是___________ 。
(3)当图甲中n=0.01mol时,则光照前的混合气体中H2和Cl2的物质的量之比为___________ 。(书写必要步骤)

(1)图甲曲线表示溶液中
(2)对溶液进行导电性实验时,发现当通入的光照反应后的混合气体体积大于V1时,随着混合气体的通入,溶液导电性明显增强,引起导电性增强的主要正、负离子是
(3)当图甲中n=0.01mol时,则光照前的混合气体中H2和Cl2的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择。
(1)①处理该钢瓶的方法正确的是_______ 。
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是_______ 。
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ;氯水可作为漂白剂,起主要作用的是氯水中含有的_______ (用化学式表示)。
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是_______ (化学方程式);根据这一原理,工业上常用廉价的石灰乳吸收制得漂白粉,漂白粉的有效成分是_______ (填化学式)。
(1)①处理该钢瓶的方法正确的是
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】用0.100mol·L-1NaOH溶液滴定等浓度的20mL柠檬酸溶液,滴定曲线如下图所示:_____ 、______ 。
(2)图中50~60mL之间,反应的离子方程式为_______ 。
(3)滴定终点的指示剂选用_______试液。
(4)在上述滴定过程中,各微粒浓度大小关系正确的是_______。
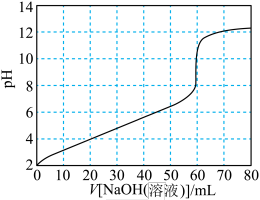
(2)图中50~60mL之间,反应的离子方程式为
(3)滴定终点的指示剂选用_______试液。
| A.无色酚酞 | B.甲基橙 | C.紫色石蕊 | D.品红 |
(4)在上述滴定过程中,各微粒浓度大小关系正确的是_______。
A. 时, 时,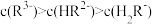 |
B. 时, 时,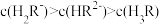 |
C. 时, 时,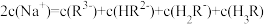 |
D. 时, 时,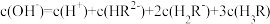 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B升华 C结晶 D过滤 E蒸馏 F分液
①分离饱和食盐水与沙子的混合物______ ;
②从硝酸钾和氯化钠的混合液中获得硝酸钾________ ;
③从碘水中提取碘单质______ ;
④分离CCl4,(沸点为76.75℃)和甲苯(沸点110.6℃)的混合物_________ 。
(2)实验室用NaCO3·10H2O晶体配制0. 5mol/L的Na2CO3溶液970mL,应用托盘天平称取Na2CO3·10H2O的质量是______ 。
(3)已知两种碱AOH和BOH的摩尔质量之比为5:7,现将7molAOH与5mol BOH混合后,从中取出5.6g,恰好可以中和100mL浓度为1.2mol/L的盐酸,则AOH的摩尔质量为____ 。
(4)某学生欲用12mol·L-1浓盐酸和蒸馏水配制500 mL 0.3 mol·L-1的稀盐酸。
①该学生需要用量筒量取____ mL 上述浓盐酸进行配制。
②下列实验操作会导致所配制的稀盐酸的物质的量浓度偏小的是_____ (填序号)。
a用量筒量取浓盐酸时俯视观察凹液面
b将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中
c稀释浓盐酸时,未冷却到室温即转移到容量瓶中
d定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
e容量瓶洗涤干净后未干燥
A萃取分液 B升华 C结晶 D过滤 E蒸馏 F分液
①分离饱和食盐水与沙子的混合物
②从硝酸钾和氯化钠的混合液中获得硝酸钾
③从碘水中提取碘单质
④分离CCl4,(沸点为76.75℃)和甲苯(沸点110.6℃)的混合物
(2)实验室用NaCO3·10H2O晶体配制0. 5mol/L的Na2CO3溶液970mL,应用托盘天平称取Na2CO3·10H2O的质量是
(3)已知两种碱AOH和BOH的摩尔质量之比为5:7,现将7molAOH与5mol BOH混合后,从中取出5.6g,恰好可以中和100mL浓度为1.2mol/L的盐酸,则AOH的摩尔质量为
(4)某学生欲用12mol·L-1浓盐酸和蒸馏水配制500 mL 0.3 mol·L-1的稀盐酸。
①该学生需要用量筒量取
②下列实验操作会导致所配制的稀盐酸的物质的量浓度偏小的是
a用量筒量取浓盐酸时俯视观察凹液面
b将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中
c稀释浓盐酸时,未冷却到室温即转移到容量瓶中
d定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
e容量瓶洗涤干净后未干燥
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室中有一未知浓度的稀盐酸,某同学在实验室中进行实验测定盐酸的浓度。请完成下列填空:
(1)配制100 mL 0.10 mol/L NaOH标准溶液。
①主要操作步骤:计算―→称量―→溶解―→___________ (冷却后)―→洗涤(并将洗涤液移入容量瓶)―→_____________ ―→_____________ ―→将配制好的溶液倒入试剂瓶中,贴上标签。
②称量___________ g NaOH固体所需仪器有:天平(带砝码、镊子)、____________ 、_____________ 。
(2)取20.00 mL待测盐酸放入锥形瓶中,并滴加 2~3 滴酚酞作指示剂,用配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
①滴定达到终点的标志是________ 。
②根据上述数据,可计算出该盐酸的浓度约为___________ (保留两位有效数字)。
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________________ 。
A.滴定终点读数时俯视读数B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥D.碱式滴定管尖嘴部分有气泡,滴定后消失
(1)配制100 mL 0.10 mol/L NaOH标准溶液。
①主要操作步骤:计算―→称量―→溶解―→
②称量
(2)取20.00 mL待测盐酸放入锥形瓶中,并滴加 2~3 滴酚酞作指示剂,用配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
| 实验编号 | NaOH溶液的浓度( mol/L ) | 滴定完成时,滴入NaOH溶液的体积( mL ) | 待测盐酸的体积( mL ) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的标志是
②根据上述数据,可计算出该盐酸的浓度约为
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有
A.滴定终点读数时俯视读数B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥D.碱式滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次



