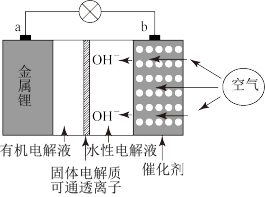
某小组学生研究常见的金属腐蚀现象,分析其原理.按要求回答下列问题.
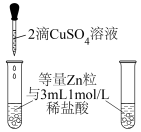
(1)甲同学设计如图所示对比实验。
当a中滴入CuSO4溶液后,观察到其中产生气泡的速率较b中的________ 。其原因是________________ 。
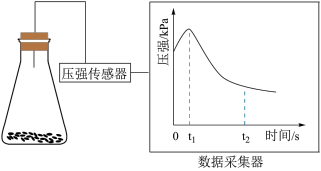
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。
① 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为________ 。
② 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为________________ 。
③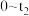 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为________________ 。
(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
①暖贴工作时,铁粉发生的反应为________ (填“氧化反应”或“还原反应”)。
②写出使用暖贴时的注意事项:________________ 。
③暖贴发热时,正极材料为________ ;食盐的作用为________ 。
④当暖贴放热结束时,铁粉转化成的物质中可能含有________ 。

(1)甲同学设计如图所示对比实验。
当a中滴入CuSO4溶液后,观察到其中产生气泡的速率较b中的
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。

①
 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为②
 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为③
 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
| 品名:一次性保暖贴 主要成分:铁粉、水、食盐、活性炭、蛭石、吸水性树脂 产品性能:平均温度 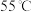 ,最高温度 ,最高温度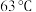 ,发热时间12小时以上 ,发热时间12小时以上 |
②写出使用暖贴时的注意事项:
③暖贴发热时,正极材料为
④当暖贴放热结束时,铁粉转化成的物质中可能含有
22-23高二上·天津河西·期末 查看更多[2]
更新时间:2023-02-23 16:01:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
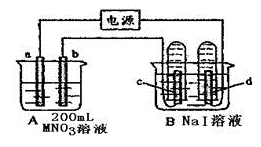
【推荐1】如下图装置中,b电极用金属 M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答:
(1)a为__________ 极,c极的电极反应式为_________________ 。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:__________ ,电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应为_________________ 。
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了_____ moL气体,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为_____________ 。
(1)a为
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】人们利用电化学原理满足不同的需求。下列每小题中的电化学原理广泛应用于日常生活、生产和科学技术等方面,请根据题中提供的信息填空。
(1)蓄电池在放电时起原电池的作用,在充电时起电解池的作用。铅蓄电池属于_______ (填“一次”或“二次”)电池,铅蓄电池的总反应为Pb+PbO2+2H2SO4 2PbSO4+2H2O,铅蓄电池的放电反应与充电反应
2PbSO4+2H2O,铅蓄电池的放电反应与充电反应_______ (填“是”或“不是”)可逆反应。
(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
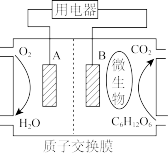
①B为微生物燃料电池的_______ (填“正”或“负”)极。
②正极的电极反应式为_______ 。
③电池工作过程中,H+将移向_______ (填“正”或“负”)极。
④在电池反应中,每消耗1mol氧气,理论上转移的电子的物质的量为_______ 。
(3)若将反应Cu+2FeCl3=CuCl2+2FeCl2设计成原电池,则该电池的正极材料可以是_______ (填“铜片”或“石墨”)。请在烧杯中画出你所设计的原电池的装置图,并标注出电极材料和电解质溶液_______ 。

(1)蓄电池在放电时起原电池的作用,在充电时起电解池的作用。铅蓄电池属于
 2PbSO4+2H2O,铅蓄电池的放电反应与充电反应
2PbSO4+2H2O,铅蓄电池的放电反应与充电反应(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①B为微生物燃料电池的
②正极的电极反应式为
③电池工作过程中,H+将移向
④在电池反应中,每消耗1mol氧气,理论上转移的电子的物质的量为
(3)若将反应Cu+2FeCl3=CuCl2+2FeCl2设计成原电池,则该电池的正极材料可以是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据化学能和热能、电能相关的知识,问答下列问题:
(1)下列变化中,属于吸热反应的是_______ (填序号)。
①液态水汽化 ② 与固体
与固体 混合 ③浓
混合 ③浓 稀释
稀释
④ ⑤生石灰跟水反应生成熟石灰 ⑥
⑤生石灰跟水反应生成熟石灰 ⑥
(2)已知在101kPa、273K时,1g甲烷 燃烧生成
燃烧生成 和液态水,放出55.6kJ的热量,则甲烷燃烧热的热化学方程式为
和液态水,放出55.6kJ的热量,则甲烷燃烧热的热化学方程式为_______ 。
(3)已知:
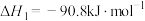



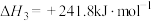
根据上述反应

_______ 
(4)航天技术上使用的氢—氧燃料电池原理可以简单看作下图,则:
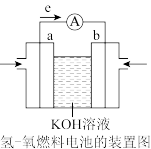
①原电池工作时涉及的能量转化形式是_______ 。
②a极为电池的_______ (填“正极”或“负极”);溶液中 移向
移向_______ 电极(填“a”或“b”);
该氢氧燃料电池的正极反应式为_______ 。
③如把 改为乙醇蒸汽(
改为乙醇蒸汽( ),则负极电极反应式为:
),则负极电极反应式为:_______ 。
(5)某学校化学兴趣小组的同学发现:实验室用稀硫酸和锌粒制取 时,加入几滴硫酸铜溶液,生成氢气的速率明显加快,并且反应结束后容器中有少量红色固体剩余。已知:将氧化还原反应设计成原电池时会加快反应速率,则在本实验中,加入几滴
时,加入几滴硫酸铜溶液,生成氢气的速率明显加快,并且反应结束后容器中有少量红色固体剩余。已知:将氧化还原反应设计成原电池时会加快反应速率,则在本实验中,加入几滴 溶液可以加快生成氢气的速率的原因是
溶液可以加快生成氢气的速率的原因是_______ 。
(6)实验室中现有 、
、 、
、 、
、 等4种溶液,可与上述实验中
等4种溶液,可与上述实验中 溶液起相似作用的是
溶液起相似作用的是_______ 。
(1)下列变化中,属于吸热反应的是
①液态水汽化 ②
 与固体
与固体 混合 ③浓
混合 ③浓 稀释
稀释④
 ⑤生石灰跟水反应生成熟石灰 ⑥
⑤生石灰跟水反应生成熟石灰 ⑥
(2)已知在101kPa、273K时,1g甲烷
 燃烧生成
燃烧生成 和液态水,放出55.6kJ的热量,则甲烷燃烧热的热化学方程式为
和液态水,放出55.6kJ的热量,则甲烷燃烧热的热化学方程式为(3)已知:

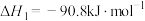



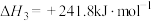
根据上述反应



(4)航天技术上使用的氢—氧燃料电池原理可以简单看作下图,则:

①原电池工作时涉及的能量转化形式是
②a极为电池的
 移向
移向该氢氧燃料电池的正极反应式为
③如把
 改为乙醇蒸汽(
改为乙醇蒸汽( ),则负极电极反应式为:
),则负极电极反应式为:(5)某学校化学兴趣小组的同学发现:实验室用稀硫酸和锌粒制取
 时,加入几滴硫酸铜溶液,生成氢气的速率明显加快,并且反应结束后容器中有少量红色固体剩余。已知:将氧化还原反应设计成原电池时会加快反应速率,则在本实验中,加入几滴
时,加入几滴硫酸铜溶液,生成氢气的速率明显加快,并且反应结束后容器中有少量红色固体剩余。已知:将氧化还原反应设计成原电池时会加快反应速率,则在本实验中,加入几滴 溶液可以加快生成氢气的速率的原因是
溶液可以加快生成氢气的速率的原因是(6)实验室中现有
 、
、 、
、 、
、 等4种溶液,可与上述实验中
等4种溶液,可与上述实验中 溶液起相似作用的是
溶液起相似作用的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学反应中的能量和速率变化对生产生活有着重要意义。某研究小组同学进行下列探究活动。
(1)甲同学探究反应2Al+3H2SO4(稀)=Al2(SO4)3+3H2↑中的能量变化。向装有铝片的试管中加入1 mol·L-1的H2SO4,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为___________ (填“放热”或“吸热”)反应。
②下列措施中,能加快氢气生成速率的是___________ (填字母标号)。
a.加CuSO4溶液 b.将稀H2SO4改成浓硫酸
c.加Na2SO4溶液 d.将铝片换成铝粉
(2)乙同学对可逆反应m X(g) +nY(g) pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
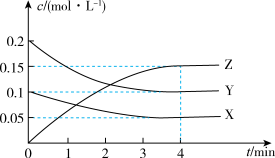
①0~4 min内的反应速率v(Z)=___________ 。
②m:n:p=___________ 。
③该反应达最大限度时Y的转化率___________ 。
④下列描述能表示该反应达平衡状态的是___________ (填字母标号)。
A.容器中Y与Z的物质的量相等
B.容器内气体的密度不再发生改变
C.单位时间内生成n molY的同时生成pmolZ
D. X的体积分数不再改变
E.容器内气体的平均相对分子质量不随时间的变化而变化
(1)甲同学探究反应2Al+3H2SO4(稀)=Al2(SO4)3+3H2↑中的能量变化。向装有铝片的试管中加入1 mol·L-1的H2SO4,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为
②下列措施中,能加快氢气生成速率的是
a.加CuSO4溶液 b.将稀H2SO4改成浓硫酸
c.加Na2SO4溶液 d.将铝片换成铝粉
(2)乙同学对可逆反应m X(g) +nY(g)
 pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
①0~4 min内的反应速率v(Z)=
②m:n:p=
③该反应达最大限度时Y的转化率
④下列描述能表示该反应达平衡状态的是
A.容器中Y与Z的物质的量相等
B.容器内气体的密度不再发生改变
C.单位时间内生成n molY的同时生成pmolZ
D. X的体积分数不再改变
E.容器内气体的平均相对分子质量不随时间的变化而变化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学使我们的生活更加美好。使用自热材料的暖贴、自热食品极大的方便了人们的生活。
(1)自热材料是利用化学反应原理,将_____ 能转化为热能供人们使用。一般利用原电池原理来_____ (“加快”或“减慢”)放热速度。
(2)暖贴中自热材料的主要化学成分有:铁粉、炭粉、氯化钠固体、其他辅助成分及保温材料等,并用可控制氧气透过速率的无纺布包装。在工作时,铁粉与炭粉形成原电池反应,该反应过程中的能量变化关系图中,正确的是______ 。

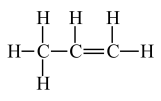
(3)控制适当的氧气透过速率,使暖贴保持一个适合人体的温度,无纺布非常重要。制作无纺布的原料为丙烯,丙烯结构如图。关于丙烯分子内 的相互作用有______ 。
A.共价键 B.离子键 C.范德华力 D.氢键
(4)自热食品的自热材料中,除有暖贴当中的成分外,还有生石灰、铝粉、碳酸钠等,仍用无纺布包装。使用时先加适量的水。开始时有放热的非氧化还原反应发生,其化学方程式为_____ 。然后会形成强碱性溶液,并进一步发生剧烈反应,并产生一种易燃易爆的气体,大量放热,将食品煮熟。该反应的离子方程式为:_______ 。商家为保证迅速放热,采取了以下哪些加速反应的措施:_____ 。
①形成原电池反应 ②将铝粒制成铝粉 ③增大压强 ④使用催化剂
(1)自热材料是利用化学反应原理,将
(2)暖贴中自热材料的主要化学成分有:铁粉、炭粉、氯化钠固体、其他辅助成分及保温材料等,并用可控制氧气透过速率的无纺布包装。在工作时,铁粉与炭粉形成原电池反应,该反应过程中的能量变化关系图中,正确的是

(3)控制适当的氧气透过速率,使暖贴保持一个适合人体的温度,无纺布非常重要。制作无纺布的原料为丙烯,丙烯结构如图。关于丙烯分子

A.共价键 B.离子键 C.范德华力 D.氢键
(4)自热食品的自热材料中,除有暖贴当中的成分外,还有生石灰、铝粉、碳酸钠等,仍用无纺布包装。使用时先加适量的水。开始时有放热的非氧化还原反应发生,其化学方程式为
①形成原电池反应 ②将铝粒制成铝粉 ③增大压强 ④使用催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请用所学的化学知识解释下列反应。
(1)Ag2O-Zn-KOH 组成的纽扣电池,正极区 pH 增大,请用电极反应式解释:______________ 。
(2)炒过菜的铁锅不及时清洗(未洗净残液中含 NaCl),不久会生锈,写出正极电极反应 式:_____________ ,其锈蚀过程属于_____ (填“析氢腐蚀”或“吸氧腐蚀”)。
(3)CuO 中含 Fe2O3,要想用此化合物制得纯净的 CuCl2 固体涉及流程为:

①物质 a 为加入_____ 把 pH 调到_____ 。
②操作 c 为在_____ 条件下加热蒸干得固体 CuCl2。
(4)C2H6在足量 O2中完全燃烧,当转移 7 mol e-时放热 a kJ,写出表示 C2H6 燃烧热的热化学方程式:_____ 。
(5)CO2 中混有 HCl,可用饱和 NaHCO3 溶液吸收 HCl,请用平衡移动原理解释原因_____
(1)Ag2O-Zn-KOH 组成的纽扣电池,正极区 pH 增大,请用电极反应式解释:
(2)炒过菜的铁锅不及时清洗(未洗净残液中含 NaCl),不久会生锈,写出正极电极反应 式:
(3)CuO 中含 Fe2O3,要想用此化合物制得纯净的 CuCl2 固体涉及流程为:

| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀 pH | 1.9 | 4.7 |
| 完全沉淀 pH | 3.2 | 6.7 |
①物质 a 为加入
②操作 c 为在
(4)C2H6在足量 O2中完全燃烧,当转移 7 mol e-时放热 a kJ,写出表示 C2H6 燃烧热的热化学方程式:
(5)CO2 中混有 HCl,可用饱和 NaHCO3 溶液吸收 HCl,请用平衡移动原理解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)写出下列物质的电离方程式:
①H2S:_______
②NaHCO3溶于水:_______ ③NaHSO4溶于水:_______
(2)下出下列盐的水解方程式(离子方程式):
①NH4Cl:_______
②明矾净水原理(只写相应离子的水解方程式):_______
③泡沫灭火器(硫酸铝和碳酸氢钠)的灭火原理:_______
(3)写出难溶电解质的溶度积表达式。Mg(OH)2:_______
(4)下出下列反应方程式:
①钢铁发生吸氧腐蚀的正极反应式:_______
②氢氧燃料电池,H2SO4做电解质溶液,正极反应式:_______
③电解饱和食盐水的总反应方程式:_______
①H2S:
②NaHCO3溶于水:
(2)下出下列盐的水解方程式(离子方程式):
①NH4Cl:
②明矾净水原理(只写相应离子的水解方程式):
③泡沫灭火器(硫酸铝和碳酸氢钠)的灭火原理:
(3)写出难溶电解质的溶度积表达式。Mg(OH)2:
(4)下出下列反应方程式:
①钢铁发生吸氧腐蚀的正极反应式:
②氢氧燃料电池,H2SO4做电解质溶液,正极反应式:
③电解饱和食盐水的总反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示3套实验装置,分别回答下列问题。
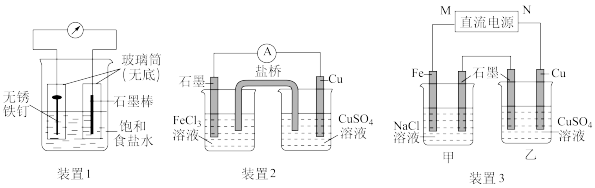
(1)装置1石墨棒电极反应式为___________ 。
(2)装置2一段时间后右池溶液中c(Cu2+)___________ (填“增大”、“减小”或“不变”),若该装置的盐桥中盛装的是NH4NO3的琼脂溶液,则盐桥中的___________ 离子(填“ ”或“
”或“ ”)向硫酸铜溶液迁移。
”)向硫酸铜溶液迁移。
(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。观察到乙烧杯的石墨电极上有气泡生成。
①电源的M端为___________ 极;甲烧杯中铁电极的电极反应式为___________ 。
②乙烧杯中电解反应的离子方程式为___________ 。
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为___________ mL。

(1)装置1石墨棒电极反应式为
(2)装置2一段时间后右池溶液中c(Cu2+)
 ”或“
”或“ ”)向硫酸铜溶液迁移。
”)向硫酸铜溶液迁移。(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。观察到乙烧杯的石墨电极上有气泡生成。
①电源的M端为
②乙烧杯中电解反应的离子方程式为
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为
您最近一年使用:0次