化学反应中的能量和速率变化对生产生活有着重要意义。某研究小组同学进行下列探究活动。
(1)甲同学探究反应2Al+3H2SO4(稀)=Al2(SO4)3+3H2↑中的能量变化。向装有铝片的试管中加入1 mol·L-1的H2SO4,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为___________ (填“放热”或“吸热”)反应。
②下列措施中,能加快氢气生成速率的是___________ (填字母标号)。
a.加CuSO4溶液 b.将稀H2SO4改成浓硫酸
c.加Na2SO4溶液 d.将铝片换成铝粉
(2)乙同学对可逆反应m X(g) +nY(g) pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
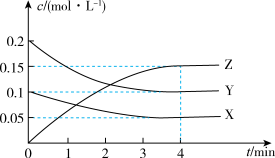
①0~4 min内的反应速率v(Z)=___________ 。
②m:n:p=___________ 。
③该反应达最大限度时Y的转化率___________ 。
④下列描述能表示该反应达平衡状态的是___________ (填字母标号)。
A.容器中Y与Z的物质的量相等
B.容器内气体的密度不再发生改变
C.单位时间内生成n molY的同时生成pmolZ
D. X的体积分数不再改变
E.容器内气体的平均相对分子质量不随时间的变化而变化
(1)甲同学探究反应2Al+3H2SO4(稀)=Al2(SO4)3+3H2↑中的能量变化。向装有铝片的试管中加入1 mol·L-1的H2SO4,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为
②下列措施中,能加快氢气生成速率的是
a.加CuSO4溶液 b.将稀H2SO4改成浓硫酸
c.加Na2SO4溶液 d.将铝片换成铝粉
(2)乙同学对可逆反应m X(g) +nY(g)
 pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
①0~4 min内的反应速率v(Z)=
②m:n:p=
③该反应达最大限度时Y的转化率
④下列描述能表示该反应达平衡状态的是
A.容器中Y与Z的物质的量相等
B.容器内气体的密度不再发生改变
C.单位时间内生成n molY的同时生成pmolZ
D. X的体积分数不再改变
E.容器内气体的平均相对分子质量不随时间的变化而变化
更新时间:2022-07-10 20:27:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂,它能将工厂排放的CO2以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入Na2CO3溶液,其原理如图1所示。

(1)这种微胶囊吸收CO2的原理是___________ (用离子方程式解释),此过程是________ (填“吸收”或“放出”)能量的过程。
(2)生活中,经常用热的碳酸钠溶液清洗油污,结合化学用语,用必要的文字说明原因:________ 。
(3)太阳能热电化学(STEP)生产水泥法可使二氧化碳排放量为零。基本原理如图2所示。利用熔融的碳酸钠为电解质,碳酸钙先分解成为CaO和CO2,最后得到石灰(CaO)、碳和氧气。石墨电极的电极反应式是________ 。


(1)这种微胶囊吸收CO2的原理是
(2)生活中,经常用热的碳酸钠溶液清洗油污,结合化学用语,用必要的文字说明原因:
(3)太阳能热电化学(STEP)生产水泥法可使二氧化碳排放量为零。基本原理如图2所示。利用熔融的碳酸钠为电解质,碳酸钙先分解成为CaO和CO2,最后得到石灰(CaO)、碳和氧气。石墨电极的电极反应式是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知:
①
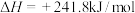
②
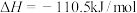
③
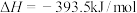
请填写下列空白。
(1)上述反应中属于吸热反应的是___________ (填序号)。
(2)表示C的燃烧热的热化学方程式为___________ (填序号)。
(3)10g 完全燃烧生成水蒸气,放出的热量为
完全燃烧生成水蒸气,放出的热量为___________ 。
①

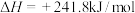
②

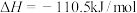
③

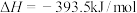
请填写下列空白。
(1)上述反应中属于吸热反应的是
(2)表示C的燃烧热的热化学方程式为
(3)10g
 完全燃烧生成水蒸气,放出的热量为
完全燃烧生成水蒸气,放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】任何化学反应都伴随着能量的变化,化学能可转化为热能、电能等。回答下列有关问题:
(1)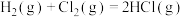 的反应过程如图所示:
的反应过程如图所示:______ (填“放热”或“吸热”)反应,生成 吸收或放出的热量为
吸收或放出的热量为______ 。
(2)下列变化中属于吸热反应的是______ (填标号)。
①液态水汽化 ②生石灰与水反应生成熟石灰
③ ④
④ 与固体
与固体 混合
混合
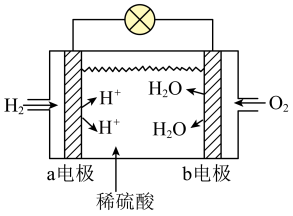
(3)氢气燃料电池在北京冬奥会上得到广泛应用,下图是一种氢气燃料电池的工作原理示意图:______ ,发生了______ 反应(填“氧化”或“还原”):a电极是原电池的______ (填“正极”或“负极”),若该极改为通入 ,其电极反应式为
,其电极反应式为____________ 。
(4)为了验证Fe与Cu的还原性强弱,下图中能达到实验目的的装置是______ (填标号),其正极的电极反应式为______ ;若构建该原电池时两个电极的质量相等,当导线中通过0.2 mol电子时,理论上两个电极的质量差为______ g。
(1)
 的反应过程如图所示:
的反应过程如图所示:
 吸收或放出的热量为
吸收或放出的热量为(2)下列变化中属于吸热反应的是
①液态水汽化 ②生石灰与水反应生成熟石灰
③
 ④
④ 与固体
与固体 混合
混合(3)氢气燃料电池在北京冬奥会上得到广泛应用,下图是一种氢气燃料电池的工作原理示意图:
 ,其电极反应式为
,其电极反应式为(4)为了验证Fe与Cu的还原性强弱,下图中能达到实验目的的装置是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=___________ 。平衡时H2的转化率为___________ %。
(2)平衡后,若提高H2的转化率,可以采取的措施有___________。
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)  2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较K1、K2的大小,K1___________ K2(填“<”“>”或“=”);
②400℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为___________ 。当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正___________ v(N2)逆(填“<”“>”或“=”)。
③下列可用于判断N2(g)+3H2(g) 2NH3(g)反应达到平衡状态的依据是
2NH3(g)反应达到平衡状态的依据是___________ 。
A.容器中气体压强不再变化
B.容器中气体的密度不再变化
C.容器中气体平均摩尔质量不再变化
D.3v(H2) 正=2v(NH3) 逆
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=(2)平衡后,若提高H2的转化率,可以采取的措施有___________。
| A.加了催化剂 | B.增大容器体积 |
| C.降低反应体系的温度 | D.加入一定量N2 |
 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②400℃时,反应2NH3(g)
 N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为③下列可用于判断N2(g)+3H2(g)
 2NH3(g)反应达到平衡状态的依据是
2NH3(g)反应达到平衡状态的依据是A.容器中气体压强不再变化
B.容器中气体的密度不再变化
C.容器中气体平均摩尔质量不再变化
D.3v(H2) 正=2v(NH3) 逆
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.将1.0molCH4和3.0molH2O(g)通入反应室(容积为100L)中,在一定条件下发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)ΔH>0,CH4的转化率与温度、压强的关系如图所示:
CO(g)+3H2(g)ΔH>0,CH4的转化率与温度、压强的关系如图所示:

(1)已知压强p1,温度为100℃时反应I达到平衡所需的时间为5min,则用H2表示的平均反应速率为___ 。
(2)图中的p1___ p2(填“<”、“>”或“=”)。
II.钼及其合金在冶金、环保和航天等方面有着广泛的应用。碳酸钠作固硫剂并用氢还原辉钼矿的原理为:MoOS2(s)+4H2(g)+2Na2CO3(s) MoO(s)+2CO(g)+4H2O(g)+2Na2S(s)△H。实验测得平衡时的有关变化曲线如图所示。
MoO(s)+2CO(g)+4H2O(g)+2Na2S(s)△H。实验测得平衡时的有关变化曲线如图所示。

(3)图中A点对应的平衡常数Kp=___ (已知A点压强为0.lMPa,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 CO(g)+3H2(g)ΔH>0,CH4的转化率与温度、压强的关系如图所示:
CO(g)+3H2(g)ΔH>0,CH4的转化率与温度、压强的关系如图所示:
(1)已知压强p1,温度为100℃时反应I达到平衡所需的时间为5min,则用H2表示的平均反应速率为
(2)图中的p1
II.钼及其合金在冶金、环保和航天等方面有着广泛的应用。碳酸钠作固硫剂并用氢还原辉钼矿的原理为:MoOS2(s)+4H2(g)+2Na2CO3(s)
 MoO(s)+2CO(g)+4H2O(g)+2Na2S(s)△H。实验测得平衡时的有关变化曲线如图所示。
MoO(s)+2CO(g)+4H2O(g)+2Na2S(s)△H。实验测得平衡时的有关变化曲线如图所示。
(3)图中A点对应的平衡常数Kp=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】阅读下列材料,并完成相应填空
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上利用H2和CO2合成二甲醚的反应如下:6H2(g) +2CO2(g) CH3OCH3(g)+3H2O(g)。已知该反应平衡常数(K)与温度(T)的关系如图所示。
CH3OCH3(g)+3H2O(g)。已知该反应平衡常数(K)与温度(T)的关系如图所示。

(1)一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是________ (选填编号)。
a c(H2)与c(H2O)的比值保持不变 b 单位时间内有2mol H2消耗时有1mol H2O生成
c 容器中气体密度不再改变 d 容器中气体压强不再改变
(2)温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将__________ (填“变大”、“变小”或“不变”,下同),混合气体的平均式量将__________ 。
(3) 一定温度和压强下,往体积为20L的容器中通入一定物质的量的H2与CO2,达到平衡时,容器中含有0.1mol二甲醚。计算H2的平均反应速率:_________ (用字母表示所缺少的物理量并指明其含义)。
(4)工业上为提高CO2的转化率,采取方法可以是__________ (选填编号)。
a 使用高效催化剂 b 增大体系压强
c 及时除去生成的H2O d 增加原料气中CO2的比例
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上利用H2和CO2合成二甲醚的反应如下:6H2(g) +2CO2(g)
 CH3OCH3(g)+3H2O(g)。已知该反应平衡常数(K)与温度(T)的关系如图所示。
CH3OCH3(g)+3H2O(g)。已知该反应平衡常数(K)与温度(T)的关系如图所示。
(1)一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是
a c(H2)与c(H2O)的比值保持不变 b 单位时间内有2mol H2消耗时有1mol H2O生成
c 容器中气体密度不再改变 d 容器中气体压强不再改变
(2)温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将
(3) 一定温度和压强下,往体积为20L的容器中通入一定物质的量的H2与CO2,达到平衡时,容器中含有0.1mol二甲醚。计算H2的平均反应速率:
(4)工业上为提高CO2的转化率,采取方法可以是
a 使用高效催化剂 b 增大体系压强
c 及时除去生成的H2O d 增加原料气中CO2的比例
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为____ 。
(2)反应前A的物质的量浓度是____ 。
(3)10 s末,生成物D的浓度为__ 。
(4)A与B的平衡转化率之比为___ 。
(5)反应过程中容器内气体的平均相对分子质量变化是_ (填“增大”、“减小”或“不变”,下同),气体的密度变化是___ 。
(6)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度____ ;②增大A的浓度_____ ;
③恒容下充入氖气________ 。
(7)下列叙述能说明该反应已达到化学平衡状态的是(填标号)___ ;
A.v(B)=2v(C)
B.容器内压强不再发生变化
C.A的体积分数不再发生变化
D.器内气体密度不再发生变化
E.相同时间内消耗n mol的B的同时生成2n mol的D
(8)将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s) NH3(g)+HI(g),2HI(g)
NH3(g)+HI(g),2HI(g)  H2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则NH3的浓度为
H2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则NH3的浓度为___ 。
 2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。(1)用C表示10 s内反应的平均反应速率为
(2)反应前A的物质的量浓度是
(3)10 s末,生成物D的浓度为
(4)A与B的平衡转化率之比为
(5)反应过程中容器内气体的平均相对分子质量变化是
(6)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度
③恒容下充入氖气
(7)下列叙述能说明该反应已达到化学平衡状态的是(填标号)
A.v(B)=2v(C)
B.容器内压强不再发生变化
C.A的体积分数不再发生变化
D.器内气体密度不再发生变化
E.相同时间内消耗n mol的B的同时生成2n mol的D
(8)将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s)
 NH3(g)+HI(g),2HI(g)
NH3(g)+HI(g),2HI(g)  H2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则NH3的浓度为
H2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则NH3的浓度为
您最近一年使用:0次
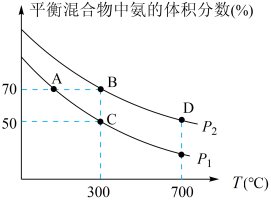
【推荐2】氨在国民经济中占有重要地位,在科学技术和生产中有重要应用。合成氨反应起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。
(1)恒压时, 反应一定达到平衡状态的标志是
反应一定达到平衡状态的标志是______ (选填字母)
A. 和
和 的转化率相等
的转化率相等
B.反应体系密度保持不变
C.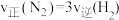
D.断开3molH—H键的同时断开6molN—H键
(2)
_____  (填“>”“=”或“<”,下同);反应的平衡常数:B点
(填“>”“=”或“<”,下同);反应的平衡常数:B点_____ C点。
(3)C点 的转化率为
的转化率为_______ 。(精确到小数点后一位)
(4)为提高合成氨的衡产率,下列可以采取的措施有____________ 。
A.增大压强 B.升高温度 C.使用铁触媒 D.将生成的 及时从混合气体中分离出去
及时从混合气体中分离出去

(1)恒压时,
 反应一定达到平衡状态的标志是
反应一定达到平衡状态的标志是A.
 和
和 的转化率相等
的转化率相等 B.反应体系密度保持不变
C.
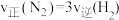
D.断开3molH—H键的同时断开6molN—H键
(2)

 (填“>”“=”或“<”,下同);反应的平衡常数:B点
(填“>”“=”或“<”,下同);反应的平衡常数:B点(3)C点
 的转化率为
的转化率为(4)为提高合成氨的衡产率,下列可以采取的措施有
A.增大压强 B.升高温度 C.使用铁触媒 D.将生成的
 及时从混合气体中分离出去
及时从混合气体中分离出去
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】近年全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。
I.氮氧化物的研究
(1)一定条件下,将2mol 与2mol
与2mol 置于恒容密闭容器中发生反应:
置于恒容密闭容器中发生反应: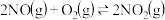 。下列状态能说明该反应达到化学平衡的是
。下列状态能说明该反应达到化学平衡的是___________ (填字母编号)。
a. 的转化率保持不变
的转化率保持不变
b.混合气体的密度保持不变
c. 和
和 的物质的量之比保持不变
的物质的量之比保持不变
d. 的消耗速率和
的消耗速率和 的消耗速率相等
的消耗速率相等
II.碳氧化物研究
(2)工业上,常采用氧化还原方法处理尾气中的CO、NO。
氧化法:沥青混凝土可作为反应 的催化剂。下图表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
的催化剂。下图表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。

①在a、b、c、d四点中,一定未达到平衡状态的是___________ 。
②已知c点时容器中 浓度为
浓度为 ,则50℃时,在α型沥青混凝土中CO转化反应的平衡常数K=
,则50℃时,在α型沥青混凝土中CO转化反应的平衡常数K=___________ (用含x的代数式表示)。
③CO转化反应的平衡常数: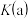
___________ 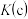 。
。
④在均未达到平衡状态时,同温下___________ (填“α”或“β”)型沥青混凝土中CO转化速率大。
⑤e点转化率出现突变的原因可能是___________ 。
I.氮氧化物的研究
(1)一定条件下,将2mol
 与2mol
与2mol 置于恒容密闭容器中发生反应:
置于恒容密闭容器中发生反应: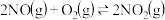 。下列状态能说明该反应达到化学平衡的是
。下列状态能说明该反应达到化学平衡的是a.
 的转化率保持不变
的转化率保持不变b.混合气体的密度保持不变
c.
 和
和 的物质的量之比保持不变
的物质的量之比保持不变d.
 的消耗速率和
的消耗速率和 的消耗速率相等
的消耗速率相等II.碳氧化物研究
(2)工业上,常采用氧化还原方法处理尾气中的CO、NO。
氧化法:沥青混凝土可作为反应
 的催化剂。下图表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
的催化剂。下图表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
①在a、b、c、d四点中,一定未达到平衡状态的是
②已知c点时容器中
 浓度为
浓度为 ,则50℃时,在α型沥青混凝土中CO转化反应的平衡常数K=
,则50℃时,在α型沥青混凝土中CO转化反应的平衡常数K=③CO转化反应的平衡常数:
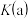
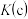 。
。④在均未达到平衡状态时,同温下
⑤e点转化率出现突变的原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】影响化学反应速率的因素主要取决于反应物本身的性质,还包括温度、浓度、压强、催化剂、接触面积等外界因素,根据所学知识分析下列实验,回答有关问题。
利用Al、Fe、Mg和2mol/L的稀硫酸分别反应,甲同学设计实验方案研究影响反应速率的因素。
(1)①甲同学的实验目的是____ 。
②要得出正确的实验结论,还需控制的实验步骤的条件②是____ 。
(2)乙同学研究用Fe和稀硫酸反应制取氢气,发现加入少量硫酸铜溶液可加快氢气的生成速率。
①上述实验中发生反应的化学方程式有:____ 。
②硫酸铜溶液可以加快氢气生成速率的原因是____ 。
③实验室中现有Na2SO4、MgSO4、AgNO3、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是____ 。
④要加快上述实验中气体产生的速率,还可采取的措施有___ (答两种)。
利用Al、Fe、Mg和2mol/L的稀硫酸分别反应,甲同学设计实验方案研究影响反应速率的因素。
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol/L硫酸于试管中;②分别在____,投入____相同的Al、Fe、Mg | 反应快慢:Mg>Al>Fe | 反应物的性质越活泼,反应速率越快 |
(1)①甲同学的实验目的是
②要得出正确的实验结论,还需控制的实验步骤的条件②是
(2)乙同学研究用Fe和稀硫酸反应制取氢气,发现加入少量硫酸铜溶液可加快氢气的生成速率。
①上述实验中发生反应的化学方程式有:
②硫酸铜溶液可以加快氢气生成速率的原因是
③实验室中现有Na2SO4、MgSO4、AgNO3、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是
④要加快上述实验中气体产生的速率,还可采取的措施有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定量的盐酸和过量的锌粒反应产生氢气,为了减慢反应速率,又不影响产生的氢气的总量,下列措施可行的是________ ①加入NaOH固体 ②加入一定量的水 ③加入少量硫酸钠溶液 ④加入少量硫酸铜溶液 ⑤加入CH3COONa固体 ⑥加入KNO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有___________ ;___________ :
(2)下图表示一定量的锌与足量的稀硫酸反应生成氢气的关系,若在反应液中加入少量硫酸铜固体,请在下图中用虚线表示这一关系的变化:___________ 。 、
、 、
、 、
、 等4种溶液,可与上述实验中
等4种溶液,可与上述实验中 溶液起相似作用的是
溶液起相似作用的是___________ ;
(4)要加快上述实验中气体产生的速率,还可采取的措施有:___________ 、___________ (答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量 粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
①请完成此实验设计,其中: =
=___________ ,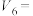
___________ ,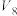 =
=___________ 。
②反应一段时间后,实验E中的金属呈___________ 色;
③该同学最后得出的结论为:当加入少量 溶液时,生成氢气的速率会大大提高,但当加入的
溶液时,生成氢气的速率会大大提高,但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析当加入少量
溶液超过一定量时,生成氢气的速率反而会下降。请分析当加入少量 溶液时,生成氢气速率会大大提高的主要原因
溶液时,生成氢气速率会大大提高的主要原因___________ ;当加入的 溶液超过一定量时,氢气生成速率下降的主要原因
溶液超过一定量时,氢气生成速率下降的主要原因___________ 。
(1)上述实验中发生反应的离子方程式有
(2)下图表示一定量的锌与足量的稀硫酸反应生成氢气的关系,若在反应液中加入少量硫酸铜固体,请在下图中用虚线表示这一关系的变化:

 、
、 、
、 、
、 等4种溶液,可与上述实验中
等4种溶液,可与上述实验中 溶液起相似作用的是
溶液起相似作用的是(4)要加快上述实验中气体产生的速率,还可采取的措施有:
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量
 粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。| 实验混合溶液 | A | B | C | D | E | F |
 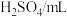 | 40 |  |  |  |  | 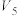 |
饱和 溶液/ 溶液/ | 0 | 0.5 | 2.5 |  | 15 | 30 |
 | 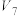 | 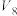 |  | 22.5 | 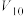 | 0 |
 =
=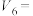
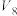 =
=②反应一段时间后,实验E中的金属呈
③该同学最后得出的结论为:当加入少量
 溶液时,生成氢气的速率会大大提高,但当加入的
溶液时,生成氢气的速率会大大提高,但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析当加入少量
溶液超过一定量时,生成氢气的速率反而会下降。请分析当加入少量 溶液时,生成氢气速率会大大提高的主要原因
溶液时,生成氢气速率会大大提高的主要原因 溶液超过一定量时,氢气生成速率下降的主要原因
溶液超过一定量时,氢气生成速率下降的主要原因
您最近一年使用:0次



